Spektrometrija v šoli: eksperimenti z izkustvenim pristopom Teach article
Prevod Nataša Gros, Irena Štrumbelj Drusany in Alma Kapun Dolinar. Nataša Gros, Tim Harrison, Irena Štrumbelj Drusany in Alma Kapun Dolinar predstavljajo izbor eksperimentov z enostavnim spektrometrom, razvitim za šolsko uporabo in natančno opisujejo, kako izvesti eno od aktivnosti.

Da bi motivirali dijake z izkustvenim pristopom h kemiji, smo s projektnimi partnerji razvili zbirko poskusov z majhnimi, nizko cenovnimi spektrometri. V projektu uporabljamo enostaven spektrometer, ki ga je razvil eden od projektnih partnerjev (Nataša Gros). Spektrometer je mogoče nadgraditi v druge analizne instrumente, kot sta npr. plinski in tekočinski kromatograf, kar razširja področje šolskih eksperimentov (več informacij je na spletni strani projektaw1). Manjše število spektrometrov je na razpolago šolam za izposojo.
Kako delujejo spektrometri
V spektrometru bela svetloba, ki izhaja iz svetlobnega vira (žarnice), vstopa v monokromator, iz katerega izstopa le svetloba izbrane valovne dolžine (barve), ki nato potuje skozi raztopino, ki je v optični celici ali kiveti (slika 1). Raztopina absorbira del svetlobe in detektor zazna zmanjšanje moči svetlobe (kar lahko prikaže kot absorbanco). Bolj intenzivno, ko je raztopina obarvana, višjo absorbanco izmerimo.

Slika: Nicola Graf
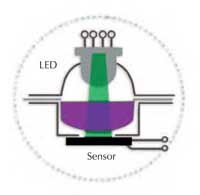
of the Spektra spectrometer
Image courtesy of Nataša Gros
V praksi so najpogostejše kivete z dolžino optične poti 1 cm, ki zahtevajo najmanj 3 mL raztopine za uspešno merjenje. Temeljni cilj konvencionalnih spektrometrov je pravilno in ponovljivo merjenje absorbance. Izbira valovne dolžine mora biti čimbolj pravilna in svetloba čim bolj monokromatska (z ozkim pasom valovnih dolžin). Zgradba instrumenta je zato zapletena in ne zelo očitna povprečnemu uporabniku; instrument pa je razmeroma drag.
Temeljni cilj pri razvoju spektrometra SpektraTM je bil izdelati nizkocenovni, prenosni in robustni instrument z nazorno in lahko razumljivo zgradbo in delovanjem, ki bo omogočal majhno porabo reagentov ter poenostavljeni eksperimentalni pristop (Gros, 2004). Ta spektrometer, ki je v osnovi namenjen uporabi v izobraževanju, zlasti uvajanju konceptov, je uporaben tudi za kvantitativne in semikvantitativne določitve sestavin v realnih vzorcih.
Spektrometer SpektraTM sestavljata dva optična elementa: tribarvna sveteča dioda (LED) in svetlobni senzor. Izbiramo lahko med modro (430 nm), zeleno (565 nm) in rdečo (625 nm) svetlobo, ki gre neposredno skozi plast tekočine in doseže senzor (slika 2). Najpomembnejši deli (svetilo, merilna komora in senzor) so vsi vidni. Za dijake ali učence instrument ni »črna škatla«; lahko ga je razumeti in upravljati (slika 3, a in b).

spektrometra Spektra. A:
svetlobni vir – LED; B: merilna
komora; C: merilno mesto s
senzorjem na dnu. Kliknite za
povečanje slike
Slika: Nataša Gros

spektrometer. Instrument je
bolj kompakten, (A: svetlobni
vir; B: merilna komora; C:
senzor) vse tri temeljne
komponente so še vedno
vidne. Kliknite za povečavo
slike
Slika: Nataša Gros
Reakcije in meritve potekajo v polimernih podlogah imenovanih blistri, ki so podobni plastični embalaži za tablete, in omogočajo delo z majhnimi volumni (0,35 mL) preiskovanih raztopin, hitro homogeniziranje reagentov, in ustvarjajo majhne volumne odpadnih raztopin. Eksperimentalno delo s spektrometrom SpektraTM je enostavno in varno, ne zahteva posebnih laboratorijskih spretnosti in uporabe steklenega laboratorijskega pribora. Volumni raztopin, ki jih rabimo, so zelo majhni. Kjer je to primerno, je mogoče uporabiti poenostavljen eksperimentaln pristop, ki temelji na odmerjanju kapljic.
Spektrometer je mogoče naročiti onlinew2. Univerza v Bristoluw3, UK, nudi omejeno število spektrometrov Spektra za izposojo učiteljem, ki bi želeli preizkusiti eksperimente s svojimi dijaki ali razviti druge aplikacije. V Sloveniji se lahko obrnete na slovenske avtorje. Učitelji, ki imajo raje konvencionalne instrumente, lahko uporabijo kolorimeter Mystrica, ki uporablja normalne kivete in je poceni ter dobre kakovostiw4.
Eksperimenti iz spektrometrije z izkustvenim pristopom
V okviru projekta je bila razvita vrsta praktičnih spektrometričnih aktivnosti, ki vzpodbujajo zanimanje za naravoslovje, in navdihujejo morebitne bodoče naravoslovce med dijaki. Te aktivnosti obsegajo tako raznolike teme kot so: analize vod, fizika svetlobe in barv, izpeljava Lambert-Beerovega zakona, kemijsko ravnotežje, okoljske analize, kinetika kemijskih reakcij in analize hraned.
Eksperimenti s področja analize hrane obsegajo spektrometrično določanje ravni železa v vzorcih posušenih zelišč ali moki; vsebnost alkohola v žganju, raven glukoze v marmeladi, vrednotenje barve piva in barve (kakovosti) začimbne paprike, raven fosfata v jabolčnem soku, fosfati in nitriti v mesnih proizvodih; koncentracija kazeina v skuti. Drugi protokol omogoča spremljanje procesa alkoholnega vrenja.
Navodila za določanje ravni glukoze v marmeladi predstavljamo tukaj; podrobni postopki za vse druge eksperimente – vključno s tistimi, ki so primerni za popularizacijo naravoslovja med osnovnošolci – so na spletni strani projektaw1. Na spletni strani so tudi napotki, kako lahko spektrometer SpektraTM nadgradimo v plinski ali tekočinski kromatograf in kakšne aktivnosti lahki izvajamo z njima (več v Gros & Vrtačnik, 2005).
Spektrometrično določanje količine glukoze v marmeladi
V večjem številu reakcij med sladkorji in različnimi reagenti nastanejo obarvani produkti. Intenzivnost barve raztopine je odvisna od koncentracije sladkorja v začetni raztopini. Absorbanco raztopine vzorca lahko izmerimo in jo primerjamo z absorbanco standardnih raztopini. Koncentracija sladkorja v standardni raztopini je znana. Znanih je manjše število reakcij, pri katerih bi s polisaharidi nastali obarvani produkti. V večini reakcij, pri katerih nastanejo obarvani produkti, sodelujejo enostavni sladkorji, običajno reducirajoči sladkorji (glej okvir).
Določanje količine glukoze je bilo izbrano, ker dijaki vedo dovolj o sladkorjih. Metoda je uporabna za določanje glukoze v vzorcih različnega izvora. Določanje vsebnosti sladkorja v marmeladi lahko uporabijo tudi v industriji kot eno od analiz za kontrolo kakovosti.
V eni od metod za določanje koncentracije sladkorja v marmeladi se med pripravo vzorca hidrolizira večino nereducirajočih sladkorjev (v marmeladi predvsem saharoza) v glukozo. Za hidrolizo se uporabi žveplovo kislino (H2SO4), nato pa se vzorec nevtralizira z natrijevim hidroksidom (NaOH). Med segrevanjem reducirajočih sladkorjev (na primer glukoze in fruktoze) z dodano 3,5-dinitrosalicilno kislino (DNS znana pod imenom 2-hidroksi-3,5-dinitrobenzojska kislina) nastane produkt, ki je rdeče rjave barve. Več informacij v Miller (1959).
Koncentracijo obarvanega kompleksa lahko določimo s spektrometrom, z uporabo modre LED (430 nm): začetno količino sladkorja v vzorcu marmelade lahko odčitamo z umeritvene krivulje, ki jo pripravimo z uporabo raztopin z znanimi koncentracijami glukoze.
Oprema in reagenti
- Spektrometer Spektra ali kakšen drug spektrometer
- Blistri ali kivete
- Pipete
- 100 mL bučka
- Erlenmajerice
- Epruvete
- Tehtnica
- Vodna kopel
- Lij
- Filtrirni papir
- Vzorci marmelad
- DNS reagent (3,5 dinitrosalicilna kislina)
- Žveplova kislina (H2SO4) množinska koncentracija 2 mol/L
- Natrijev hidroksid (NaOH) masni delež 10 %
- Natrijev kalijev tartrat (NaK(CH2OH)2(COO)2.4H2O)
- Glukoza v prahu (C6H12O6)
Priprava raztopin
Reagent DNS: Za pripravo raztopine DNS raztopimo 10 g DNS v 200 mL raztopine NaOH (2 mol/L). Topljenec raztopimo med segrevanjem in stalnim mešanjem. Stabilizator barve pripravimo tako, da 300 g natrijevega kalijevega tartrata raztopimo v 500 mL destilirane vode. Združimo obe raztopini, dobro premešamo in dopolnimo do 1 L z destilirano vodo.
Marmelada (sladkorji) : natehtamo 1–2 g marmelade v erlenmajerico in dodamo 10 mL žveplove kisline. Med mešanjem 20 minut segrevamo v vreli vodni kopeli, da poteče hidroliza. Vzorec pustimo, da se ohladi in hladnemu dodamo12 mL natrijevega hidroksida. Premešamo, prelijemo v 100 mL merilno bučko in dopolnimo z destilirano vodo do 100 mL. Testni vzorec pripravimo tako, da s pipeto prenesemo 10 mL raztopine v drugo merilno bučko in z destilirano vodo dopolnimo do 100 mL ter dobro premešamo.
Marmelada (reducirajoči sladkorji): Natehtamo 3,0 g marmelade v erlenmajerico, dodamo 50 mL destilirane vode, segrejemo in mešamo 10 minut. Prefiltriramo v 100 mL erlenmajerico in dopolnimo z destilirano vodo do 100 mL. Testni vzorec pripravimo tako, da s pipeto prenesemo 10 mL pripravljene raztopine v drugo 100 mL merilno bučko in dopolnimo z destilirano vodo do 100 mL. Dobro premešamo.
Osnovna standardna raztopina glukoze (15 mg/mL): 1,5 g glukoze natehtamo v 100 mL merilno bučko in z destilirano vodo dopolnimo do 100 mL. Dobro premešamo.
Priprava umeritvene krivulje
- Pet merilnih bučk (100 mL) označimo s črkami od A do E. V vsako označeno merilno bučko s pipeto prenesemo toliko osnovne standardne raztopine in destilirane vode kot je zapisano v tabeli 1.
| Merilna bučka | A | B | C | D | E |
|---|---|---|---|---|---|
| Volumen osnovne standardne raztopine glukoze (mL) | 2 | 3 | 6 | 8 | 10 |
| Volumen destilirane vode (mL) | 98 | 97 | 94 | 92 | 90 |
| Masna koncentracija glukoze (mg/mL) | 0.3 | 0.45 | 0.9 | 1.2 | 1.5 |
2. Označite in napolnite šest epruvet kot je zapisano v tabeli 2.
| Oznaka vzorca | Slepa | 1 | 2 | 3 | 4 | 5 |
|---|---|---|---|---|---|---|
| Standardna raztopina glukoze (merilna bučka) | N/A | A | B | C | D | E |
| Volumen standardne raztopine glukoze (mL) | 0 | 1 | 1 | 1 | 1 | 1 |
| Volumen raztopine reagenta DNS (mL) | 1 | 1 | 1 | 1 | 1 | 1 |
| Volumen destilirane vode | 3 | 2 | 2 | 2 | 2 | 2 |

umeritveno krivuljo
Slika: Irena Štrumbelj Drusany
- Epruvete ohladimo in dodamo 6 mL destilirane vode v vsako epruveto.
- S spektrometrom izmerimo transmitance vseh raztopin. Pri tem uporabimo modro LED (430 nm).
Izmerjene vrednosti transmitance so izražene v odstotkih. Da dobimo vrednosti transmitanc, s katerimi lahko računamo, je treba izmerjene vrednosti deliti s 100. Transmitanca je z absorbanco povezna s formulo: A = -log T. Poglej drugi in tretji stolpec v tabeli 3.
Slika na desni prikazuje raztopine za kalibracijo (umeritveno krivuljo). Tudi slepa raztopina, ki ne vsebuje glukoze (samo voda in DNS) je intenzivno obarvana. Transmitance vseh raztopin zato merimo proti destilirani vodi. Specifično absorbanco glukoze izračunamo tako, da od absorbance vsake raztopine odštejemo absorbanco slepe (poglej četrti stolpec v tabeli 3).
6. Narišite graf odvisnosti glukozno specifične absorbance od koncentracije glukoze kot kaže slika 5.
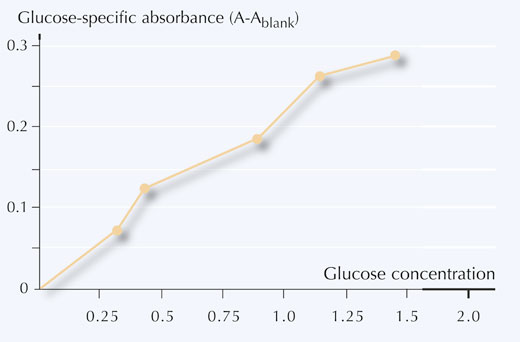
Meritve za vzorce marmelade
Vzorce marmelade obravnavamo podobno kot raztopine glukoze za kalibracijo.
- Za vsak vzorec marmelade, ki ga želimo analizirati, prenesemo 1 mL raztopine vzorca marmelade, pripravljenega kot je opisano v enoti Priprava raztopin, v epruveto in dodamo 1 mL DNS in 2 mL destilirane vode.
- Segrevajte epruvete in njihovo vsebino v vreli vodi 5 minut; DNS bo reagiral s prisotnimi sladkorji in nastal bo rdečerjav produkt.
- Ohladite epruvete, v vsako dodajte 6 ml destilirane vode in vsebino dobro pretresite.
- Z uporabo modre LED (430 nm) izmerite transmitanco (T (%)) vsakega vzorca marmelade. Delite merilne vrednosti s 100, in transmitanco pretvorite v absorbanco po zvezi A = –logT, in uporabite te vrednosti glukozno specifične absorbance (A – Aslepe).
Tabela 4 prikazuje primer izmerjenih transmitanc in izračunanih glukozno specifičnih absorbanc za vzorce.
| Vzorec |
Transmitance (Odčitek T (%) na spektrometru Spektra) |
Absorbanca (A) |
Glukozno specifična absorbanca (A – Aslepe) |
|---|---|---|---|
| 1 | 18.6 | 0.73 | 0.17 |
| 2 | 21.3 | 0.67 | 0.11 |
- Uporabite svojo kalibracijsko krivuljo in pretvorite absorbance (A) v koncentracijo glukoze (mg/mL) v vaših vzorcih.
Če uporabimo primere iz tabele 4, so vrednosti koncentracije, ki jih odčitamo iz kalibracijske krivulje naslednje:
Vzorec 1: 0.8 mg/ml
Vzorec 2: 0.5 mg/ml
6. Iz koncentracije glukoze izračunajte maso glukoze v 1 g vzorca marmelade z uporabo naslednjih zvez:
Masa glukoze (g na 1 g vzorca) = masna koncentracija (mg/mL) x 10 x 100 mL
kjer
je masna koncentracija odčitana iz kalibracijske krivulje
10 je zaradi razredčitve kot je razvidno iz enote Priprava raztopin
100 mL je volumen raztopine vzorca, ki vsebuje 1g vzorca.
V našem primeru,
Vzorec 1: masa glukoze (g na 1 g vzorca) = 0.8 mg/ml x 10 x 100 ml = 0.8 g
Vzorec 2: masa glukoze (g na 1 g vzorca) = 0.5 mg/ml x 10 x 100 ml = 0.5 g.
Izračun predvideva, da je začetna masa vzorca 1 g. Če je vzorca na primer 2 g, moramo prej navedene številke deliti z 2, da dobimo maso glukoze v g na 1 g vzorca.
Reducirajoči in nereducirajoči sladkorji
Reducirajoči sladkorji so aldoze, kot je glukoza, ki ima aldehidno skupino, ki jo je mogoče oksidirati v karboksilno kislino. Pogost kemijski preizkus za dokaz reducirajočih sladkorjev je, da vzorec segrejemo z Benediktovo ali Fehlingovo raztopino, ki vsebuje bakrove(II) ione, ki se reducirajo do bakrovega(I) oksida, ki ga prepoznamo po rjavo-oranžni barvi.
Nereducirajoči sladkorji, kot je sukroza, imajo lahko ketonsko namesto aldehidne funkcionalne skupine, ki ne more reducirati bakrovih(II) ionov, zato ti sladkorji pri uporabi Benediktove ali Fehlingove raztopine ne povzročijo nastanka obarvane oborine.
Zahvala
Avtorji se želijo zahvaliti Evropski komisiji, Generalnemu direktoratu za izobraževanje in kulturo za finančno podporo projektu Izkustvenemu pristopu k analizni kemiji za strokovne šole II (AnalChemVoc II, LLP-LDV-TOI-2008-SI-15) Leonardo da Vinci programa.
References
- Gros N (2004) Spectrometer with microreaction chamber and tri-colour light emitting diode as a light source. Talanta 62: 143-150. doi: 10.1016/S0039-9140(03)00420-X
- Gros N, Vrtačnik M (2005) A small-scale low-cost gas chromatograph. Journal of Chemical Education 82: 291-293. doi: 10.1021/ed082p291
- Miller GL (1959) Use of dinitrosalicylic acid reagent for determination of reducing sugar. Analytical Chemistry 31: 426-428.
- Ta članek je prosto dostopen s spletnega mesta the American Chemical Society na naslovu: http://pubs.acs.org/doi/pdf/10.1021/ac60147a030
Web References
- w1 – Več informacij o projektu je na naslovu: www.kii2.ntf.uni-lj.si/analchemvoc2/file.php/1/HTML/experiments.htm
- w2 – Spektrometer Spektra je mogoče naročiti pri Laboratorijski tehniki Burnik: www.lt-burnik.si/index.php?newlang=english
- w3 – Bristol ChemLabS Univerze v Bristolu (www.chemlabs.bris.ac.uk) nudijo manjše število spektrometrov Spektra za izposojo učiteljem, ki bi želeli preizkusiti eksperimente s svojimi dijaki ali razviti druge aplikacije. Zainteresirani se lahko obrnejo na Tima Harrisona (t.g.harrison@bristol.ac.uk). Za morebitno izposojo v Sloveniji se obrnite na slovenske avtorje članka.
- w4 – več podatkov o Mystrica kolorimetrih je na naslovu: http://mystrica.com/Colorimeter.aspx. Spletno mesto ima tudi vrsto opisov eksperimentov, posebno zanimivi so tisti, ki vključujejo encimske reakcije.
Review
Spektrometrične analize so pomemben del analizne kemije. Profesionalni spektrometri so dragi, zato šolam v mnogih državah niso lahko dostopni. Članek opisuje spektrometer, ki ga je razvila ena od avtoric, da bi spektrometrične analize lahko uporabljala vsaka srednja šola. Na projektni strani so podrobno opisani mnogi šolski eksperimenti s področja spektrometrije, eden od eksperimentov je podrobneje predstavljen v tem članku.
Ta članek bi predlagala za uvajanje analizne kemije v naravoslovne predmete (ne le kemijo, temveč tudi biologijo in okoljske znanosti), posebej za srednje šole, ki nimajo dobro opremljenih laboratorijev. Predlagani pristop je dovolj enostaven in prijazen, da lahko vzpodbudi učitelje in dijake, da preizkusijo tu opisan eksperiment in raziščejo nove.
Učitelji lahko uporabijo članek za razpravo o metodologiji spektrometrije in teoriji spektrometričnih meritev. Eksperimenti s področja analizne kemije odpirajo možnosti za matematično obravnavo dobljenih podatkov in povezavo s statistiko.
Članek je tudi mogoče uporabiti za preverjanje razumevanja, kot sledi v nadaljevanju:
- Opišite postopek za pripravo raztopin za kalibracijsko krivuljo iz osnovne standardne raztopine:
| Bučka | A | B | C | D | E |
|---|---|---|---|---|---|
| Volumen standardne raztopine glukoze (mL) | 2 | 3 | 6 | 8 | 10 |
| Volumen destilirane vode (ml) | 98 | 97 | 94 | ||
| Koncentracija glukoze (mg/mL) | 0.3 | 1.2 | 1.5 |





