L’évolution en action: les pathogènes Understand article
Les pathogènes qui menacent la santé humaine évoluent constamment pour avoir une longueur d’avance sur nos défenses immunitaires. Mais il est désormais possible de retracer ces changements au niveau génétique, même lorsqu’ils sont en train de se…
L’un des moteurs de l’évolution est la sélection naturelle – où certains individus avec une constitution génétique et des adaptations particulières produisent plus de descendants que d’autres dans un environnement donné. Les individus les plus adaptés survivent, les autres meurent.
Science Photo Library/De Angelis, Maurizio
Ce processus de sélection naturelle positive découvert par Darwin – où les traits qui augmentent la survie et le succès reproducteur (ou « fitness ») d’un organisme prédominent dans une population – contribue à la diversité que l’on peut observer chez les espèces existantes. Mais ce processus peut aussi mettre notre propre survie en danger, par exemple à travers la propagation d’infections virales et l’émergence de résistance aux antibiotiques chez des bactéries pathogènes. Cependant, grâce à des expériences ingénieuses (par exemple, voir Bryk, 2017), et des avancées technologiques de séquençage génétique, il est maintenant possible de suivre ce processus de près – non seulement en laboratoire, mais n’importe où dans le monde. Ces progrès sont d’une immense valeur pour comprendre l’évolution des micro-organismes pathogènes.
Dans cet article, nous nous concentrons sur deux études qui examinent l’évolution constante de pathogènes et qui révèlent les changements génétiques – et les facteurs limitants – qui contribuent au processus.
La résistance aux antibiotiques sous les feux des projecteurs
Un exemple classique d’évolution par sélection naturelle positive est l’émergence de résistances aux antibiotiques chez les bactéries. L’utilisation d’antibiotiques applique une pression de sélection sur une population de bactéries, qui mutent et se divisent rapidement. Ainsi, une variante génétique qui protège les bactéries de l’antibiotique reste dans la population, alors que les autres variantes disparaissent.
Ce processus a été filmé par le Dr Michael Baym, un chercheur de l’Université de Harvard aux États-Unis qui a choisi de se battre contre les résistances aux antibiotiques. En 2015, Baym a créé une installation pour visualiser la propagation de bactéries résistantes dans un environnement contenant un antibiotique. Il a utilisé une boîte de Petri rectangulaire géante, 60cm de large sur 120cm de long (une boîte de Petri standard a un diamètre de 9cm), remplie d’agar teint en noir, une substance gélatineuse sur laquelle les bactéries peuvent se multiplier. Il a imprégné l’agar avec une solution antibiotique dont la concentration augmentait par paliers le long de la boîte (figure 1), d’une concentration nulle aux extrémités à 1000 unités d’antibiotique au centre – une concentration normalement suffisante à tuer n’importe quelle bactérie. Il a installé un projecteur et une caméra au-dessus de la boîte, pour que chaque colonie bactérienne soit clairement visible sous forme de point blanc sur le fond noir de l’agar. Puis, il a introduit les bactérie Escherichia coli (E. coli) aux extrémités de la boîte, où il n’y avait pas d’antibiotique – et il a attendu que le processus débute (figure 2).

Kishony Lab, Harvard Medical School and Technion – Israel Institute of Technology
Qu’a-t-il observé? Les E. coli pouvaient se déplacer au sein de la couche supérieure de l’agar, donc lorsque les bactéries n’avaient plus de nourriture à proximité, elles se sont déplacées vers une autre zone (figure 3). Leur croissance était cependant inhibée par l’antibiotique des zones avoisinantes, de manière que seules les bactéries avec une mutation leur permettant d’y survivre puissent continuer à se propager. La première zone à contenir l’antibiotique (avec une concentration d’une unité seulement) s’est faite initialement colonisée par des bactéries mutantes isolées. Celles-ci se sont multipliées, et leurs descendants se sont approprié toute la zone – jusqu’à atteindre le palier suivant, qui contenait une concentration d’antibiotique plus élevée. À la frontière, les bactéries se sont arrêtées jusqu’à l’émergence de nouvelles mutations leur conférant une plus grande tolérance à l’antibiotique.
Ce processus s’est répété à chaque frontière pendant 11 jours jusqu’à ce qu’E. coli ait recouvert la surface entière de la boîte de Petri géante. Les bactéries au centre ont développé une résistance à une concentration d’antibiotique 1000 fois supérieure à celle du bord de la boîte (figure 4). Chaque étape du processus a été filmée : la vidéo est maintenant célèbrew1.

Kishony Lab, Harvard Medical School and Technion – Israel Institute of Technology

Kishony Lab, Harvard Medical School and Technion – Israel Institute of Technology

Kishony Lab, Harvard Medical School and Technion – Israel Institute of Technology
Puisque les chercheurs pouvaient observer la propagation des bactéries en continu, ils ont pu prendre un échantillon des bactéries aux moments critiques où de nouveaux mutants sont apparus. En séquençant leur génomes, ils ont pu déterminer quels changements génétiques ont permis l’évolution de la résistance (figure 5).
Il s’est avéré que beaucoup des mutations concernées sont apparues à plusieurs reprises ; il semble donc que certains chemins vers la résistance sont plus communs que d’autres. De plus, certains gènes mutés n’avaient aucun lien direct avec l’antibiotique, ce qui illustre un point important du développement de résistances : le besoin de s’adapter à l’antibiotique est un fardeau qui pèse sur les voies métaboliques de base. En l’absence d’antibiotique, les bactéries résistantes poussent donc plus lentement que des bactéries non-résistantes. Les mutations ne semblant pas être liées à l’antibiotique étaient nécessaires pour compenser ce fardeau métabolique. Cela pourrait aussi expliquer le ralentissement de la croissance bactérienne aux frontières entre zones de concentrations en antibiotique différentes.
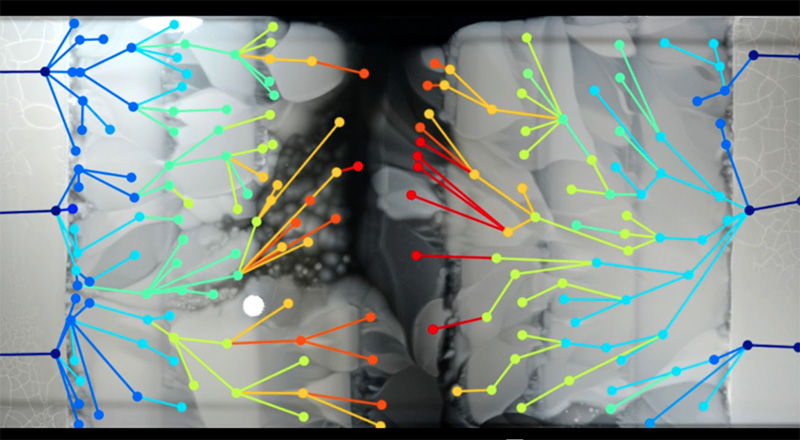
Kishony Lab, Harvard Medical School and Technion – Israel Institute of Technology
Lors d’une étape supplémentaire de cette expérience, Baym et ses collègues ont fait une autre observation cruciale. Lorsque la différence de concentrations entre deux zones était très grande, aucun mutant n’a survécu dans la zone suivante, et la croissance bactérienne s’est complètement arrêtée à la première frontière. Ce phénomène peut s’expliquer de la façon suivante: lorsque la pression sélective des antibiotiques est très élevée dans l’environnement, il est quasiment impossible pour les bactéries de se multiplier, parce que les mécanismes nécessaires à surmonter ce fardeau demandent trop de mutations simultanées – donc les bactéries meurent.
L’épidémie d’Ebola
Un autre exemple d’évolution de pathogènes microbiens qui a fait l’objet d’études approfondies est celle de l’un des pathogènes humains les plus mortels : le virus Ebola. L’épidémie de maladie à virus Ebola de 2013-2015 était la plus grande et la plus longue à ce jour, comptant 28’646 cas et 11’323 morts en juin 2016. La durée de l’épidémie et les technologies de séquençage génétique déployées sur le terrain ont permis aux chercheurs de suivre l’évolution du virus alors qu’il infectait de nouveaux patients.
Menée par les généticiens Dr. Pardis Sabeti (Université d’Harvard), Dr. Jeremy Luban (École de Médecine de l’Université du Massachussetts) et Dr. Andrew Rambaut (Université d’Édimbourg), l’équipe scientifique étudiant Ebola a construit un « arbre généalogique » du virus alors qu’il se propageait à travers l’Afrique de l’Ouest sur une période de deux ans (Park, 2015). Chaque branche de l’arbre représentait une nouvelle souche (ou ensemble de mutations) qui se multipliait et se propageait mieux que d’autres souches. En comparant les génomes viraux échantillonnés chez des patients de différents pays et à différents moments, l’équipe a déterminé que l’origine de la souche principale du virus était en Guinée – et qu’elle a pu se propager au-delà seulement après avoir acquis cinq nouvelles mutations. Alors que le virus se propageait jusqu’à Sierra Leone en avril-mai 2014, une autre mutation est apparue et est devenue bien plus commune dans cette région (Diehl et al., 2016)w2. La nouvelle mutation a d’abord été observée chez un seul patient, mais elle était tellement avantageuse pour le virus que 97% des quelques 200 génomes d’Ebola analysés dans l’étude étaient des descendants de ce mutant. Ce cas représente un exemple remarquable de propagation rapide d’une souche seulement deux ans après son émergence (figure 6).
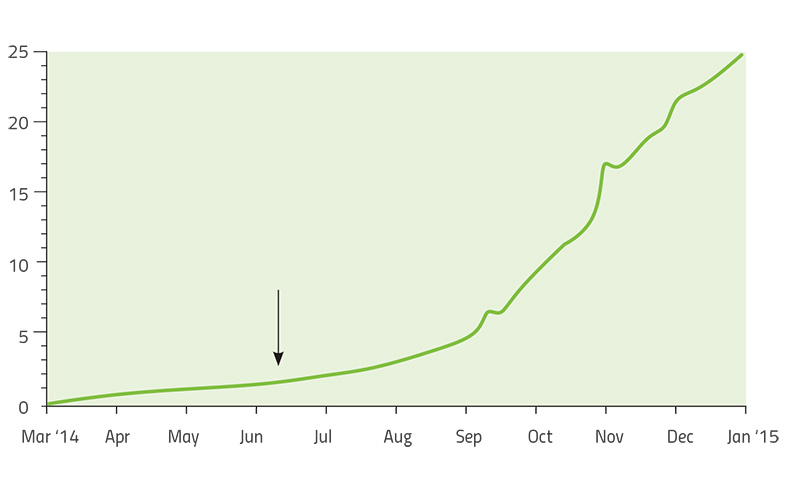
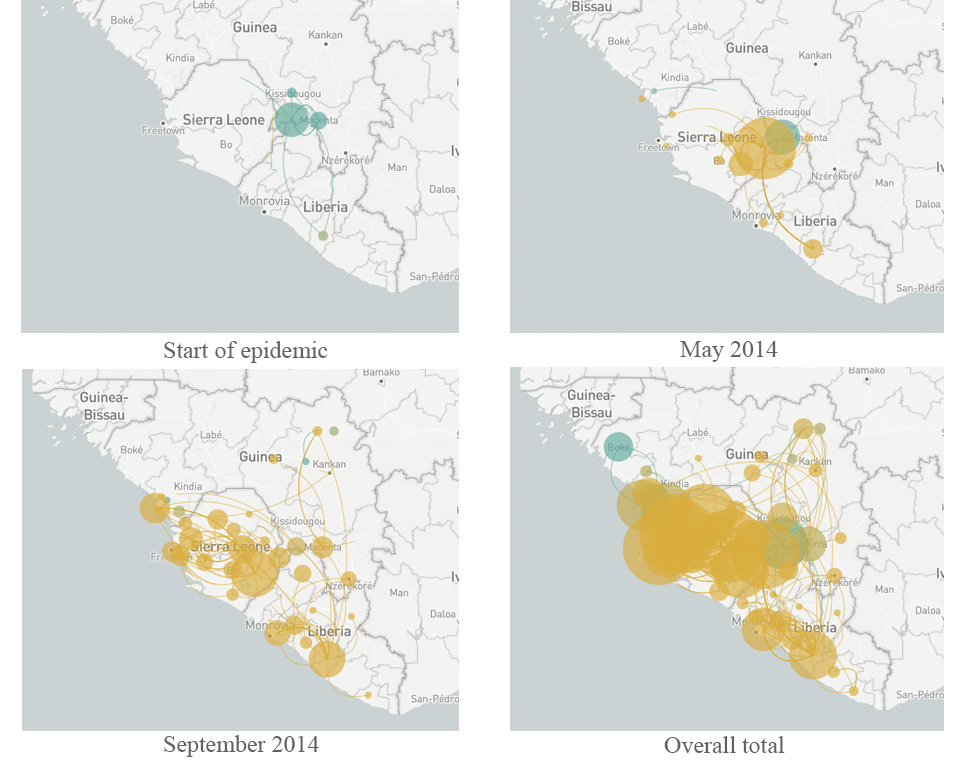
(Source : nextstrain.org)
L’étude a révélé que les modifications de certains gènes du génome d’Ebola étaient bien plus importantes qu’attendues, y compris pour des gènes codant pour des protéines présentes sur la surface extérieure du virus. Ces protéines virales seraient une cible pour les anticorps humains qui combattent l’infection – des changements rapides chez ces protéines découlant de la sélection naturelle permettraient donc au virus d’éviter de se faire neutraliser par l’hôte. Ces gènes sont devenus un sujet d’étude prometteur pour contrecarrer la propagation de nouvelles épidémies. Comprendre davantage les mécanismes de l’évolution permettra aux chercheurs de développer des stratégies efficaces pour combattre de futurs pathogènes.
References
- Bryk J (2017) Evolution in action: the 67 000-generation experiment. Science in School 41: 24-29.
- Park D et al. (2015) Ebola virus epidemiology, transmission, and evolution during seven months in Sierra Leone. Cell 161 1516-1526. doi: 10.1016/j.cell.2015.06.007
- Diehl W E et al. (2016) Ebola virus glycoprotein with increased infectivity dominated the 2013–2016 epidemic. Cell 167 1088–1097. doi: 10.1016/j.cell.2016.10.014
Web References
- w1 – Regardez la vidéo créée par Michael Braym et ses collègues montrant la propagation d’E. coli à travers différentes concentrations d’antibiotique dans la « mega-boîte de petri».
- w2 – Regardez une animation montrant la propagation du virus Ebola, et comment la nouvelle souche qui a émergé autour de mai 2014 l’a affectée.
Resources
- Visitez le site de The Atlantic pour accéder à un article sur l’expérience de Baym et ses implications (en anglais).
- Lisez l’article scientifique dans la revue Science parlant de l’expérience de Baym (en anglais) :
- Baym M et al. (2016) Spatiotemporal microbial evolution on antibiotic landscapes. Science 53: 1147-1151. doi: 10.1126/science.aag0822
- Regardez le TED talk de Pardis Sabeti à propos du combat contre Ebola (en anglais).
- Lisez un article de blog à propos du travail de surveillance d’Ebola, avec des liens vers la couverture médiatique de la recherche et des technologies impliquées.
- Un guide sur Ebola se trouve sur le site de Médecins Sans Frontières (en anglais).
Review
L’un des principaux problèmes avec l’enseignement de l’évolution est sa dimension temporelle. Puisque l’existence humaine est courte comparée à l’échelle temporelle des grands processus évolutifs, le concept de changement au cours du temps est une difficulté basique pour comprendre l’évolution. Des exemples de processus évolutifs qui se produisent sur une période compatible à la perception humaine présente une opportunité pour surmonter ce problème.
L’expérience décrite dans cet article offre une vue d’ensemble des éléments temporels et des mutations qui affectent l’évolution. Les enseignants pourraient utiliser cet article pour enseigner l’évolution, en démontrant que l’évolution peut se produire sur une courte période. L’article se prête également à l’explication du rôle central des mutations au cours de l’évolution, comme source de diversité sur laquelle la sélection naturelle peut agir. De plus, l’expérience implique une situation courante – l’utilisation d’antibiotiques – ce qui la rend facile à comprendre.
Panagiotis K. Stasinakis, enseignant en biologie, 4ème Lycée de Zografou, Grèce





