Evolucija na delu: patogeni Understand article
Patogeni koji ugrožavaju ljudsko zdravlje se neprestano menjaju i tako izmiču mogućnostima naše odbrane. Ali danas možemo da pratimo te promene na genetskom nivou, čak i dok se one odvijaju.
Jedan od najvažnijih pokretača evolucije je prirodna selekcija – na osnovu koje pojedinačni organizmi sa određenom genetskom strukturom ostavljaju više potomaka od drugih koji žive u datom okruženju, što dovodi do adaptacija koje tom organizmu omogućuju da opstane, dok drugi organizmi nestaju.
Kolekcija naučnih fotografija/ De Angelis, Maurizzio
Kao što je Darvin utvrdio, ovaj proces pozitivne prirodne selekcije – na osnovu kog osobine koje uvećavaju sposobnost opstanka nekog organizma postaju dominantne u populaciji – doprinosi diverzitetu koji postoji među organskim vrstama. Ali prirodna selekcija je takođe faktor i u procesima koji ugrožavaju i naš opstanak, kao što je širenje virusnih infekcija i pojava otpornosti na antibiotike kod bakterijskih patogena. Međutim, zahvaljujući izuzetnim laboratorijskim eksperimentima (npr. Bryk, 2017), i napretku u tehnologiji sekvenciranja gena, kao što je upotreba ručnih mini uređaja za sekvenciranje, danas možemo brzo i precizno da pratimo ovaj proces – ne samo u laboratoriji, nego i bilo gde na svetu. Ispostavilo se da je ovo izuzetno značajno za razumevanje evolucije mikroorganizama koji izazivaju bolesti.
U ovom članku se fokusiramo na dve važne studije koje se detaljnije bave načinom kako se ovakvi patogeni neprestano razvijaju, i otkrivaju obrasce genetičkih promena – kao i faktore koji taj razvoj ograničavaju – a koji postoje u pozadini tog procesa.
Proučavanje otpornosti na antibiotike
Pojava otpornosti na antibiotike kod bakterija predstavlja udžbenički primer evolucije izazvane prirodnom selekcijom. Upotreba antibiotika proizvodi selektivni pritisak na populaciju bakterija, koje mutiraju i koje se veoma brzo reprodukuju. Za posledicu toga imamo to da bilo koja genetska varijanta koja štiti bakterije od antibiotika ostaje prisutna u populaciji, dok sve ostale varijante nestaju.
Ovaj proces je na dramatičan način snimio kamerom Dr Majkl Bejm, istraživač sa univerziteta Harvard u SAD, koji sebe smatra borcem protiv otpornosti na antibiotike. Tokom 2015. godine Bejm je napravio inteligentnu spravu pomoću koje je moguće videti kako se rezistentne bakterije šire u okruženju u kom se nalaze antibiotici. Koristio je jednu ogromnu pravougaonu Petrijevu posudu, koja je bila široka 60 cm, a dugačka 120 cm (standardna Petrijeva posuda ima u prečniku 9 cm) koju je napunio agarom, pihtijastim medijumom za uzgajanje bakterija, koji je bio obojen u crno. Ključna stvar je bila to što je u agar ubacio koncentracije antibiotika koje su se postepeno povećavale prateći dužinu posude (slika 1), od nulte koncentracije na obodima posude do 1000 jedinica antibiotika u sredini – što bi trebalo da bude dovoljno da u potpunosti uništi bilo koju bakteriju. Posudu je osvetlio reflektorom i ka njoj je usmerio kameru, tako da može jasno da vidi bilo koju koloniju bakterija u vidu belih tačaka u odnosu na crnu pozadinu agara. Zatim je u posudu ubrizgao bakteriju ešerihija koli (E. Coli ) na svakom kraju posude, gde nije bilo antibiotika – i čekao je da proces počne (slika 2).

Laboratorija Kišoni, Medicinski fakultet Univerziteta Harvard i Tehnion – Izraelski institut za tehnologiju
Pa, šta se to dogodilo? Ešerihija koli je mogla da se kreće po površinskom sloju agara, tako da su se bakterije koje su ostale bez hrane u svom okruženju premestile u druge delove posude (slika 3). Međutim, njihov rast su kočili antibiotici u okolnim delovima posude, tako da su samo bakterije koje su mutirale tako da mogu da prežive izloženost antibioticima mogle da se šire i dalje. Onaj deo posude u kom su se nalazili antibiotici (u koncentraciji od samo jedne jedinice su u početku naselili pojedinačni mutanti. Oni su se razmnožavali, tako što se njihova sledeća generacija širila po celom delu posude – dok se i sami nisu suočili sa višom koncentracijom antibiotika. Bakterije koje su se nalazile na graničnoj liniji su ponovo prestale da se šire dok se nisu pojavile nove mutacije koje su kod njih proizvele uvećanu toleranciju na antibiotike.
Ponavljali su ovaj proces na svakoj graničnoj liniji sve dok, posle 11 dana rasta, bakterija E. coli nije prekrila celokupnu površinu te velike posude, s tim što su bakterije koje su se nalazile u centru posude razvile otpornost na koncentracije antibiotika koje su bile 1000 puta veće od onih pored graničnih linija (slika 4). Svaki faza ovog procesa je snimljena u video filmu koji je danas veoma poznatw1.

Laboratorija Kišoni, Medicinski fakultet Univerziteta Harvard i Tehnion – Izraelski institut za tehnologiju

Laboratorija Kišoni, Medicinski fakultet Univerziteta Harvard i Tehnion – Izraelski institut za tehnologiju

Laboratorija Kišoni, Medicinski fakultet Univerziteta Harvard i Tehnion – Izraelski institut za tehnologiju
Kao što straživači mogu da prate širenje bakterija iz slike u sliku, isto tako mogu da uzmu uzorke bakterija sa kritičnih tačaka na kojima su nastali određeni mutanti. Uz pomoć sekvenciranja ovih genoma uspeli su da uoče promene u svakoj fazi evolucije njihove rezistentnosti (slika 5).
Ispostavilo se da su se mnoge od tih mutacija dogodile više puta, tako da izgleda da su neki putevi koji dovode do rezistentnosti uobičajeniji od drugih. Pored toga, neke mutacije su se dogodile u genima koji očigledno nemaju nikakve veze sa antibioticima, što je ilustrovalo jedan važan momenat u razvoju rezistentnosti: potreba da se prilagode antibioticima predstavlja opterećenje u osnovnim metaboličkim procesima, tako da i ako nema antibiotika, rezistentne bakterije se često razmnožavaju sporije nego one koje nisu rezistentne. Dodatne mutacije su bile potrebne da bi se kompenzovalo to metaboličko opterećenje, i to može biti još jedan razlog zbog kog su nastajali prekidi u razmnožavanju bakterija na graničnim linijama gde se povećavala koncentracija antibiotika.
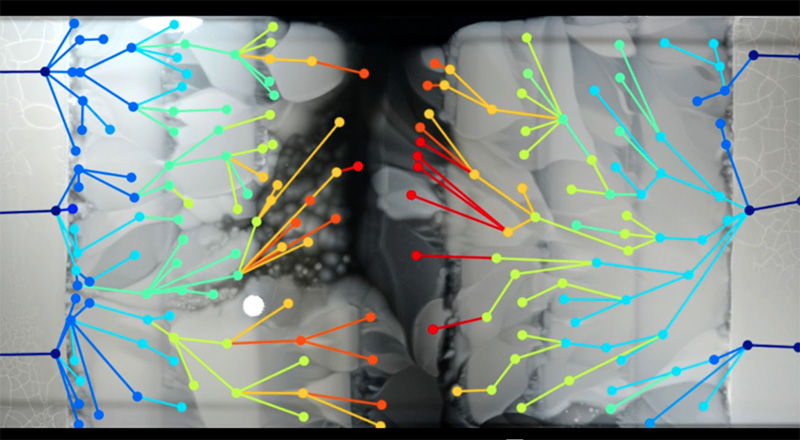
Laboratorija Kišoni, Medicinski fakultet Univerziteta Harvard i Tehnion – Izraelski institut za tehnologiju
U jednoj daljoj fazi eksperimenta Bejm i kolege su uočili još jednu ključnu stvar. Kad god su pojačali razliku u koncentraciji antibiotika u delovima posude koji se graniče jedni sa drugima, nijedan mutant nije mogao da preživi u susednom delu, i tako je u potpunosti zaustavljen rast bakterija na prvoj graničnoj liniji. Ova pojava se može objasniti istovetnim principom: rast bakterija je skoro nemoguć kad imamo veoma visok selektivni pritisak antibiotika u okruženju, zato što je za mehanizme koji su neophodni da se ovakvo opterećenje prevaziđe potrebno previše mutacija odjednom – tako da dolazi do uginuća bakterija.
Epidemija ebole
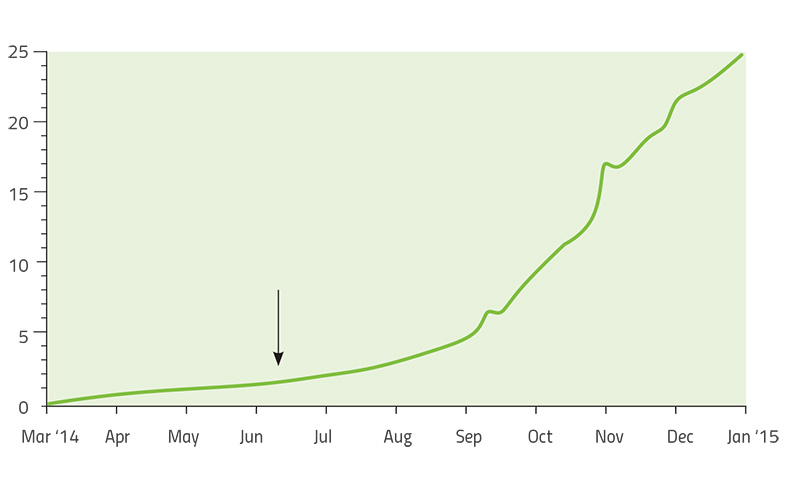
Još jedan primer u evoluciji mikrobijalnih patogena koji je intenzivno proučavan je jedan od najsmrtonosnijih ljudskih patogena: virus ebole. Epidemija ebole 2013. – 2015. bila je najdugotrajnija i najveća do sada, tokom koje je obolelo 28 646 osoba, od kojih je do juna 2016. godine umrlo njih 11 323. Trajanje epidemije se poklopilo sa uvođenjem tehnologije brzog sekvenciranja gena koja je mogla da se primeni na terenu, što je omogućilo istraživačima da prate evoluciju virusa tokom perioda širenja zaraze na nove pacijente.
Predvođeni američkim genetičarima Dr Pardiom Sabetijem ( Univerziteta Harvard), Dr Džeremijem Lubanom ( Medicinski fakultet Univerziteta u Masačusetsu) i Dr Endruom Ramboom (Univerzitet u Edinburgu), naučnici koji su proučavali ebolu napravili su ,,porodično stablo” virusa tokom perioda njegovog dvogodišnjeg širenja zapadnom Afrikom (Park, 2015). Svaka grana ovog stabla je predstavljala novi skup mutacija koje su virusu dozvoljavale da raste, opstaje i da se multiplifikuje bolje od ostalih sojeva. Upoređivanjem virusnih genoma uzetih od različitih pacijenata iz različitih zemalja u različito vreme, tim naučnika je utvrdio da je glavna varijanta virusa došla iz Gvineje – i da je dobila sposobnost da se proširi tek nakon što je pretrpela novih pet mutacija. Nakon što se virus preselio iz Gvineje u Sijera Leone u maju 2014. godine pojavila se još jedna mutacija i postala je mnogo uobičajenija u tom regionu. (Diehl i sar., 2016)w2. Ta nova mutacija je bila prvi put uočena kod samo jednog pacijenta i bila je tako uspešna da je 97% od više od dve stotine i više genoma ebole koji su bili analizirani u ovoj studiji vodilo poreklo od tog mutanta. Ovo predstavlja veoma značajan prikaz uspeha jednog soja koji se pojavio samo dve godine ranije (slika 6).
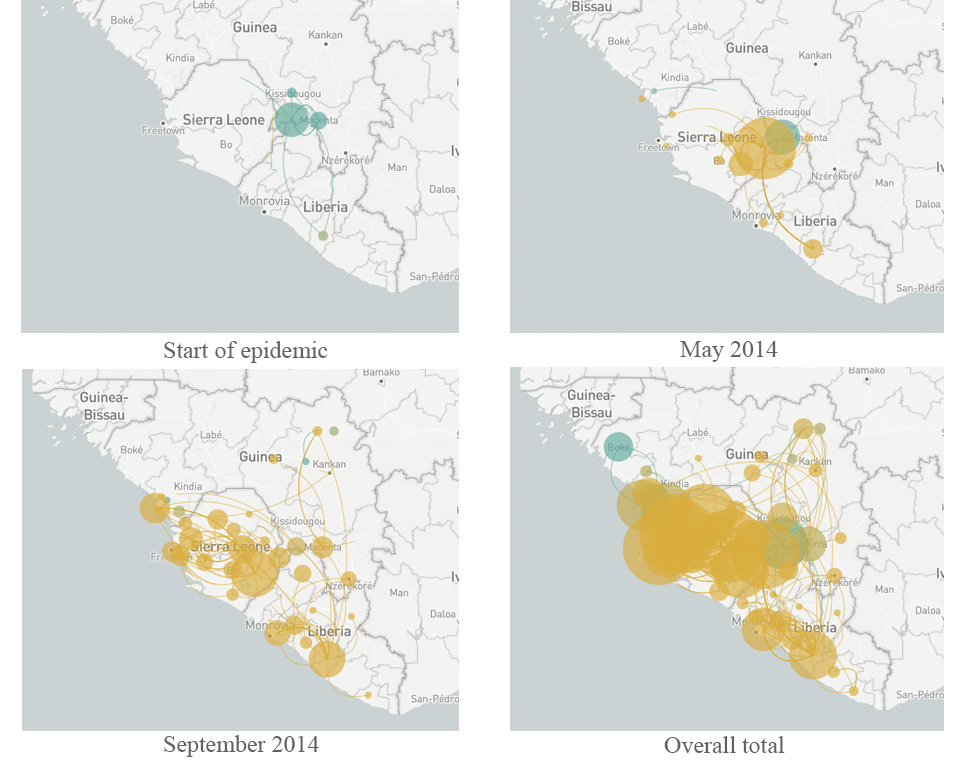
(Izvor: nextstrain.org)
Još je važnije to što je studija otkrila da su se neki geni iz genoma ebole izmenili u većoj meri od očekivane, uključujući i one za molekule proteina koji se nalaze izvan virusa. Smatra se da su ovi proteini virusa meta ljudskih antitela koje se bore protiv infekcije, tako da brze promene u ovim proteinima mogu da pomognu virusu da izbegne neutralizaciju od strane domaćina – što predstavlja obrazac izazvan prirodnom selekcijom. Ti geni su sada u fokusu istraživanja koja obećavaju da ćemo moći da se suprotstavimo tom virusu prilikom neke buduće epidemije. Sticanje novih znanja o mehanizmima evolucije pomaže istraživačima i u razvijanju efikasnih strategija za borbu protiv patogena u budućnosti.
References
- Bryk J (2017) Evolucija na delu: eksperiment od 67 000 generacija. Science in School 41.
- Park D et al. (2015) Ebola virus epidemiology, transmission, and evolution during seven months in Sierra Leone. (Virus ebole u Siera Leone, epidemiologija, prenošenje i evolucija tokom sedmomesečnog perioda.) Cell 161 1516-1526. doi: 10.1016/j.cell.2015.06.007
- Diehl W E et al. (2016) Ebola virus glycoprotein with increased infectivity dominated the 2013–2016 epidemic. (Glikoprotein virusa ebole sa povećanom infektivnošću koja je dominirala tokom epidemije 2013 – 2016.) Cell 167 1088–1097. doi: 10.1016/j.cell.2016.10.014
Web References
- w1 – Pogledajte video film koji su snimili Majkl Bejm i kolege u kom se prikazuje širenje E. coli po delovima ,,mega-posude” sa povećanim koncentracijama antibiotika.
- w2 – Pogledajte animacije koje prikazuju širenje virusa ebole, i kako je novi soj virusa koji se pojavio oko juna 2014. godine uticao na njegovo dalje širenje.
Resources
- Posetite The Atlantic website gde ćete moći da pročitate članke o Bejmovom eksperimentu i njegovoj primeni.
- Pročitajte nučni rad o Bejmovom eksperimentu u časopisu Science:
- Baym M et al. (2016) Spatiotemporal microbial evolution on antibiotic landscapes. Science 53: 1147-1151. doi: 10.1126/science.aag0822
- Pogledajte TED govor o suzbijanju ebole istraživača Pardis Sabetija.
- Pročitajte blog na temu Praćenje ebole sa medijskim predstavljanjem istraživanja i tehnologije koja se u tu svrhu koristi.
- Vodič kroz ebolu možete pronaći na vebsajtu Lekara bez granica.
Review
Vremenska dimenzija predstavlja jedan od glavnih problema prilikom predavanja o evoluciji. Pošto je ljudski život kratak u poređenju sa vremenskim okvirom u kom se odvijaju veliki evolutivni procesi, koncept promena koje se vremenom odvijaju nameće se kao osnovni problem za razumevanje evolucije. Primeri evolutivnih procesa koji se odvijaju tokom nekog vremenskog perioda koji je ljudima shvatljiv mogu da posluže za prevazilaženje problema u shvatanju evolucije.
Eksperiment koji je opisan u ovom članku pruža veoma dobar uvid u to kako elementi vremena i mutacija utiču na evoluciju. Nastavnici bi mogli da koriste ovaj članak za svoja predavanja o evoluciji, tako što mogu da pokažu kako evolucija može da se odigra i tokom kratkog vremenskog perioda. Članak je koristan i za objašnjavanje ključne uloge koju mutacije igraju tokom evolucije, kao izvor različitosti na koji kasnije utiče prirodna selekcija. Lako je razumeti ovaj eksperiment budući da je zasnovan na ideji koja je bliska ljudima – upotrebi antibiotika.
Panajotis K Stasinakis, nastavnik biologije, Četvrta gimnazija, Zografu, Grčka





