Kaip veikia evoliucija: ligų sukėlėjai Understand article
Sveikatai grėsmę keliantys ligų sukėlėjai nuolat evoliucionuoja, kad aplenktų apsaugines mūsų organizmo užkardas. Tačiau šiais laikais mes galime sekti jų pokyčius genų lygmeniu bemaž realiu laiku.
Viena pagrindinių evoliucijos jėgų yra natūralioji atranka, kuomet individualūs specifinių genetinių bruožų turintys organizmai tam tikromis sąlygomis susilaukia daugiau palikuonių ir adaptuojasi, kad išgyventų, o likusieji – pražūsta.
Paveikslėlio autorinės teisės priklauso Science Photo Library/Maurizio De Angelis
Darvinas nustatė, kad teigiama natūralioji atranka, kuomet populiacijoje ima dominuoti bruožai, pagerinantys organizmo šansus išlikti, skatina rūšių įvairovę. Tačiau ji taip pat gali prisidėti ir prie procesų, keliančių pavojų mūsų pačių išlikimui, pavyzdžiui, plintant virusinėms infekcijoms ar ligas sukeliančioms bakterijoms tampant atsparioms antibiotikams. Vis dėlto, genialūs eksperimentai laboratorijose (pavyzdžiui, Bryk, 2017), ir naujos genų sekvenavimo technologijos, tokios kaip rankoje telpantys sekvenavimo aparatai, leidžia mums greitai ir tiksliai tirti šį reiškinį – ne tik laboratorijoje, o beveik bet kur. Jos ypač vertingos norint suprasti ligas sukeliančių mikroorganizmų evoliuciją.
Šiame straipsnyje susikoncentruosime ties dviem išskirtiniais tyrimais, atskleidžiančiais, kaip ligų sukėlėjai evoliucionuoja, po šiuo reiškiniu slypinčius genų pokyčių dėsningumus ir jį ribojančius veiksnius.
Lempų šviesoje – atsparumas antibiotikams
Klasikinis teigiamos natūraliosios aplinkos pavyzdys – atsiradęs bakterijų atsparumas antibiotikams. Antibiotikų vartojimas labai greitai mutuojančių ir besidauginančių bakterijų populiacijai sukelia selekcinį spaudimą. To pasekmė yra tai, kad toje populiacijoje visi genų variantai, apsaugantys bakterijas nuo antibiotikų, išliks, o kiti – išnyks.
Šis reiškinys labai vykusiai užfiksuotas daktaro Michael‘o Baym‘o, Harvardo universiteto (JAV) mokslininko ir prisiekusio kovotojo prieš atsparumą antibiotikams. 2015-aisiais, Baym‘as paruošė gudrų įrengimą, leidžiantį stebėti, kaip atsparios bakterijos plinta terpėje, kurioje esama antibiotikų. Tam jis pasinaudojo milžiniška stačiakampe, 60 cm pločio ir 120 cm ilgio Petri lėkštele (įprastinės Petri lėkštelės diametras – 9 cm), užpildyta juodai nudažytu agaru – į želė panašia terpe auginti bakterijoms. Svarbiausia, kad į agarą įmaišė antibiotiko, kurio koncentracija didėjo išilgai lėkštutės krašto (paveikslėlis nr. 1), nuo visiškai nė kiek antibiotiko lėkštelės kraštuose, iki 1000 antibiotiko vienetų viduriniuose terpės segmentuose, ko visiškai turėtų užtekti išsyk užmušti bet kokioms bakterijoms. Virš lėkštelės jis įtaisė apšvietimą ir kamerą, kad bakterijų kolonijos būtų aiškiai pastebimos kaip balti taškai juodame agare. Tuomet jis pasėjo Escherichia coli (E. coli) bakterijų pačiuose lėkštelės galuose, kur nebuvo nė kiek antibiotiko ir ėmė laukti (paveikslėlis nr. 2).

Paveikslėlio autorinės teisės priklauso Kishony laboratorijai (Harvardo medicinos mokykla) ir Technion (Izraelio technologijų institutas)
Tad kas nutiko? E. coli galėjo judėti viršutiniame agaro sluoksnyje, tad kai bakterijoms jų aplinkoje pristigo maistinių medžiagų, jos persikėlė kitur (paveikslėlis nr. 3). Tačiau čia jų augimą stabdė antibiotikas, tad tik bakterijos, turėjusios mutacijų, leidžiančių išgyventi susidūrimą su antibiotiku, galėjo sklisti toliau. Tad pirmajame plotelyje, kuriame buvo antibiotiko (viso labo vieno koncentracijos vieneto) iš pradžių atsirado pavienės mutantės. Jos ėmė daugintis, o jų palikuonės sklido tol, kol pačios pateko į plotelį su didesne antibiotiko koncentracija. Plotelio pakraštyje bakterijos liovėsi augusios tol, kol įvyko naujų mutacijų, leidžiančių toleruoti antibiotiką.
Šis reiškinys kartojosi kiekvieno plotelio pakraštyje tol, kol augusios 11 dienų, E. coli bakterijos uždengė visą milžiniškos lėkštelės paviršių, bakterijoms lėkštelės vidury tapus 1000 kartų atsparesnėms antibiotikui nei toms, kurios augo prie kraštų (paveikslėlis nr. 4). Kiekvienas šio reiškinio etapas buvo nufilmuotas dabar jau išgarsėjusiam videow1.

Paveikslėlio autorinės teisės priklauso Kishony laboratorijai (Harvardo medicinos mokykla) ir Technion (Izraelio technologijų institutas)

Paveikslėlio autorinės teisės priklauso Kishony laboratorijai (Harvardo medicinos mokykla) ir Technion (Izraelio technologijų institutas)

Paveikslėlio autorinės teisės priklauso Kishony laboratorijai (Harvardo medicinos mokykla) ir Technion (Izraelio technologijų institutas)
Kadras po kadro stebėdami bakterijų sklidimą, mokslininkai taip pat galėjo surinkti ir bakterijų mėginius tais kritiniais etapais, kai rasdavosi mutantės. Sekvenuodami jų genomus, mokslininkai galėjo ieškoti pokyčių, vykusių kiekviename atsparumo antibiotikams evoliucijos etape (paveikslėlis nr. 5).
Paaiškėjo, kad dalis mutacijų įvyko daugelį kartų, tad panašu, kad kai kurie atsparumo mechanizmai dažnesni nei kiti. Be to, kai kurios mutacijos paveikė genus, kurie kaip ir neturėjo nieko bendro su antibiotiku, atkreipdamos dėmesį į tai, kad formuojantis atsparumui antibiotikams, svarbu štai kas: poreikis prisitaikyti prie antibiotiko – apkrova elementariems medžiagų apykaitos procesams, tad, aplinkoje nebelikus antibiotikų, atsparios bakterijos dažnai augdavo lėčiau nei neatsparios. Papildomos mutacijos buvo reikalingos tam, kad kompensuotų apkrovą medžiagų apykaitai, ir šitai galėjo tapti dar viena priežastimi, kad bakterijų augimas plotelių pakraščiuose, kur didėjo antibiotiko koncentracija, laikinai stabtelėtų.
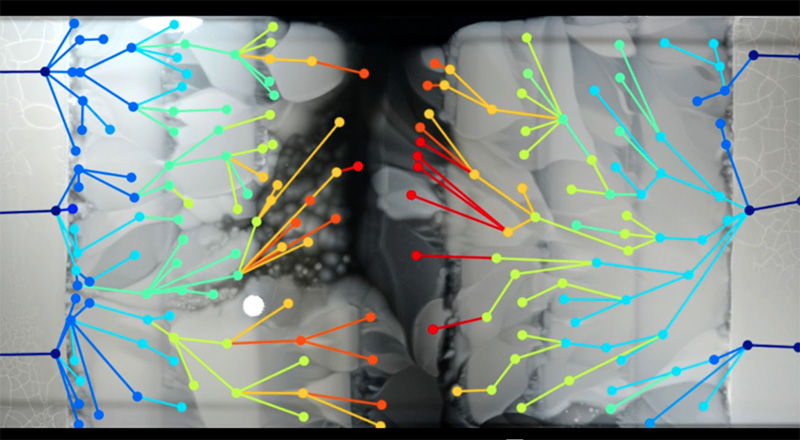
Paveikslėlio autorinės teisės priklauso Kishony laboratorijai (Harvardo medicinos mokykla) ir Technion (Izraelio technologijų institutas)
Kitame šio eksperimento etape, Baym‘as ir jo kolegos pastebėjo dar vieną esminį dalyką. Padidinus skirtumą tarp antibiotiko koncentracijų gretimuose ploteliuose, mutantės nebegalėdavo išgyventi kitoje lėkštelės dalyje ir bakterijos liaudavosi augti ties pirma riba. Šį reiškinį galima paaiškinti tuo pačiu principu: kai antibiotikų sukeltas selekcinis spaudimas labai didelis, bakterijoms beveik išvis neįmanoma augti, nes mechanizmams, būtiniems ištverti tokį spaudimą, reikia labai jau daug mutacijų vienu metu, tad bakterijos miršta.
Ebolos epidemija
Kitas daug tirtas ligas sukeliančių mikrobų evoliucijos pavyzdys – vienas mirtiniausių žmonijos ligų sukėlėjų: Ebolos virusas. 2013-2015-ųjų Ebolos epidemija buvo lig šiol ilgiausiai trukusi ir pareikalavusi daugiausiai aukų, iki 2016-ųjų birželio užregistravus 28646 ligos atvejus ir 11323 mirtis. Tai, kad epidemija užsitęsė ir sutapo su greitojo genų sekvenavimo technologijos, kurią galima pritaikyti čia ir dabar, atvykimu, leido mokslininkams stebėti viruso evoliuciją, šiam užkrečiant vis naujus pacientus.
Mokslininkai, tiriantys Ebolą, vedami JAV dirbančių genetikų – daktarės Pardis Sabeti (Harvardo universitetas), daktaro Jeremy Luban (Masačiusetso universiteto medicinos mokykla) ir daktaro Andrew Rambaut (Edinburgo universitetas), sudarė viruso, dvejus metus sklidusio vakarų Afrikoje, „genetinį medį“ (Park, 2015). Kiekviena medžio atšaka vaizdavo naują mutacijų kombinaciją, leidžiančią virusui augti ir daugintis geriau nei kitoms atmainoms. Palyginus virusų, skirtingu metu surinktų iš pacientų įvairiose valstybėse, genomą, komanda nustatė, kad pagrindinis viruso variantas atsirado Gvinėjoje, ir kad jis galėjo pasklisti toliau tik tada, kai įgijo penkias naujas mutacijas. Virusui iš Gvinėjos 2014-ųjų gegužę paplitus Siera Leonėje, įvyko kita mutacija ir paplito tame regione (Diehl et al., 2016)w2. Naujoji mutacija pirmiausiai buvo pastebėta viename paciente, tačiau paplito taip sėkmingai, kad 97% iš daugiau nei 200 Ebolos genomų analizuotų šio tyrimo metu, buvo kilę iš to mutavusio viruso. Kaip atmainai, atsiradusiai vos prieš porą metų, tai – stebėtina sėkmės istorija (paveikslėlis nr. 6).
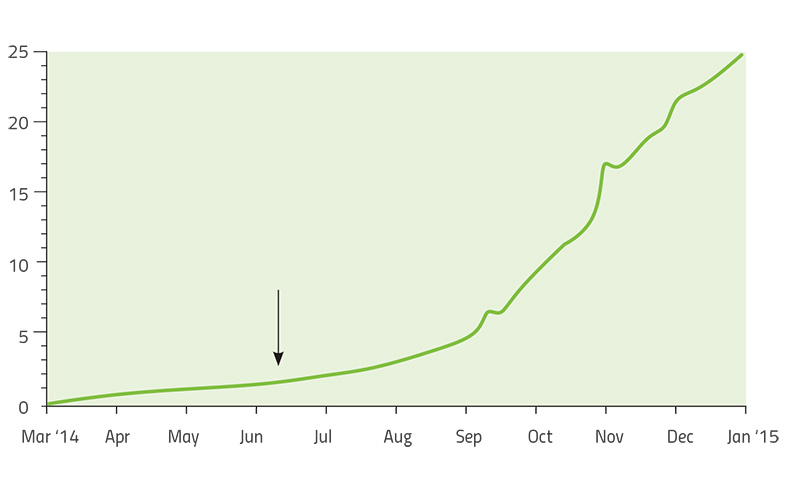
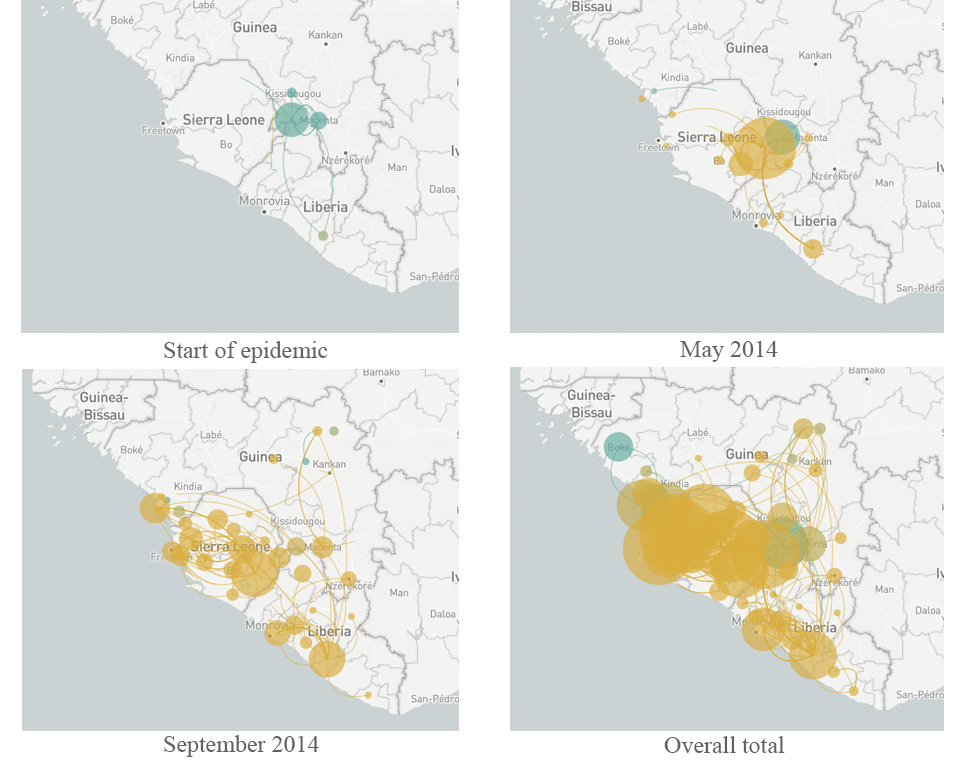
(Šaltinis: nextstrain.org)
Svarbiausia, kad Ebolos genomo tyrimas aptiko keletą genų, pakitusių labiau nei tikėtasi, įskaitant ir tuos genus, kurie koduoja viruso paviršiaus baltymų molekules. Manoma, kad kovojant su infekcija, žmogaus organizme gaminami antikūnai taikosi būtent šiuos viruso baltymus, tad staigiai įvykę jų pokyčiai gali padėti virusui išvengti neutralizavimo organizme, kas jau būtų natūraliosios atrankos dėsningumas. Šie genai tapo daug žadančiu tyrimų epicentru tikintis suvaldyti viruso plitimą ateities epidemijų metu. Tolimesni evoliucijos mechanizmų tyrimai ateityje taip pat padės mokslininkams sukurti efektyvias priemones kovoti su ligų sukėlėjais.
References
- Bryk J (2017) Evolution in action: the 67 000-generation experiment. Science in School 41: 24-29.
- Park D et al. (2015) Ebola virus epidemiology, transmission, and evolution during seven months in Sierra Leone. Cell 161 1516-1526. doi: 10.1016/j.cell.2015.06.007
- Diehl W E et al. (2016) Ebola virus glycoprotein with increased infectivity dominated the 2013–2016 epidemic. Cell 167 1088–1097. doi: 10.1016/j.cell.2016.10.014
Web References
- w1 – Siūlome pasižiūrėti Michael’o Baym‘o ir kolegų nufilmuotą video, vaizduojanti, kaip E. coli Petri „megalėkštelėje“ sklinda per plotus didėjant antibiotiko koncentracijomis.
- w2 – Siūlome pasižiūrėti animuotą žemėlapį, rodantį Ebolos viruso plitimą ir kaip jis pasikeitė, 2014-ųjų birželį atsiradus naujai viruso atmainai.
Resources
- Siūlome aplankyti „The Atlantic“ puslapį ir paskaityti straipsnį apie Baym‘o eksperimentą ir iš jo darytinas išvadas.
- Siūlome paskaityti mokslinį straipsnį, komentuojantį Baym‘o eksperimentą žurnale „Science“:
- Baym M et al. (2016) Spatiotemporal microbial evolution on antibiotic landscapes. Science 53: 1147-1151. doi: 10.1126/science.aag0822
- Siūlome pažiūrėti mokslininkės Pardis Sabeti TED paskaitą apie kovą su Ebola.
- Siūlome perskaityti komentarą apie Ebolos stebėjimus, taip pat it nuorodas į žiniasklaidos komentarus apie susijusius tyrimus ir technologijas.
- Informacinį straipsnį apie Ebolą galite perskaityti Médecins Sans Frontières puslapyje.
Review
Viena didesnių problemų dėstant evoliucijos principus yra laikas. Kadangi žmogaus gyvenimas, palyginus su evoliucijos procesais, yra trumpas, vienas didesnių iššūkių bandant suvokti evoliuciją yra pokyčių per ilgą laiko tarpą samprata. Tad pavyzdžiai, kur pokyčiai įvyksta per žmonėms suvokiamą laiko tarpą, leidžia apeiti šią problemą.
Eksperimentas, aprašytas šiame straipsnyje, siūlo labai gerą perspektyvą tam, kaip laikas ir mutacijos paveikia evoliuciją. Mokytojai galėtų naudotis šiuo straipsniu mokydami apie evoliuciją, kad parodytų, jog ji gali įvykti ir prie trumpą laiko tarpą. Straipsnis taip pat padeda paaiškinti, kad mutacijos, kaip šaltinis įvairovei ir dar veikiamos natūraliosios atrankos, vaidina labai svarbų vaidmenį vykstant evoliucijai. Ir todėl, kad eksperimentas naudoja pažįstamą sampratą – atsparumą antibiotikams, jį lengva suprasti.
Panagiotis K Stasinakis, biologijos mokytojas, 4-toji vidurinė mokykla, Zografou, Graikija





