Las cambiantes tecnologías del diseño de fármacos Understand article
A lo largo de varias décadas, la búsqueda de nuevos medicamentos ha pasado de la imitación de moléculas naturales al cribado de muchos millones de compuestos.
Los primeros medicamentos diseñados por los químicos se inspiraron en la naturaleza. La aspirina procedía de un extracto de sauce; la belladona, de la una planta a la que debe su nombre; y los opiáceos, como la morfina, de la adormidera. Más tarde, se encontraron medicamentos en otros materiales naturales- cabe destacar la penicilina, que se aisló de un moho.
Aunque la naturaleza ha seguido siendo una rica fuente de ideas para nuevos fármacos, hay muchas enfermedades para las que no existen compuestos naturales como tratamiento. Los científicos tienen ahora un papel fundamental en el diseño de nuevos compuestos que puedan dar lugar a tratamientos farmacéuticos eficaces. Esto ha exigido la adopción de nuevos enfoques y técnicas -desde el cribado automatizado hasta la ingeniería genética- para desarrollar un proceso de descubrimiento de fármacos más complejo y preciso que nunca.
Diseñando medicamentos modernos
Entender cómo funcionan los procesos bioquímicos es fundamental para el diseño de la medicina moderna. Al estudiar la bioquímica de un efecto concreto, los científicos pueden diseñar moléculas que imiten su efecto o impidan que se produzca. Dado que en la mayoría de los procesos de nuestro cuerpo intervienen proteínas, los científicos quieren crear fármacos que alteren el comportamiento de las proteínas asociadas a una determinada enfermedad.
El primer medicamento nuevo que se inventó de este modo, a principios de los años 60, fue el betabloqueante propranolol. Cuando un paciente toma propranolol, el fármaco se asienta en los receptores beta de las células e impide la unión de la adrenalina. Como bloquea la actividad natural de la adrenalina, el propranolol tiene una serie de usos, desde reducir la presión arterial hasta prevenir las migrañas.
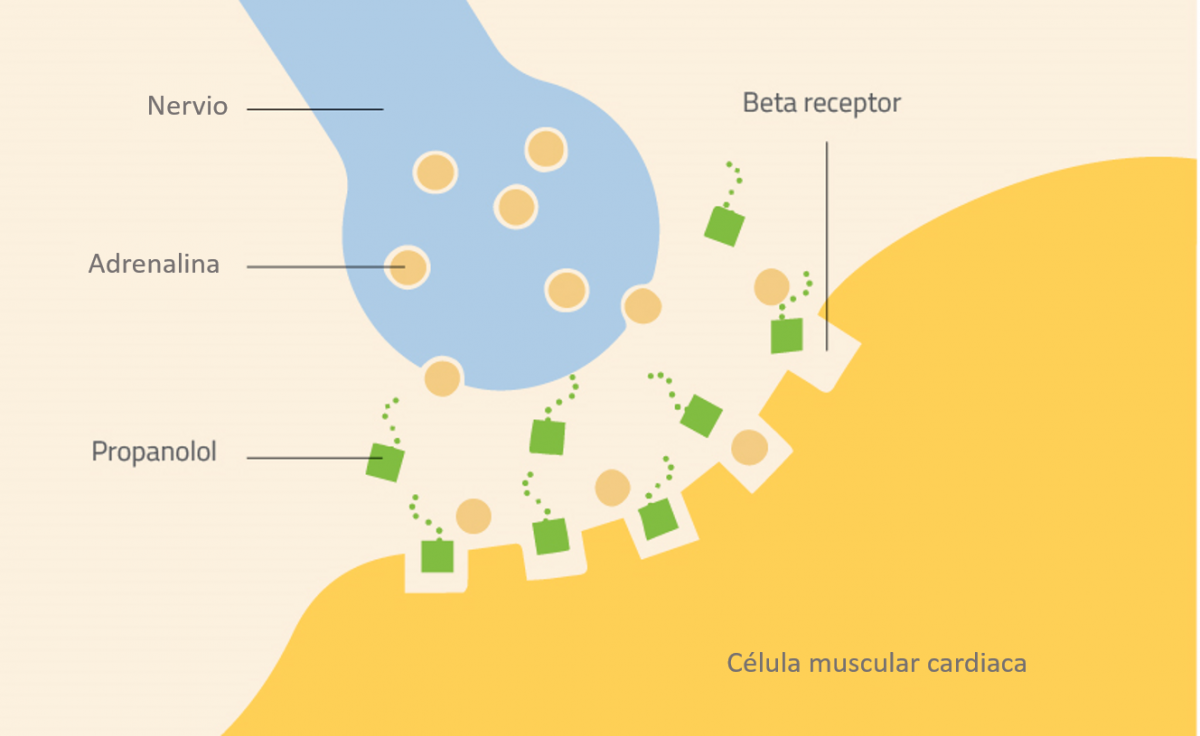
Nicola Graf
A finales de la década de 1980, los científicos pudieron aislar proteínas individuales utilizando nuevas técnicas de biología molecular. Esto les permitió estudiar y medir la fuerza y la naturaleza de las interacciones de unión entre las proteínas y las posibles moléculas farmacológicas. Las técnicas incluían la adición de etiquetas fluorescentes o radiomarcadores a la proteína o a la molécula del fármaco, lo que permitía su seguimiento. La inspiración fue la estructura química de la hormona natural que encaja en el receptor diana: su forma, y sus grupos funcionales, proporcionan pistas sobre la forma que debe tener un fármaco para encajar en el receptor. Los químicos también podrían diseñar modificaciones de esa estructura natural que podrían alterar su actividad según las necesidades.
Al principio, este proceso fue en gran medida un caso de ensayo y error. Pero con el tiempo, se han acumulado muchos conocimientos sobre cómo los diferentes grupos funcionales pueden afectar a la actividad en los receptores. Hoy en día, los químicos pueden predecir qué cambios deben introducir en la estructura de una molécula para conseguir la respuesta deseada. Al modificar con precisión el diseño de las moléculas naturales, los químicos pueden mejorar su afinidad (lo bien que se unen al receptor), su actividad (lo bien que funcionan) y su selectividad (para que no actúen también en otros receptores). Los químicos también harán todo lo posible por ajustar las moléculas para que sean menos propensas a causar efectos secundarios.
Puntos de partida moleculares
Hoy en día, sin embargo, los químicos no siempre utilizan la hormona natural como punto de partida molecular. En su lugar, prueban enormes «bibliotecas» de compuestos diferentes sobre el receptor diana. En un proceso automatizado denominado cribado de alto rendimiento, se realizan pruebas para encontrar moléculas que tengan la actividad deseada en el receptor. En este proceso tan rápido, no es inusual el cribado de un millón de compuestos en una semana. Los resultados de estas pruebas proporcionan a los químicos un punto de partida muy importante para el diseño de fármacos.
El cribado de alto rendimiento encuentra moléculas que interactúan de forma razonablemente fuerte con la proteína diana, pero suelen ser bastante grandes. Para identificar pequeños fragmentos químicos -que suelen producir un efecto más débil- los científicos utilizan un proceso similar denominado descubrimiento de fármacos basado en fragmentos. En lugar de buscar moléculas que ya se parezcan a los fármacos, como las moléculas de una biblioteca de compuestos normal, la idea es utilizar moléculas más pequeñas y sencillas que puedan convertirse en moléculas más complejas más adelante. Este enfoque puede dar una mejor visión de los grupos funcionales que tienen un efecto biológico, porque una molécula pequeña tiene menos partes para interactuar con su diana. Además, los atributos de más de un fragmento pueden combinarse finalmente en una única molécula compleja.
Dos medicamentos contra el cáncer derivados del descubrimiento de fragmentos han llegado al mercado: vemurafenib y venetoclax. Hay varios más en fase de ensayo clínico.

National Center for Advancing Translational Sciences/Flickr, CC BY 2.0

Daniel Soñé Photography, LLC/National Center for Advancing Translational
Sciences/Flickr, CC BY 2.0
Cribado fenotípico
En los últimos años, se ha producido una especie de retorno al antiguo enfoque del descubrimiento de fármacos: identificar un efecto fisiológico y luego averiguar qué proceso biológico lo causó. En lugar de una proteína aislada, los químicos utilizan una célula, un tejido o incluso un organismo entero. Esto se conoce como cribado fenotípico, porque identifica las moléculas que alteran el fenotipo de esa célula, tejido u organismo.
Por ejemplo, en el cáncer, el efecto fisiológico es la multiplicación de las células, y el fenotipo a cambiar es el crecimiento celular, por lo que una molécula farmacológica adecuada matará las células cancerosas o detendrá su crecimiento. O en la diabetes, los investigadores podrían tomar una célula de los islotes pancreáticos y buscar moléculas que alteren la secreción de insulina estimulada por la glucosa.
Una vez identificadas las moléculas, el siguiente paso es averiguar qué ocurre cuando se añaden a la célula, el tejido o el organismo. Los avances de la biología química nos permiten ahora mirar dentro de la célula y ver cómo las moléculas se unen a las proteínas dentro de ella. Hoy en día se pueden observar y estudiar múltiples procesos moleculares al mismo tiempo, tanto si tienen lugar dentro de las células como en su superficie.
La espectrometría de masas extremadamente sensible y los métodos de fluorescencia son la clave de estos avances, ya que ayudan a detectar proteínas individuales entre las miles que expresa una célula.
Técnicas genéticas modernas
Los avances en ingeniería genética y edición de genes también han contribuido al descubrimiento de nuevos fármacos. Gracias a las modernas técnicas de edición del ADN, como TALEN y CRISPR, los científicos pueden eliminar, insertar o sustituir genes de forma muy precisa. Los científicos pueden utilizar estas modificaciones genéticas muy específicas para editar el genoma de las células, lo que les da la seguridad de que lo que ven como resultado del cribado fenotípico es el efecto que quieren ver y no otra cosa.
La edición de genes también puede utilizarse para modificar un sitio de unión y ver si impide que se produzca el proceso biológico original. Las combinaciones de estas nuevas técnicas han acelerado una investigación que, en el pasado, habría llevado muchos años, incluso décadas. La ingeniería genética tiene, pues, el potencial de transformar la forma en que los científicos buscarán medicamentos en el futuro.

Orawan Pattarawimonchai/Shutterstock.com
Acknowledgement
Esta es una versión editada de un artículo publicado por primera vez en la revista Education in Chemistry en mayo de 20177w1.
Web References
- w1 – Education in Chemistry es una revista para profesores de química, publicada por la Royal Society of Chemistry del Reino Unido. Para ver el artículo original, visite el sitio web de EiC.
Resources
- Conozca los pasos del proceso de desarrollo de fármacos, desde el cribado de la molécula hasta su comercialización, en un artículo de Tomorrow’s Pharmacist.
- Vea un vídeo de TED-Ed sobre el descubrimiento de la aspirina.
- Explore el proceso de ensayo y error de la modificación química en el diseño de fármacos con un juego imprimible sobre el descubrimiento de fármacos..
Review
El diseño de nuevos fármacos es un tema apasionante de la química del siglo XXI. La investigación en este campo consiste en diseñar moléculas específicas que actúen localmente a nivel molecular.
Este artículo puede utilizarse para presentar los métodos actuales de búsqueda y diseño de nuevos fármacos, especialmente a los alumnos avanzados. Los profesores pueden utilizar el artículo para discutir los métodos de diferentes campos de la ciencia que se utilizan actualmente para modificar los mecanismos del funcionamiento del cuerpo humano.
A través de estos métodos, el artículo establece vínculos entre la química, la biología e incluso la filosofía. También podría utilizarse para preparar a los estudiantes de ciencias de secundaria para los futuros cursos universitarios, o como conferencia complementaria para los cursos finales.
Las preguntas de comprensión que pueden utilizar los profesores son las siguientes
- En la actualidad, ¿de dónde surgen las primeras ideas para diseñar nuevas moléculas de medicamentos?
- ¿Por qué la combinación de diferentes técnicas es una buena manera de diseñar nuevas moléculas de medicamentos?
- Los efectos secundarios no son deseables cuando tomamos tratamientos farmacológicos. ¿Cómo pueden los químicos ayudar a evitar los efectos secundarios en los nuevos fármacos?
Manuel Hernández Rodríguez, profesor de química, colegio IES Pedro Mercedes, Cuenca, España





