En busca de una mejor batería de ion de litio Understand article
Traducción de Elisa López Schiaffino. Una mirada a lo que les sucede a los electrodos en una batería de ion de litio, con ayuda de los neutrones.
Las baterías de ion de litio almacenan y proporcionan energía para que funcionen los teléfonos y las computadoras portátiles. También se están empezando a utilizar para los vehículos, pero el desarrollo de los automóviles eléctricos se ha visto dificultado por el lento avance en la tecnología de las baterías. Para intentar acelerar este proceso y mejorar la tecnología de las baterías de ion de litio, mis colegas y yo en el Istitut Laue-Langevin (ILL)w1 construimos una batería muy grande para ver qué pasa en su interior mientras está en funcionamiento. Hicimos una película de lo que sucede, y eso les permitió a los científicos comprender cómo mejorar los electrodos de la batería.
El poder del litio
Sabemos que el litio es un metal muy reactivo del grupo I, y que se encuentra arriba y a la izquierda en la tabla periódica de los elementos. El litio es uno de los tres elementos que se crearon en el Big Bang, y no solo se usa para las baterías, además se consume en la combustión estelar.
En la Tierra, obtenemos el litio del suelo: se aprovechan los enormes lagos subterráneos que contienen sales de litio para generar alrededor de 25 000 toneladas de litio cada año. Gran parte de eso se usa para fabricar baterías de ion de litio recargables y livianas.
Al igual que en otras baterías, en las de ion de litio el almacenamiento de energía eléctrica está relacionado con el potencial químico. A diferencia de otras baterías, las de ion de litio son recargables: los reactivos pueden generarse nuevamente al hacer pasar electricidad por el producto. Cuando la batería se agota, puede conectarse a un cargador que usa energía eléctrica para revertir las reacciones químicas que ocurrieron en la batería mientras estaba en uso.
Como su nombre lo indica, las baterías de ion de litio realizan una transferencia de carga mediante iones de litio cargados positivamente. Al igual que otras baterías, la de ion de litio está compuesta por dos electrodos: uno positivo, hecho de un compuesto que contiene litio (muchas veces con un óxido de algún metal de transición, como por ejemplo el manganeso); y otro negativo, generalmente hecho de carbono. Estos dos electrodos están conectados mediante un electrolito que permite que los portadores de carga (los iones de litio) se muevan entre los electrodos. Las dos semirreacciones son, por ejemplo:
LiMn2O4 ⇌ Li1-xMn2O4 + xLi+ + xe–
xLi+ + xe– + xC6 ⇌ xLiC6
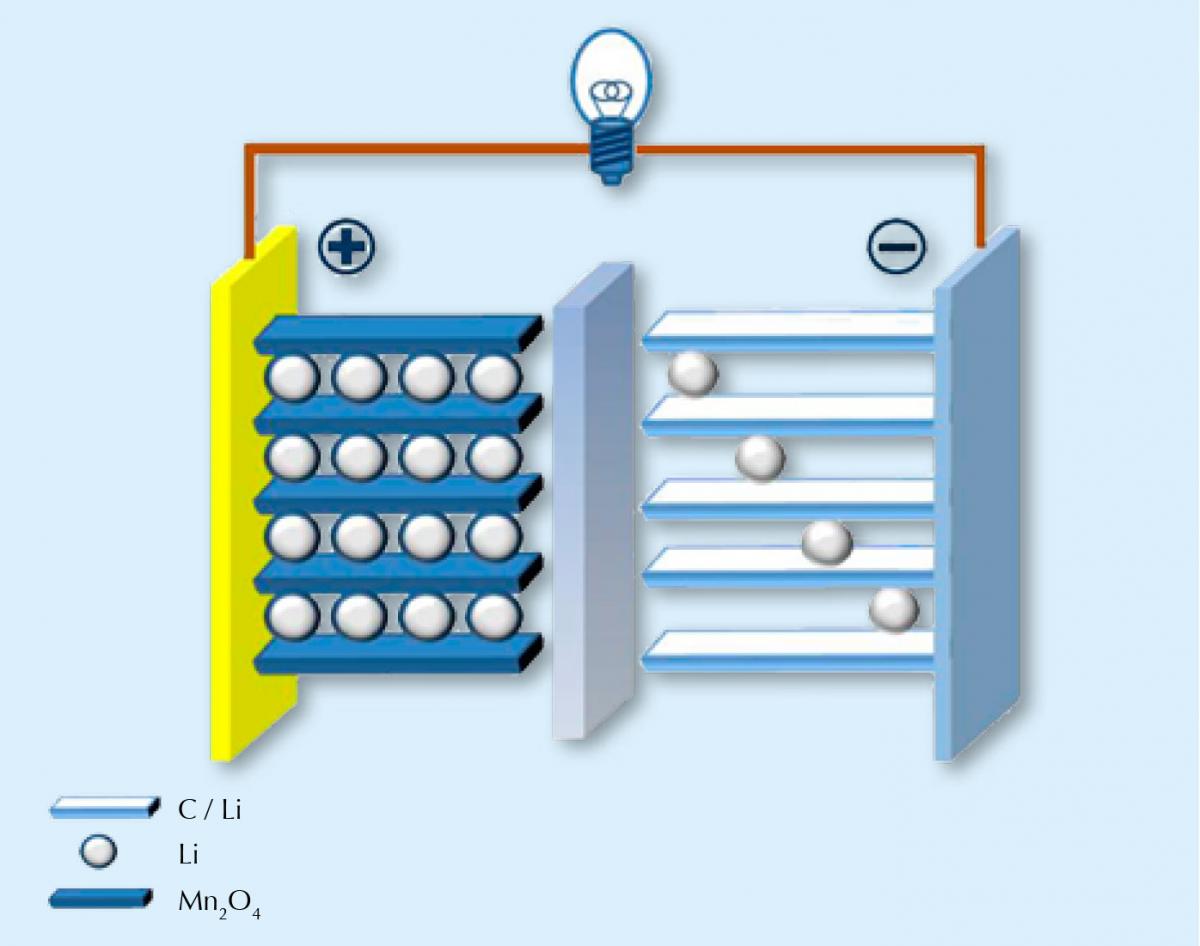
Imagen de dominio público de Chem511grpThinLiBat; origen de la imagen: Wikimedia Commons
Cuando la batería se descarga (es decir, cuando suministra energía), los iones de litio se mueven desde el electrodo de carbono al electrodo que contiene litio, y cuando se recarga, se mueven en la dirección opuesta. Desafortunadamente, este proceso de movimiento de iones no continúa de manera infinita. Con el paso del tiempo, los iones de litio que se mueven entre los electrodos hacen que estos se extiendan y se encojan en forma repetida, lo que los degrada lentamente. Ocurre algo parecido con la ropa que pierde su forma y se deshilacha por el uso y lavado frecuente: pasado un tiempo, los pantalones favoritos ya no quedan tan bien como antes; y, de manera similar, los iones de litio no encajan tan bien en el entramado de los electrones. La batería pierde capacidad.
Por ello, para mejorar el rendimiento de las baterías se necesita mejorar los materiales de los electrodos, lo que implica comprender cómo cambian estos materiales con los reiterados ciclos de carga y descarga. Aquí es donde interviene el ILL con su fuente de neutrones, que nos permite visualizar los cambios en la estructura cristalina de los electrodos. La difracción de neutrones es una técnica excelente para ver cómo se mueven los iones de litio entre los electrodos, ya que los neutrones se dispersan fácilmente con elementos livianos como el litio.
Una película en tiempo real
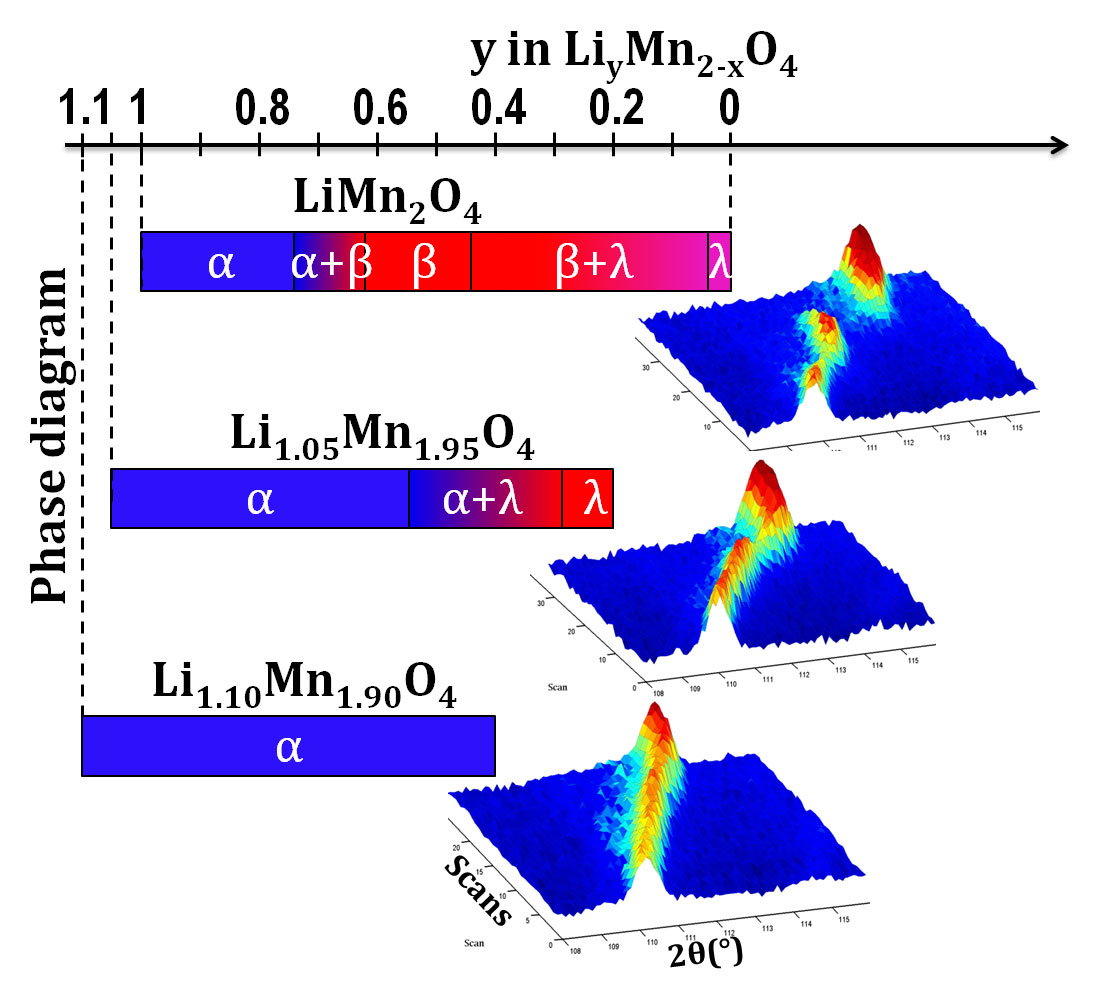
manganeso sufren diferentes
cambios cuando se cargan y
descargan
Imagen cortesía del autor
Es por ello que desarrollamos una batería especial, para investigar qué pasa en los materiales del electrodo cuando está en funcionamiento (Bianchini M et al 2013; 2014). El objetivo era obtener una película de alta calidad en tiempo real sobre el proceso. Para hacer la película, creamos muchas imágenes de difracción de neutrones al dispersarlos a través del material del electrodo mientras la batería se cargaba y descargaba. Luego, usamos estas imágenes como cuadros de la película: una serie de imágenes, una tras otra, al igual que en una animación cuadro por cuadro o en un folioscopio, que nos permite ver qué pasa con el electrodo.
Primero probamos y optimizamos el funcionamiento de una sola celda de la batería y de la metodología y la calidad de las imágenes de difracción. Utilizamos materiales comúnmente empleados para construir electrodos, como el fosfato de hierro y litio (LiFePO4). El LiFePO4 se usa para fabricar electrodos duraderos, seguros y de bajo costo. Cuando estuvimos satisfechos con el experimento, investigamos algunos nuevos materiales para electrodos basados en óxido de manganeso y litio (LiMn2O4) para saber si se comportaban de manera diferente. El LiMn2O4 es un material interesante para construir electrodos positivos, ya que tiene mucha capacidad y un ritmo de carga y descarga elevado, pero la rápida pérdida de capacidad que ocurre con los ciclos de carga limita su uso comercial. Modificamos levemente la fórmula molecular del material y descubrimos que si agregábamos más litio a la estructura, y por lo tanto menos manganeso, podíamos superar ese obstáculo.
Basamos nuestro trabajo en la fórmula molecular LiMn2O4 e hicimos tres compuestos con la fórmula Li1+xMn2-xO4, en la que x es la cantidad adicional de litio. Los valores de x de los tres compuestos fueron 0; 0,05 y 0,10. Al observar cómo cambian los materiales durante la carga, descubrimos que el litio adicional reduce la durabilidad de la batería pero elimina el problema de la pérdida de capacidad. La batería no tiene tanta capacidad, pero esa menor capacidad no va disminuyendo tanto con la carga y descarga.
Descubrimos que esto se debe a que:
- El cambio en el volumen debido a la pérdida de iones de litio es menor a medida que aumenta la cantidad de litio en el material del electrodo, y el mecanismo físico que hace que esto suceda sufre un cambio.
- Cuando aumenta la cantidad de litio, se reduce la cantidad de Mn3+ en una cantidad equivalente, y sabemos que esta especie química obstaculiza la larga vida de las baterías.
En consecuencia, el material con la mayor cantidad de litio resulta mucho mejor para construir una batería.
Hemos demostrado que la difracción de neutrones puede ayudarnos a comprender el comportamiento de los iones de litio y de las baterías de ion de litio, y además hemos encontrado una manera de mejorar este tipo de baterías. Debido a estos resultados prometedores, estamos expandiendo el estudio de este tipo de material a otros de composición diferente, como los que contienen níquel adicional (LiMn1.6Ni0.4O4), que funcionan a mayores voltajes y por ende tienen más energía. Tal vez un día nuestro trabajo ayude a que un automóvil eléctrico funcione más rápido y por más tiempo.
La batería transparente
La celda especial de la batería que usamos para este experimento tenía electrodos más grandes que lo normal para que pudiéramos obtener imágenes de difracción de neutrones de la más alta calidad. La característica más importante de esta batería especial es el uso de una aleación de titanio y circonio, que es transparente a los neutrones: no produce la dispersión de neutrones, sino que pasan a través de este material. De esta manera, solo se recoge la señal del electrodo que nos interesa y se evitan otras contribuciones no deseadas de la celda. También empleamos una versión deuteriada del electrolito: usamos deuterio en lugar de átomos de hidrógeno para reducir la dispersión aún más y mejorar la señal obtenida.
A pesar del gran tamaño de la batería, las muestras que analizamos fueron pequeñas (≈200 mg) en relación a lo que en general se requiere para los experimentos de difracción de neutrones (≈1 g). Pero gracias al alto poder de la fuente de neutrones del ILL y a los modernos difractómetros disponibles, pudimos obtener las imágenes que deseábamos.

Imagen de Wurzeller [domino público]; origen de la imagen: Wikimedia Commons
Más información sobre el ILL
El Institut Laue-Langevin (ILL)w1 es un centro de investigación internacional ubicado en Grenoble (Francia). Ha sido el líder mundial en la ciencia y la tecnología de la dispersión de neutrones por 40 años, desde el comienzo de los experimentos en 1972. El ILL opera una de las fuentes de neutrones más poderosas del mundo; dispara haces de neutrones a una serie de 40 instrumentos de alto rendimiento que son constantemente mejorados. Cada año, 1200 investigadores de más de 40 países visitan el ILL para realizar actividades de investigación en las áreas de física de la materia condensada, química, biología, física nuclear y ciencia de materiales.
El ILL forma parte de EIROforumw2, organismo que publica Science in School.
References
- Bianchini M et al (2013) A New Null Matrix Electrochemical Cell for Rietveld Refinements of In-Situ or Operando Neutron Powder Diffraction Data. Journal of the Electrochemical Society 160: A2176–A2183. doi: 10.1149/2.076311jes
- Bianchini M et al (2014) Li-Rich Li1+xMn2–xO4 Spinel Electrode Materials: An Operando Neutron Diffraction Study during Li+ Extraction/Insertion. Journal of Physical Chemistry C 118: 25947–25955. doi: 10.1021/jp509027g
Web References
- w1 – Si desea más información sobre el ILL.
- Consulte la lista de los artículos de Science in School relacionados con el ILL.
- w2 – EIRO forum es un grupo de colaboración que representa a ocho de las mayores organizaciones intergubernamentales de investigación de Europa. Estas organizaciones combinan sus recursos, instalaciones y experiencia en apoyo de la ciencia europea para que alcance su pleno potencial. Entre sus actividades de educación y divulgación, EIROforum publica Science in School.
Resources
- Los científicos del European Synchrotron Radiation Facility (ESRF, Laboratorio europeo de radiación sincrotón) ubicado en Grenoble (Francia) también trabajan con baterías de ion de litio, y hay un artículo interesante sobre ese trabajo en las páginas 16 y 17 del número de ESRF news de julio (2015).
Institutions
Review
La batería de ion de litio es uno de los insumos electroquímicos más importantes que está presente en la vida cotidiana de los estudiantes. Sin embargo, la baja capacidad y durabilidad de este tipo de batería son factores que han retrasado su implementación en, por ejemplo, los vehículos eléctricos.
En este artículo, los científicos del Institut Laue-Langevin (ILL) explican el trabajo que llevaron a cabo para mejorar las características de las baterías de ion de litio. Con este artículo, los docentes pueden proveer ejemplos de investigación de punta y además explicar los conceptos básicos de electroquímica en los que se basa el funcionamiento de las baterías en general.
Se pueden plantear varias preguntas de comprensión, por ejemplo relacionadas con la dirección de la corriente eléctrica o el flujo de electrones; la función del electrolito; y la estequiometría de los compuestos iónicos. Este artículo permite hablar sobre las dificultades que surgen durante el desarrollo de un producto tecnológico, especialmente al mencionar el ejemplo de la durabilidad vs. la capacidad de las baterías. El artículo permite establecer una relación entre la ciencia de materiales y la electroquímica. También es apropiado para tratar temas medioambientales en lo que respecta a dónde y cómo se deben desechar las baterías.
Duarte Nuno Januário, Portugal





