Verso migliori batterie agli ioni di litio Understand article
Tradotto da Rocco G. Maltese. Osserviamo cosa succede agli elettrodi in una batteria agli ioni di litio mediante la scienza dei neutroni.
Le batterie agli ioni di litio forniscono l’energia ai nostri telefoni cellulari e ai nostri computer. Esse hanno iniziato a fornire energia alle nostre automobili, ma lo sviluppo delle automobili elettriche è stato rallentato dai lenti progressi nel campo della tecnologia delle batterie a ioni di litio. Per accelerare questo apprendimento e migliorare ulteriormente la tecnologia delle batterie a ioni di litio, i miei colleghi ed io, recentemente all’Istituto Laue-Langevin (ILL)w1 abbiamo costruito una batteria di grosse dimensioni tanto da poter osservare cosa succede al suo interno mentre è in funzione. La conseguente serie di immagini ‘come in un film’, ha aiutato i ricercatori nella loro opera di miglioramento della costruzione degli elettrodi della batteria.
L’energia del litio
Sappiamo che il litio fa parte dei metalli del gruppo uno situato nell’angolo in alto a sinistra nella tabella periodica degli elementi. Uno dei soli tre elementi creati dal Big Bang, il litio non solo fornisce l’energia al tuo computer portatile – ma costituisce anche il carburante bruciato da una stella.
Sulla Terra, prendiamo il litio dal sottosuolo, dove immensi laghi sotterranei contenenti sali di litio forniscono annualmente 25 000 tonnellate di litio sotto forma di metallo. La maggior parte del quale viene utilizzato per realizzare batterie più leggere (di quelle al piombo – N.d.T.) e ricaricabili agli ioni di litio.
Come tutte le batterie, anche quelle agli ioni di litio immagazzinano l’energia usando il potenziale chimico. A differenza di altri tipi di batterie, quelle agli ioni di litio possono essere ricaricabili poiché i suoi reagenti possono essere rigenerati semplicemente facendoli attraversare da una corrente elettrica. Una volta che la batteria è arrivata ad un livello piatto di energia, si può collegare ad un caricatore che utilizza l’energia elettrica per invertire le reazioni chimiche che avvengono nella batteria mentre è in uso.
Non deve sorprendere che le batterie agli ioni di litio funzionano trasferendo la carica mediante gli ioni positivi. Come tutte le batterie, anche questa è costruita avendo due elettrodi: uno positivo, costituito da un composto contenete litio (spesso mediante una transizione di un ossido metallico, per esempio manganese); e uno negativo, spesso costruito in carbonio. Questi due elettrodi sono messi in comunicazione da un elettrolita che fa in modo che i portatori di carica (gli ioni di litio) si muovano tra gli elettrodi. Le due semi reazioni sono, ad esempio:
LiMn2O4 ⇌ Li1-xMn2O4 + xLi+ + xe–
xLi+ + xe– + xC6 ⇌ xLiC6
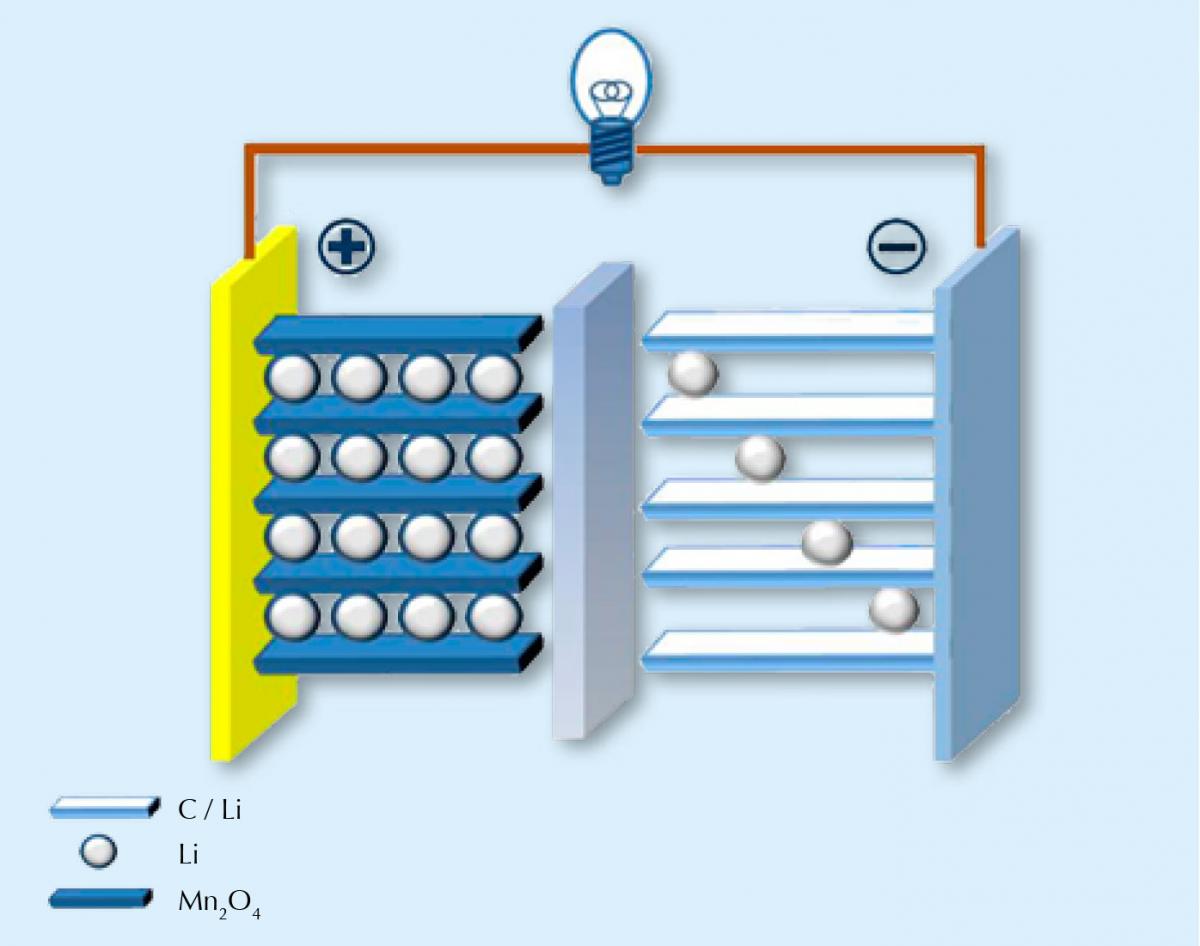
Immagine di pubblico dominio del Chem511 grp ThinLiBat; fonte dell’immagine: Wikimedia Commons
Quando la batteria si sta scaricando (cioè quando sta erogando energia), gli ioni di litio si muovono dall’elettrodo in carbonio all’elettrodo che contiene litio e nuovamente si muovono in direzione opposta quando la batteria viene ricaricata. Sfortunatamente, questo movimento di andare avanti e indietro tra gli elettrodi non può durare in eterno. Dopo un certo tempo, gli ioni di litio entrando ed uscendo dagli elettrodi provocano un lento degrado. Analogamente ai nostri abiti preferiti, iniziano a consumarsi nei punti strategici come i gomiti, e il continuo lavaggio li rendono sempre più lisi, allo stesso modo, gli ioni di litio non riescono a rimanere nel reticolo degli elettrodi. La batteria perde la sua capacità.
Per migliorare le batterie, allora, occorre migliorare la qualità del materiale degli elettrodi – il che significa comprendere come questi materiali si comportano dopo cicli successivi di carica e scarica. Questo è da dove deriva l’ILL e la sua fonte di neutroni, permettendoci di ‘visualizzare’ le variazioni della struttura cristallina degli elettrodi. La diffrazione dei neutroni è una eccellente tecnica di visualizzazione degli ioni di litio che si muovono tra gli elettrodi perché i neutroni sono più facilmente urtati da elementi leggeri come il litio.
Movimento in tempo reale
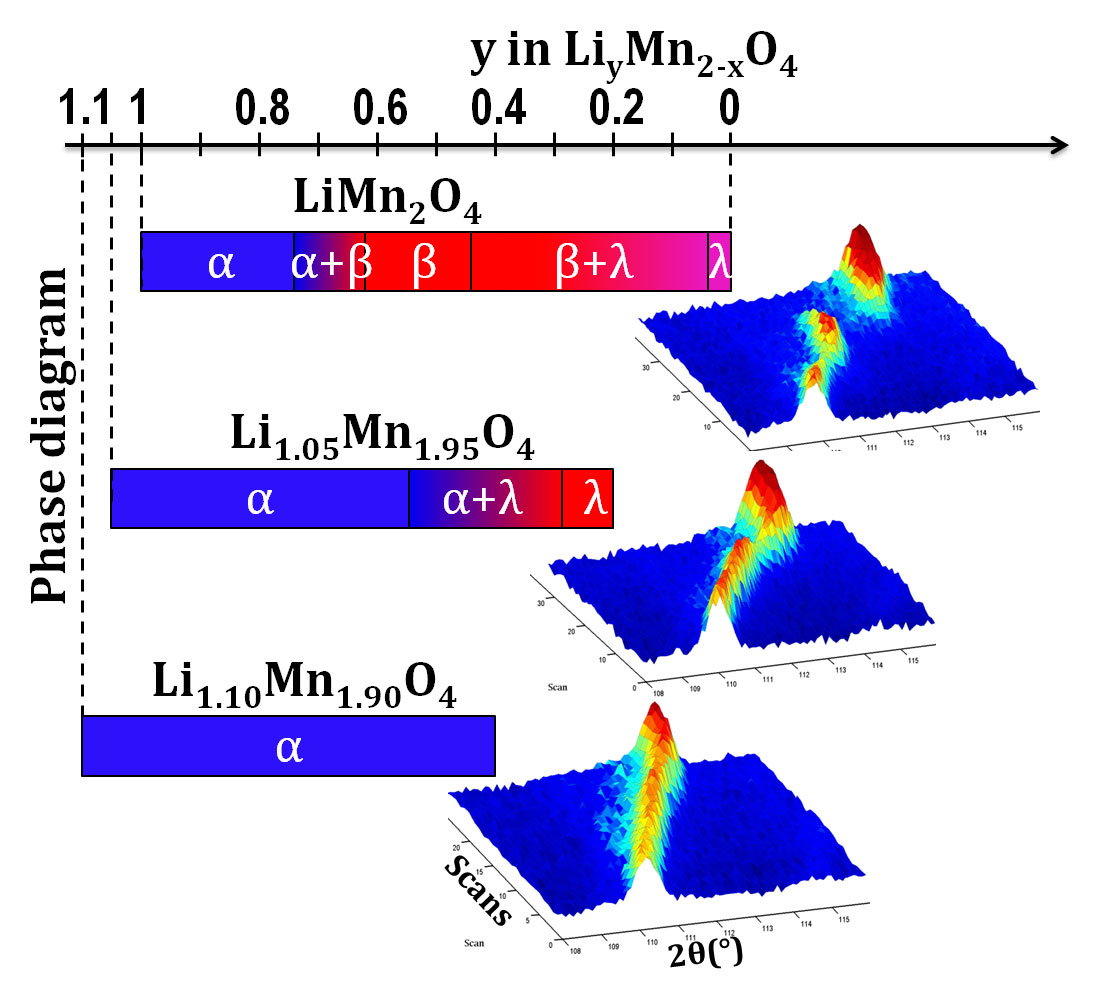
manganese si sottopongono
a differenti modifiche nel
processo di carica e scarica
Immagine per cortesia
dell’autore
Per questa ragione, abbiamo sviluppato una nuova batteria per studiare cosa succede nel materiale degli elettrodi mentre la batteria è realmente in funzione (Bianchini M et al 2013; 2014). Lo scopo era quello di ottenere un film di alta qualità in tempo reale dell’intero processo. Per realizzare questo film si sono utilizzate delle immagini di diffrazione a neutroni attraverso il materiale degli elettrodi mentre la batteria si sta caricando e scaricando. Abbiamo utilizzato le figure di diffrazione come fotogrammi di un film; simile ad un film di animazione o un libro di immagini che viene sfogliato velocemente, permettendoci di osservare cosa succede realmente nell’elettrodo.
Per prima cosa verifichiamo ed ottimizziamo il funzionamento di una singola cella di una batteria, la metodologia e la qualità delle immagini di diffrazione, utilizzando un elettrodo costituito da un materiale che si conosce relativamente bene, il ferro fosfato di litio (LiFePO4). Il LiFePO4 è già disponibile sul mercato, ed è un elettrodo sicuro, di lunga durata, e poco costoso. Una volta che fummo soddisfatti dell’esperimento realizzato ci dedicammo allo studio di elettrodi di materiali più moderni come l’ossido di manganese di litio (LiMn2O4) e ad osservare come differisce il loro comportamento. Il LiMn2O4 è il materiale interessante di un elettrodo positivo con un’alta capacità di sequenze di carica/scarica, sebbene la sua capacità svanisce dopo il ciclo di carica e scarica, impedendo la piena realizzazione di una sua applicazione commerciale. Modificando la formula molecolare del materiale, abbiamo trovato che aggiungendo più litio alla struttura, a spese del manganese, possiamo evitare questa sfida.
Basando il nostro lavoro sulla formula molecolare del LiMn2O4, abbiamo formato tre composti con la formula Li1+xMn2-xO4, dove x è la quantità di litio extra. Questi tre composti avevano valori di x di 0, 0.05 e 0.10. Osservando come i materiali si modificano durante la carica, abbiamo trovato che l’extra litio riduce la capacità d’uso della batteria ma elimina il problema della dissolvenza della capacità. La batteria non mantiene la carica iniziale ma dura più a lungo ad uno stesso livello.
Ed ecco il perché:
- La variazione di volume indotto dalla perdita di ioni di litio è pari alla quantità di litio guadagnata dal materiale dell’elettrodo, e viene modificato il meccanismo fisico per il quale questo fenomeno succede.
- Quando la quantità di litio viene aumentata, allora si riduce la quantità di Mn3+ di una quantità equivalente, e noi sappiamo che questo mette a repentaglio la lunga vita delle batterie di questa specie.
Per questo, il materiale con il più alto contenuto di litio rappresenta un materiale migliore per la batteria.
Non solo abbiamo dimostrato che la diffrazione a neutroni ci può aiutare nella comprensione del comportamento degli ioni di litio e delle batterie a ioni di litio, ma abbiamo anche trovato con un esempio reale come migliorare questo tipo di batterie. Dati questi promettenti risultati, si potrà allargare l’applicazione di altre composizioni di materiale come quelli contenenti come elemento aggiuntivo, il nichel (LiMn1.6Ni0.4O4), potendo operare ad un voltaggio più elevato e avendo così maggior energia a disposizione. E’ possibile che un giorno le nostre automobili possano viaggiare più velocemente e durare molto più a lungo.
La batteria trasparente
La speciale batteria che abbiamo utilizzato per l’esperimento ha gli elettrodi più grandi di quelli normali così da ottenere una più alta qualità per l’analisi delle immagini di diffrazione dei neutroni. La più importante caratteristica di questa batteria speciale riguarda l’utilizzo di una lega di titanio e zirconio, che è noto sia trasparente ai neutroni – cioè i neutroni vi passano attraverso senza essere diffratti. In questo modo, si poterono ricevere solo i segnali provenienti dall’elettrodo, evitando altri contributi indesiderati proveniente dalla cella. Abbiamo utilizzato anche un elettrolita contenente deuterio, dove gli atomi di idrogeno sono stati sostituiti dal più pesante deuterio, per ridurre ulteriormente la dispersione e migliorare il segnale ottenuto.
Nonostante le dimensioni della batteria più grandi della media, i campioni che abbiamo ottenuto per lo studio erano ancora piccoli (≈200 mg) rispetto a quanto normalmente richiesto per gli esperimenti che utilizzano diffrazione a neutroni (≈1 g). Ma grazie alla grande potenza della sorgente di neutroni dell’ILL e lo stato dell’arte dei diffrattometri disponibili, abbiamo potuto ottenere le immagini che speravamo di ottenere.

Immagine di Wurzeller [Public domain]; fonte imaggine: Wikimedia Commons
Maggiori informazioni riguardo l’ILL
L’Istituto Laue-Langevin (ILL)w1 è un centro di ricerca internazionale con sede a Grenoble, Francia. E’ stato all’avanguardia nella scienza e tecnologia nella diffrazione a neutroni per oltre 40 anni, sin dal 1972. L’ILL opera con la sorgente di neutroni più potente del mondo, alimentando fasci di neutroni ad un complesso di 40 strumentazioni ad alto rendimento che sono costantemente aggiornati. Ogni anno 1200 ricercatori provenienti da più di 40 paesi visitano l’ILL per condurre ricerche di fisica dello stato condensato, chimica, biologia, fisica nucleare e scienza dei materiali.
ILL è un membro dell’EIROforumw2, l’editore di Science in School.
References
- Bianchini M et al (2013) A New Null Matrix Electrochemical Cell for Rietveld Refinements of In-Situ or Operando Neutron Powder Diffraction Data. Journal of the Electrochemical Society 160: A2176–A2183. doi: 10.1149/2.076311jes
- Bianchini M et al (2014) Li-Rich Li1+xMn2–xO4 Spinel Electrode Materials: An Operando Neutron Diffraction Study during Li+ Extraction/Insertion. Journal of Physical Chemistry C 118: 25947–25955. doi: 10.1021/jp509027g
Web References
- w1 – Per saperne di più ILL.
- Consulta l’elenco di tutti gli articoli relativi a ILL in Science in School.
- w2 – EIRO forum è una collaborazione tra le otto maggiori organizzazioni governative di ricerca scientifica, che condividono le loro risorse, strumentazioni e laboratori ed esperienze affinché la ricerca Europea sia sostenuta nel raggiungimento del suo pieno potenziale. EIROforum come parte integrante delle sue finalità educative e diffusione delle scienze, pubblica Science in School.
Resources
- Gli scienziati all’European Synchrotron Radiation Facility (ESRF) a Grenoble, Francia, lavorano anche sulle batterie a ioni di litio e vi è un interessante articolo sul loro lavoro a pagg. 16 e 17 del numero di Luglio 2015 di ESFR news.
Institutions
Review
Le batterie agli ioni di litio è una delle più importanti applicazioni dell’elettrochimica presente nella vita di tutti i giorni degli studenti. Tuttavia, la loro bassa capacità e durata sono fattori che hanno ritardato la loro implementazione, per esempio nei veicoli elettrici.
Gli scienziati dell’Istituto Laue-Langevin (ILL) spiegano in questo articolo alcuni dei loro lavori tesi a migliorare le caratteristiche delle batterie agli ioni di litio. Gli insegnanti possono utilizzare l’articolo non solo per esporre un esempio della ricerca d’avanguardia, ma anche per spiegare in classe i concetti dell’elettrochimica che stanno alla base nel funzionamento delle batterie in generale.
Diverse domande potrebbero essere avanzate, riguardanti per esempio la direzione della corrente elettrica, o il flusso di elettroni; il ruolo dell’elettrolita; o anche la stechiometria dei composti ionici. L’articolo può essere utilizzato per discutere le difficoltà che sorgono nello sviluppo di un prodotto tecnologico sfruttando ad esempio la durata delle batterie rispetto alla loro capacità di immagazzinare energia. Permette altresì un collegamento tra la scienza dei materiali e l’elettrochimica. Può anche insorgere la problematica dello smaltimento delle batterie fuori uso.
Duarte Nuno Januário, Portogallo





