Lesiones medulares: ¿tienen la solución las células madre? Understand article
Traducido por I. Carrero, Univ. de Valladolid. Las lesiones medulares producen con frecuencia parálisis permanente y en la actualidad todavía no tienen cura. ¿Podría aportar esperanza contra ellas la terapia con células madre?
Wikimedia Commons
El actor y activista americano Christopher Reeve será recordado por su papel protagonista en la exitosa película de 1978 Supermán. Por desgracia, también se le recordará como un hombre cuya vida extraordinariamente activa, tanto dentro como fuera de la pantalla, se vio truncada tras un grave accidente que le dejó paralítico desde el cuello –estado en el que permaneció hasta su muerte en 2004.

en 2003 los posibles
beneficios de la investigación
con células madre en una
conferencia sobre
neurociencia en el MIT
(Instituto de Tecnología de
Massachusetts, EE. UU.).
Imagen cortesía de Mike Lin /
Wikimedia Commons
En mayo de 1995, durante una competición ecuestre, Reeve cayó de cabeza desde su caballo. El impacto del golpe se transmitió a través de la columna y se le rompieron dos vértebras del cuello lo que le provocó una importante lesión medularw1.
¿Qué sucedió durante el accidente –a nivel circulatorio, óseo, celular y molecular– para producir esa parálisis permanente? ¿Cómo puede proporcionar esperanzas a la gente con lesiones medulares la investigación sobre nuevos tratamientos basados en las células madre?, ¿podría ayudarles a recuperar el control de sus cuerpos y sus vidas?
¿Qué son las lesiones medulares?
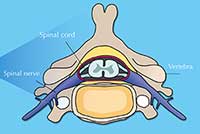
La médula espinal es una vía de comunicación entre el cerebro y el resto del organismo (Figura 1). Las lesiones medulares normalmente se deben a traumas repentinos, como los que se producen practicando ciertos deportes o en accidentes de coche, que producen luxaciones o rotura de vértebras que acaban afectando a la médula espinal al dañar o presionar los axones neuronales. El control sensorial y el motor se pierden por debajo del punto donde se produce el daño (Figura 2).
Múltiples células mueren en la zona donde se produce la lesión, o en sus alrededores, debido a los efectos secundarios del trauma: cambios en el riego sanguíneo, respuesta inmune y aumento de radicales libres y de neurotransmisores excitadores (ver recuadro sobre efectos secundarios del daño medular).
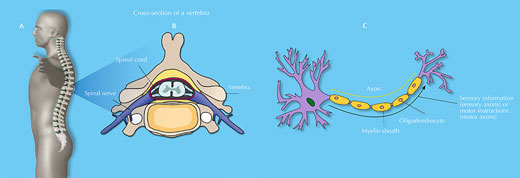
La médula espinal es una estructura blanda y gelatinosa que se extiende desde la base del cráneo hasta el final de la columna (A). Tiene 38-43 cm de longitud y, en su zona más ancha, su grosor puede ser como el de un pulgar. Se encuentra en el canal que atraviesa la columna vertebral a lo largo de las 33 vértebras que la forman (B).
Los nervios espinales (que forman parte del sistema nervioso periférico) se conectan a la médula en distintas zonas a lo largo de su longitud; estos nervios pueden salir hacia regiones concretas del cuerpo o llegar desde estas. En conjunto, la médula espinal y el cerebro forman elsistema nervioso central.
La médula espinal consta de neuronas sensoriales y motoras (C). Los axones sensoriales llevan información sensorial de distintas zonas del cuerpo hasta el cerebro, mientras que los motores llevan instrucciones motoras (tanto voluntarias como involuntarias) en dirección opuesta. Las neuronas de la médula están acompañadas por diferentes células gliales, como oligodendrocitos–que rodean la mielina que envuelve los axones, aislando eléctricamente a estos y facilitando así la transmisión rápida y eficaz del potencial de acción– y astrocitos –con múltiples funciones, como el aporte de nutrientes y la liberación de factores de crecimiento necesarios para otras células neurales.
Imágenes cortesía de Debivort / Wikimedia Commons (vertebra); Faigl.ladislav / Wikimedia Commons (neurona); Barnabé-Heider & Frisén (2008), con permiso de Elsevier (cuerpo humano)
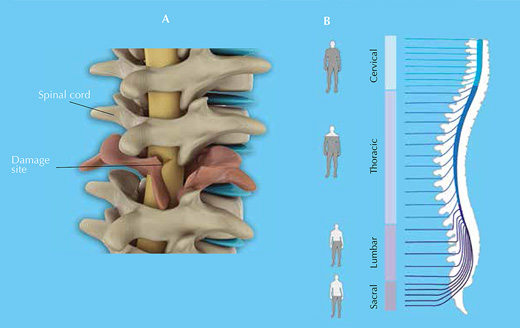
Imágenes cortesía de Barnabé-Heider & Frisén (2008), con permiso de Elsevier
Efectos secundarios del daño medular
Los efectos secundarios que tienen lugar cuando se produce una lesión medular conducen a la muerte de diversos tipos celulares, incluyendo neuronas y oligodendrocitos. Estos efectos pueden ser:
- Isquemia: disminución del riego sanguíneo (debido a la rotura de vasos sanguíneos) que hace que se reduzca el aporte de oxígeno y nutrientes a las células.
- Edema: acumulación de líquido en los tejidos que produce inflamación y también reduce la eficacia del intercambio de nutrientes y otras moléculas entre la sangre y las células de la médula espinal.
- Invasión inmune: la lesión produce una respuesta inflamatoria que provoca la llegada de células del sistema inmune (neutrófilos, linfocitos T, macrófagos y monocitos) a esa zona de la médula espinal. Esta respuesta puede ser protectora (gracias a la liberación de moléculas que promueven la reparación del daño y la eliminación del tejido dañado) pero también puede tener consecuencias perjudiciales (como la inflamación que afecta al tejido sano).
- Liberación de neurotransmisores: las neuronas dañadas liberan cantidades elevadas de un neurotransmisor excitador, el glutamato, que sobreexcita a las células neurales, pudiendo bloquear su función o, incluso, llegar a matarlas.
- Producción de radicales libres: el daño celular y la respuesta inflamatoria hacen que aumenten los niveles de radicales libres que provocarán daños adicionales a las células neurales al reaccionar con moléculas cruciales para determinadas funciones celulares.
Tratamientos actuales: limitación del daño
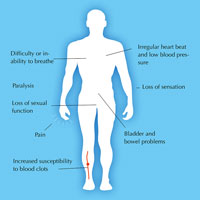
del daño medular. Haga clic
sobre la imagen para
ampliarla.
Imagen cortesía de Nicola Graf
El organismo no puede reemplazar por sí solo las células que se pierden como resultado de una lesión medular, de manera que se pierde su funcionalidad. En la actualidad, los tratamientos a corto plazo simplemente se limitan a reducir el daño: cirugía, para liberar la presión sobre la médula y estabilizar la columna, o inmovilización (mediante corsés) para evitar daños posteriores. A largo plazo, los pacientes reciben fisioterapia y otros tratamientos que les alivian los síntomas relacionados con su lesión, como el dolor, así como consejos para ayudarles a afrontar su nueva situación (Figura 3).
Hasta el momento, las lesiones medulares, acompañadas de un intenso sufrimiento físico y emocional, no tienen cura. Sin embargo, diversos grupos científicos están investigando la posibilidad de usar las células madre para tratarlas.
Terapias con células madre
Las células madre son células que pueden tanto diferenciarse para dar tipos celulares concretos como autoperpetuarse y producir más células madre. En líneas generales, hay dos tipos: células madre pluripotentes, que se pueden diferenciar para dar cualquier tipo celular, y células madre adultas, que solo se diferencian para dar ciertos tipos celulares. Las células madre pluripotentes se pueden obtener bien extrayéndolas de embriones (células madre embrionarias), bien generándolas en el laboratorio (células madre pluripotentes inducidas –células iPS, de las siglas en inglés–) a partir de células especializadas, como las de pielw2. Las células madre adultas se encuentran en distintos tejidos, p. ej. la médula ósea.
Hay dos estrategias posibles para utilizar las células madre en las lesiones medulares:
- Transplantar células madre en la zona dañada.
- Reclutar células madre neurales residentes (propias) de la médula dañada.
En ambos casos, la intención es que las células madre reemplacen a las células de la médula dañadas o perdidas, o que promuevan su recuperación de forma indirecta. Esta segunda vía se puede producir debido a las propias células madre o mediante las células que se originen de ellas.
1) Transplante de células madre
Estudios sobre lesiones medulares llevados a cabo con modelos animales (sobre todo con roedores) han mostrado que la terapia con transplantes puede facilitar la recuperación, aunque es difícil saber qué mecanismos participan. En estos estudios se han usado tres tipos de células madre: pluripotentes, adultas no neurales y neurales (tanto adultas como embrionarias).
Células madre pluripotentes
El transplante a animales de experimentación de células madre pluripotentes ha tenido algunos efectos secundarios, como la formación de tumores. Antes de su aplicación contra el daño medular, las células se tratan para conseguir que se diferencien en células neurales progenitoras –células con el potencial de diferenciarse en tipos concretos de células neurales especializadas–. En un estudio se vio que siete días después de haber transplantado células progenitoras de oligodendrocitos a ratas con daño medular, los axones se remielinizaron y mejoró la capacidad de estos animales para mover las patas (Keirstead et al., 2005).
Células madre adultas no neurales
Las células madre adultas no neurales se obtienen de distintos tejidos, como médula ósea, tejido adiposo y placenta. Se cree que estas células favorecen la reparación de las lesiones medulares de forma indirecta. Diversos estudios muestran que la movilidad y la sensibilidad de los animales de experimentación mejoraron después de haberles sido transplantadas estas células (Parr et al., 2007).
Células madre neurales
Las células madre neurales se extraen de distintas zonas del sistema nervioso de embriones o de adultos. Varios estudios muestran que las células transplantadas se diferencian en astrocitos que favorecen el crecimiento de nuevas células neurales (Enzmann et al., 2006; Pfeifer et al., 2006). Una investigación publicada recientemente planteaba que las células madre neurales pueden reprogramar la respuesta inflamatoria local a la lesión al reducir la proporción de células inmunes dañinas (como los macrófagos) al tiempo que promueven la reparación de la lesión (Cusimano et al., 2012). En muchos trabajos que han estudiado la recuperación tras el transplante de células madre neurales, los animales utilizados ganaron movilidad en las patas.
2) Reclutamiento de células madre residentes
El transplante de células madre es arriesgado: requiere una delicada operación quirúrgica y, en el caso de células madre embrionarias y neurales, el sistema inmune puede rechazarlas. Estos riesgos se podrían evitar con un enfoque alternativo mediante el uso de fármacos para inducir la recuperación mediante las células madre neurales residentes (Barnabé-Heider & Frisén, 2008).
Incluso aunque los riesgos asociados se puedan superar, la investigación en este tratamiento potencial, conocido como terapia de reclutamiento de células madre, está en sus inicios y aún no se sabe si puede ayudar a recuperar las lesiones medulares en animales.
Pequeños cambios con grandes consecuencias
Comprender los mecanismos implicados, probar la eficacia en animales, llevar a cabo ensayos clínicos en humanos: el desarrollo de nuevos tratamientos es un proceso lento y complicado. Al menos por ahora, la terapia mediante transplante es una de las principales esperanzas para el tratamiento del daño medular con células madre. En 2010, la compañía californiana Geron empezó un ensayo clínicow3 basado en este enfoque, pero tuvo que abandonarlo debido a problemas económicos. En la actualidad, el Hospital Universitario Balgrist de Zurich (Suiza) está realizando ensayos clínicosw4 con células derivadas de tejido cerebral humano. La esperanza es que, cuando se transplanten en una médula espinal lesionada, estas células puedan restablecer algunos de los circuitos necesarios de la red nerviosa que transmite la información por todo el cuerpo.
Dada la naturaleza multifactorial del daño medular, es improbable que un solo tratamiento pueda curarlo pero incluso pequeñas mejoras podrían constituir grandes aportes a la vida diaria de los pacientes. Imagina: si, como Christopher Reeve, estuvieras paralizado desde el cuello, volver a ser capaz de mover los brazos y agarrar cosas con las manos podría marcar la diferencia entre vivir de forma dependiente o independiente.
Agradecimientos
Este artículo se basa en una ficha técnica de la página web de Eurostemcellw5 y en un artículo de revisión de Barnabé-Heider & Frisén (2008).
El autor quiere agradecer a Kate Doherty, de EuroStemCell, su ayuda en la planificación y la redacción del artículo. También le agradece al doctor Stefano Pluchino, del Departamento de Neurociencias Clínicas de la Universidad de Cambridge (Reino Unido), sus expertos consejos.
References
- Barnabé-Heider F, Frisén J (2008) Stem cells for spinal cord repair. Cell Stem Cell3(1): 16-24. doi: 10.1016/j.stem.2008.06.011
- Cusimano M et al. (2012) Transplanted neural stem/precursor cells instruct phagocytes and reduce secondary tissue damage in the injured spinal cord. Brain.135(2): 447-60. doi: 10.1093/brain/aws002
- Enzmann GU et al. (2006) Functional considerations of stem cell transplantation therapy for spinal cord repair. Journal of Neurotrauma 23: 479–495. doi:10.1089/neu.2006.23.479
- Keirstead HS et al. (2005). Human embryonic stem cell-derived oligodendrocyte progenitor cell transplants remyelinate and restore locomotion after spinal cord injury. The Journal of Neuroscience 25: 4694–4705. doi: 10.1523/JNEUROSCI.0311-05.2005
- Parr AM et al. (2007). Bone marrow-derived mesenchymal stromal cells for the repair of central nervous system injury. Bone Marrow Transplant 40: 609–619. doi: 10.1038/sj.bmt.1705757
- Pfeifer K et al. (2006). Autologous adult rodent neural progenitor cell transplantation represents a feasible strategy to promote structural repair in the chronically injured spinal cord. Regenerative Medicine 1: 255–266. doi:10.2217/17460751.1.2.255
Web References
- w1 – La Fundación Christopher y Dana Reeve financia investigaciones sobre el tratamiento de las lesiones medulares para así mejorar la calidad de vida de las personas afectadas.
-
La página web incluye vídeos sobre gente con parálisis hablando sobre sus experiencias.
-
- w2 – En 2012, John Gurdon y Shinya Yamanaka recibieron el premio Nobel en Fisiología y Medicina por descubrir la posibilidad de reprogramar células adultas para convertirlas en pluripotentes.
-
Puedes leer más sobre células madre pluripotentes embrionarias e inducidas en la página web de Nature Education’s Scitable.
-
En un vídeo disponible en la página web de EuroStemCell, «Stem cells – the future: an introduction to iPS cells» (Células madre: el futuro. Introducción a las células iPS), destacados científicos cuentan la historia de las células madre pluripotentes inducidas.
-
- w3 – Lea sobre el ensayo clínico de Geron en el New York Times.
- w4 – Lea más sobre el ensayo clínico del Hospital Universitario de Balgrist en la página web Clinical Trials.
- w5 – Descargue la ficha técnica Spinal cord injuries: how could stem cells help? (Lesiones medulares: ¿pueden ayudar las células madre?) de la página web de EuroStemCell.
-
Eurostemcell’s stem cell toolkit (Recursos sobre células madre de EuroStemCell) es una serie de recursos y actividades, que se pueden descargar bajo la licencia Creative Commons, adecuados para cubrir distintos niveles de formación. Ejemplos:
-
Ficha técnica sobre Embryonic stem cell research: an ethical dilemma.
-
Hope Beyond Hype (Esperanza más allá de las grandes expectativas) es un relato sobre las terapias con células madre, desde su descubrimiento hasta la terapia, en forma de cómic interactivo.
-
Ready or not? (¿Estáis listos?) es un juego de rol sobre la utilización de células madre para aplicaciones clínicas diseñado para su uso en clase.
-
Resources
- Para la revisión sobre un DVD para colegios de EuroStemCell, ver:
-
Gebhardt P (2006) Review of A Stem Cell Story. Science in School 3: 88.
-
- Spinal cord injury: progress and promise in stem cell research (Lesiones medulares: progresos y promesas en la investigación sobre células madre) es un breve vídeo sobre un lesionado medular, Roman Reed, abogado y anteriormente jugador de fútbol americano.
- La página web del NINDS (siglas en inglés del Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares de los NIH) tiene información detallada sobre las lesiones medulares.
- La ICCP (International Campaign for Cures of Spinal Cord Injury Paralysis, –Asociación internacional para la cura de la parálisis por daño medular–) tiene estadísticas y otras informaciones sobre las lesiones medulares.
Review
El artículo muestra las posibles consecuencias de las lesiones medulares en humanos, presenta los últimos avances científicos y plantea la posibilidad de futuros tratamientos basados en el uso de células madre.
A los estudiantes más jóvenes (11-14 años) les puede motivar a estudiar el sistema nervioso (p. ej. el arco reflejo) el caso del protagonista de Supermán, Christopher Reeve; pero para ellos habría que simplificar el texto.
El artículo puede ser bastante apropiado para los estudiantes de más edad (15-18 años) debido al nivel de detalles que tiene. Se podría relacionar con anatomía y fisiología del sistema nervioso, con aspectos fisiológicos del sistema inmune y con la proliferación y la diferenciación celulares. La lista de recursos que se ofrece complementa muy bien el artículo.
El artículo también se puede usar como punto de partida para proyectos de investigación interdisciplinares relacionados con química y física. Ejemplos de temas podrían ser: ¿Por qué las células dañadas producen radicales libres y por qué estos son perjudiciales para las células? ¿Con qué moléculas reaccionan primero los radicales libres? ¿Por qué los edemas reducen la eficacia del intercambio de nutrientes y otras moléculas entre sangre y células de la médula espinal? ¿Qué tipo de moléculas pueden favorecer la reparación de la médula espinal?
Además, el artículo puede ser la base para tareas de comprensión y desarrollo como:
- Diferenciar las células madre pluripotentes de las células madre adultas neurales y no neurales (tanto adultas como embrionarias) y considerar su potencial para generar células madre neurales especializadas. Relacionar esto con los mecanismos de regulación génica.
- «Las células madre pluripotentes se pueden obtener de embriones (células madre embrionarias) o se pueden generar en el laboratorio a partir de células especializadas, como las de piel (células madre pluripotentes inducidas)». «El transplante de células madre pluripotentes a animales puede tener graves efectos secundarios, como la formación de tumores». Relaciona estas afirmaciones con los procesos de diferenciación celular y regulación genética.
- «El transplante de células madre es arriesgado: conlleva un delicado procedimiento quirúrgico y, en el caso de células madre embrionarias y neurales, el sistema inmune puede rechazar las células que se transplantan». Explica el mecanismo biológico en que se basa este riesgo.
Betina da Silva Lopes, Portugal





