Omurilik hasarı: kök hücreler cevaba sahip mi? Understand article
Tercüme eden: Canbolat Gürses ve Hikmet Geçkil (İnönü Üniversitesi, Moleküler Biyoloji ve Genetik Bölümü). Omurilik hasarı tipik olarak kalıcı felce yol açar ve şu an için tedavisi olmayan bir durumdur. Kök hücre tedavisi umut sağlayabilir mi?
Commons’un izniyle
Amerikalı aktör ve aktivist Christopher Reeve 1978’de hâsılat rekoru kıran Superman filminde öne çıkan rolüyle hatırlanacak. Perde önü ve arkasındaki aktif hayatının acı bir kaza sonucu altüst olup, 2004’teki ölümüne kadar boynundan aşağısının felç olması ile de hatırlanacak.

Teknoloji Enstitüsündeki
sinir bilim konferansında
Christopher Reeve kök
hücrelerinin potansiyel
yararlarını tartışıyor.
Resim Mike Lin/Wikimedia
Commons’un izniyle
Mayıs 1995’te, bir binicilik yarışması sırasında, Reeve atından kafa üstü düştü. Vücudunun ağırlığı omurgasına binerek boynundaki iki omurunun kırılmasına ve aşırı derecede omurilik hasarınaw1 neden oldu.
Bu kaza sırasında kan, kemik, hücre ve molekül düzeyinde ne oldu da bu durum onun hayat boyu felç kalmasına neden oldu? Kök hücrelere dayalı yeni tedaviler, omurilik hasarına bağlı felç insanlara umut vaat etmekte midir? Bu tedavi şekli, bu insanların vücutlarının ve hayatlarının kontrolünü tekrar ellerine almalarında yardımcı olabilir mi?
Omurilik hasarı nedir?
Omurilik, beyninizi vücudunuzun kalanına bağlayan bir bilgi otoyoludur (Şekil 1). Omurilik hasarları genellikle spor veya araba kazaları gibi ani travmalardan kaynaklanır. Bu tür kazalarda omurga kayarak veya parçalanarak omurilik dokusunun içine girer ve aksonlara zarar verir. Bu durum, yaralanmanın olduğu yerden aşağıda kalan tüm vücutta duyu ve motor kontrolünün kaybolmasına sebep olur (Şekil 2).
Travmanın ikincil etkisine bağlı olan kan ihtiyacındaki değişiklik, bağışıklık yanıtlar, serbest radikallerin ve uyarıcı nörotransmitterlerin artması gibi sebeplerden dolayı, omurilik yaralanmasının olduğu yer ve çevresinde birçok hücre çeşidi ölür (omurilik yaralanmasının ikincil etkileri için kutucuğa bakınız).
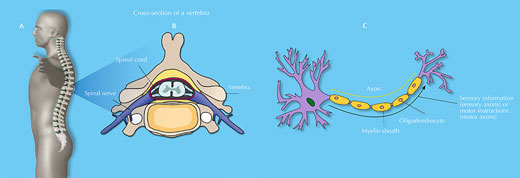
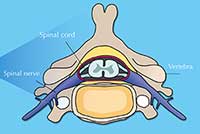
Omurilik, beyin sapından bele kadar uzanan yumuşak, jelimsi bir yapıdır (A). Uzunluğu 38 ila 43 cm, kalınlığı başparmak genişliğindedir. Omurilik, omurga sütununun 33 sıkı omurunun içinden geçen oyuklu kanala oturur (B).
Omurilik sinirleri (periferal sinir sisteminin parçası) omuriliğin uzunluğu boyunca çeşitli aralıklarla bağlıdır ve vücudun spesifik bölgelerine uzanır. Omurilik ve beyin merkezi sinir sistemini oluşturur.
Omurilik duyu ve sinirlerini içerir (C). Duyu aksonları vücuttan beyne his bilgilerini taşır, oysa motor aksonları istemli ve istemsiz motor hareketlerini ters yönde taşır. Omurilik sinirleri, çeşitli gliyal hücreler tarafindan desteklenirler. Örneğin bu gliyal hücrelerden oligodentrositler, aksonların etrafındaki miyelinleri sararak onları yalıtması sonucunda akson potansiyelinin hızlı ve etkili iletimini sağlarken, astrositler diğer sinir hücreleri için besleyici madde sağlama ve büyüme faktörleri salınımı gibi çoklu fonksiyonlara sahiptir.
Debivort’un müsadesiyle/Wikimedia Commons (omurga); Faigl.ladislav /; Wikimedia Commons (nöron); Elsevier Barnabé-Heider & Frisén (2008), izniyle
Barnabé-Heider & Frisén (2008)’in müsadesiyle ve Elsevir’in izniyle
Omurilik hasarının ikincil etkileri
Omurilik yaralanması sırasında yer alan ikincil etkiler sinir ve oligodendrositleri içeren çok sayıda hücre çeşidinin ölümüne yol açar. Bu ikincil etkiler:
- İskemi: uygun kan beslemesinin eksikliği (kan damarlarının çatlamasına bağlı olarak). Bu, hücrelere oksijen ve besin tedarikini azaltır.
- Ödem: doku sıvısı toplanması. Bu, şişmeye yol açar ve kanla omurilik hücreleri arasındaki besin maddelerinin ve moleküllerin değişimindeki verimi azaltır.
- Bağışıklık istilası: yaralanma, yangı (enflamasyon) yanıtını tetikleyerek yaralanma bölgesi ve civarındaki omuriliğe bağışıklık hücrelerinin (nötrofil, T-hücreleri, makrofajlar ve monositler) akın etmesine yol açar. Bu yanıt hem koruyucu (örn., omurilik tamirini destekleyen moleküllerin salınması ve hasarlı dokuların temizlenmesi) ve hem de zararlı olabilir (örn., enflamasyondan sağlıklı dokuların da etkilenmesi).
- Nörotransmitter salınımı: glutamat uyarıcı bir nörotransmitter olup, zarar görmüş nöronlar tarafından bol miktarda salınır. Bu nörotransmitter sinir hücrelerinin aşırı uyarılmasını sağlayarak, onların ölümüne ya da işlevlerinin kaybolmasına neden olur.
- Serbest radikal salınımı: hücre hasarı ve inflamasyon yanıt, düzgün hücresel fonksiyonlar için çok önemli olan moleküllerle reaksiyona girerek sinir hücrelerine başka hasarlar veren serbest radikallerin düzeyini yükseltir.
Varolan tedaviler: hasar sınırlandırılması
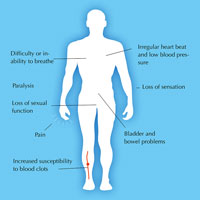
yaralanmasının potansiyel
semptomları. Resmi
büyütmek için tıklayın.
Nicola Graf’ın izniyle
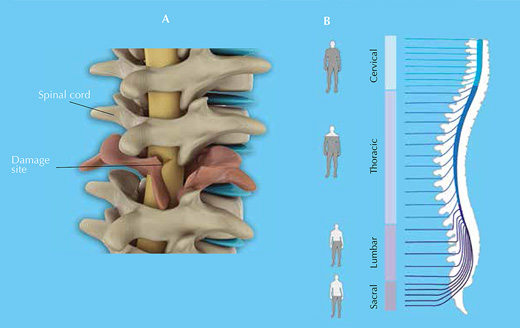
Omurilik hasarı sonucu meydana gelen hücre kaybı vücudun kendisi tarafından yerine konamaz ve böylece omurilik fonksiyonu kalıcı olarak kaybolur. Günümüz kısa dönem tedavileri sadece zararın azaltılmasını içerir (örn., omurilik üzerindeki basıncı dindirilmek için cerrahi müdahale). Uzun dönemde, hastalara ağrı ve kazayla ilişkili semptomları rahatlatıcı fizyoterapi ve tedavilerin yanı sıra danışmanlık da verilir (Şekil 3).
Omurilik hasarının şu an için tedavisi olmayıp, yoğun fiziksel ve duygusal bir sürece sebep olur. Ancak bazı bilim çevreleri tarafından son zamanlarda kök hücrelerin omurilik hasarındaki kullanım potansiyelleri araştırılmaya başlanmıştır.
Kök hücre tedavileri
Kök hücreler hem özel hücre çeşitlerine farklılaşabilir hem de kendi kendilerini yenileyerek daha çok kök hücre üretebilirler. Genel nlamda iki çesit kök hücre vardır: herhangi bir vücut hücresine farklılaşabilen pluripotent kök hücreler ve sadece bazı tip hücrelere farklılaşabilen yetişkin kök hücreler. Pluripotent kök hücreler embriyolardan (embriyonik kök hücreler) elde edilebilir veya deri hücreleriw2 gibi özelleşmiş hücrelerden laboratuarda oluşturulabilirler (indüklenmiş pluripotent kök hücreler). Yetişkin kök hücreler ise kemik iliği gibi çeşitli dokularda bulunurlar.
Omurilik yaralanmasında kök hücrelerin kullanıldığı iki potansiyel yaklaşım vardır:
- Yaralanan bölgeye kök hücrelerin transplantasyonu.
- Hasar görmüş omurilikteki sinir kök hücrelerinin kullanılması.
Her iki yaklaşımda da amaç, zarar görmüş omurilik hücrelerinin yerine bunlara dönüşecek kök hücreler koymak veya dolaylı olarak iyileşmeyi teşvik etmeye dayanır. Bu dolaylı yarar kök hücrelerin kendisinden ya da farklılaştıkları hücrelerden gelebilir.
1) Kök hücre transplantasyonu
Model hayvanlar (genellikle kemirgenler) üzerinde yapılan omurilik hasarı tedavi çalışmaları, transplantasyon tedavisinin iyileşmeye yardımcı olduğunu göstermiştir. Ancak, bu iyileşmede hangi mekanizmaların sorumlu olduğu henüz bilinmemektedir. Bu çalışmalarda, üç çeşit kök hücre kullanılır: pluripotent kök hücreler, nöral olmayan yetişkin kök hücreler ve nöral kök hücreler (yetişkinden veya embriyodan elde edilen).
Pluripotent kök hücreler
Pluripotent kök hücrelerin hayvanlara transplantasyonu tümör oluşumu gibi çeşitli ciddi yan etkilere yol açar. Omurilik yaralanmasının etkili tedavisinde kullanılmadan önce bu hücreler nöral progenitör hücrelere (özel nöral hücrelerin belirli biçimlerine farklılaşma potansiyeline sahip olan hücreler) farklılaşmaları için muamele edilir. Bir çalışma oligodendrosit progenitör hücrelerin omurilik yaralanmasına sahip sıçanlara transplantasyonundan yedi gün sonra aksonların yeniden miyelinlendiğini ve sıçanların ayaklarını daha iyi hareket ettirebildiklerini göstermiştir (Keirstead ve ark., 2005).
Nöral olmayan yetişkin kök hücreler
Nöral olmayan yetişkin kök hücreler kemik iliği, yağ dokusu ve plasenta gibi çeşitli dokulardan çıkarılır. Bu kök hücrelerin omurilik yaralanmasını dolaylı olarak tamir etmede yardımcı oldukları düşünülmektedir. Birçok çalışma bu hücrelerin transplantasyonundan sonra hayvanların daha iyi hareket edip hissettiklerini gösternektedir (Parr ve ark., 2007).
Nöral kök hücreler
Nöral kök hücreler embriyo veya yetişkinlerin sinir sistemlerinin belli kısımlarından çıkarılır. Birçok çalışma transplantasyon yapılan hücrelerin yeni nöral hücrelerin büyümesine yardım eden astrositlere farklılaştığını göstermektedir (Enzmann ve ark., 2006; Pfeifer ve ark., 2006). Geçen yıl yayınlanan bir araştırma, nöral kök hücrelerin yaralanmaya karşı lokal inflamatuar yanıtını yeniden programlayabildiğini ve böylece makrofajlar gibi yıkıcı bağışıklık hücrelerinin azaltılması hasarlı omuriliğin iyileşmesini teşvik ettiğini ortaya koymuştur (Cusimano ve ark., 2012). Birçok araştırma, nöral kök hücre transplantasyonundan sonra hayvanların ayaklarını daha iyi hareket ettirdiğini ortaya koymuştur.
2) Yerleşik kök hücrelerden yararlanma
Kök hücrelerin transplantasyonu riskli bir iş olup hassas bir cerrahi prosedür gerektirir ve (embriyonik ve nöral kök hücre kullanımı durumlarında) immün sistemin yeni hücreleri reddedebileceği olasıdır. Omuriliğin yerleşmiş nöral kök hücrelerinin ilaç yardımı ile tedaviyi teşvik etmesinde alternatif bir yaklaşım olarak kullanılması bu riski azaltabilir (Barnabé-Heider & Frisén, 2008).
Bu risklerin üstesinden gelinilse bile, kök hücre iyileştirme tedavisi olarak bilinen bu potansiyel terapideki araştırma hala erken bir aşamadadır ve hayvanlardaki omurilik hasarından iyileşmeye yardımcı olup olmadığı henüz gözlemlenmemiştir.
Küçük değişiklikler büyük farklar yaratabilir
İlişkili mekanizmayı anlamak, hayvanlardaki etkinin testi, insanlardaki klinik deneme (tedavi geliştirme) süreçleri yavaş ve karmaşıktır. En azından şimdilik, transplantasyon tedavisi kök hücrelerle omurilik hasarının tedavisi için büyük bir umudu barındırmaktadır. 2010’da, Kalifornya’lı şirket Geron bu yönteme dayanarak bir klinik deneme başlatmasınaw3 rağmen finansal nedenlerden bunu durdurmak zorunda kalmıştır. Son olarak, Zürih (İsviçre)’deki Balgrist Üniversitesi Hastanesi, insan beyin dokusundan elde edilen hücrelerin kullanıldığı bir denemew4 yürütüyor. Hasarlı omuriliğe bu hücrelerin transplantasyonu ile vücut etrafında bilgi taşıyan sinir ağı için önemli olan devrelerin yeniden kurulması umut edilmektedir.
Çok yönlü doğasından dolayı omurilik hasarının her hangi tek bir uygulamanın sonucu tedavisinin yapılabilirliği şüphelidir. Ancak çok küçük gelişmeler bile hastaların hayatlarında büyük bir fark yaratacaktır. Christopher Reeve gibi boyundan altınızın felç olduğunu hayal edin: kollarınızı hareket ettirebilmeniz ve ellerinizle sıkıca tutabilmeniz bile bağımlı veya bağımsız yaşam arasında fark yaratırdı.
Teşekkür
Bu makale Eurostemcell websitew5, ve Barnabé-Heider & Frisén (2008) derleme makalesi için yaratılan bilgi formuna dayanmaktadır.
Yazar, makalenin yazımı ve planlanmasındaki yardımı için Eurostemcell’den Kate Doherty’e teşekkür etmektedir. University of Cambridge, Klinik Sinirbilimleri Bölümü’nden Dr Stefano Pluchino’ya uzman tavsiyeleri için de teşekkürler.
References
- Barnabé-Heider F, Frisén J (2008) Stem cells for spinal cord repair. Cell Stem Cell3(1): 16-24. doi: 10.1016/j.stem.2008.06.011
- Cusimano M et al. (2012) Transplanted neural stem/precursor cells instruct phagocytes and reduce secondary tissue damage in the injured spinal cord. Brain.135(2): 447-60. doi: 10.1093/brain/aws002
- Enzmann GU et al. (2006) Functional considerations of stem cell transplantation therapy for spinal cord repair. Journal of Neurotrauma 23: 479–495. doi:10.1089/neu.2006.23.479
- Keirstead HS et al. (2005). Human embryonic stem cell-derived oligodendrocyte progenitor cell transplants remyelinate and restore locomotion after spinal cord injury. The Journal of Neuroscience 25: 4694–4705. doi: 10.1523/JNEUROSCI.0311-05.2005
- Parr AM et al. (2007). Bone marrow-derived mesenchymal stromal cells for the repair of central nervous system injury. Bone Marrow Transplant 40: 609–619. doi: 10.1038/sj.bmt.1705757
- Pfeifer K et al. (2006). Autologous adult rodent neural progenitor cell transplantation represents a feasible strategy to promote structural repair in the chronically injured spinal cord. Regenerative Medicine 1: 255–266. doi:10.2217/17460751.1.2.255
Web References
- w1 – Christopher ve Dana Reeve Vakfı araştırmalara destek vererek omurilik hasarlı ve felçlilerin hayatlarının kalitesini iyileştirmeye kendini adamıştır.
-
Websitesi, hayatları hakkında konuşan felçli insanların videolarını içermektedir.
-
- w2 – 2012’de, John Gurdon ve Shinya Yamanaka, yetişkin hücrelerin yeniden programlanarak pluripotent olabileceğini keşfettiklerinden Nobel Fizyoloji ve Tıp ödülüyle ödüllendirildi.
-
Embriyonik ve indüklenmiş pluripotent kök hücreler hakkında Nature Education’s Scitable web sayfasından daha çok bilgi edinebilirsiniz.
-
Konunun öncü bilim adamları Eurostemcell web sayfasındaki bir online videoda, ‘Kök hücreler – gelecek: iPS hücrelerine giriş’, indüklenmiş pluripotent kök hücreleri anlatmaktadır.
-
- w3 – Geron klinik deneme hakkında New York Times‘ı okuyun.
- w4 – Balgrist Üniversite Hastanesi’ndeki klinik denemeler hakkında Klinik Denemeler websitesinden daha fazla okuyun.
- w5 – Eurostemcell’in web sayfasından Omurilik yaralanmaları: kök hücreler nasıl yardım edebilir? bilgi notunu indirin.
-
Eurostemcell’in kök hücre alet takımı indirilebilirdir, Creative Commons lisanslı kaynaklıdır ve eğitimsel aktiviteler için uygundur. Örneğin:
-
Embriyonik kök hücre araştırması: etik bir ikilem bilgi notu.
-
Hope Beyond Hype kök hücre tedavisi hakkında, keşiften tedaviye, etkileşimli çizgi roman şeklinde bir hikayedir.
-
Hazır veya değil? omurilik yaralanmaları hakkında sınıf kullanımı için dizayn edilmiş bir rol oyunudur.
-
Resources
- Okullar için Eurostemcell’in DVDlerinin birinin incelenmesi için bkz.:
-
Gebhardt P (2006) Review of A Stem Cell Story. Science in School 3: 88.
-
- Omurilik hasarı: kök hücre araştırmasında gelişim ve vaat omurilik hasarı hastası(eski futbolcu) avukat Roman Reed’i gösteren kısa bir videodur.
- TUlusal Nörolojik Bozukluklar ve Felç Enstitüsü’nün web sayfası omurilik hasarı bilgilerini detaylandırıyor.
- Omurilik Hasarı Felcinin Tedavileri için Uluslararası Kampanya, omurilik hasarları hakkında başka bilgilere ve istatistiklere sahiptir.
Review
Bu makale, insanlardaki omurilik hasarının çeşitli sonuçlarına odaklanmakta, bilimin geldiği son noktayı sunmakta ve kök hücrelere dayanarak gelecekteki potansiyel tedavileri göz önünde bulundurmaktadır.
Christopher Reeve Superman‘in durumu ile genç öğrenciler (yaşları 11-14) sinir sistemini (örn., yay refleksi) çalışmaya motive edilebilir. Ancak, metnin basitleştirilmesi gerekli olacaktır.
Sunulan detay seviyesi dolayısıyla makale özellikle ortaokul üstü öğrenciler (15-18 yaşları) içindir. Sinir sisteminin anatomi ve fizyolojisi, bağışıklık sisteminin fizyolojisi, hücre çoğalması ve farklılaşmasını içeren konularla bağlantılıdır. Önerilen kaynakların listesi makaleyi iyi bir şekilde tamamlamaktadır.
Makale, fizik ve kimyayla ilişkili disiplinlerarası araştırma projeleri için de başlangıç noktası olarak kullanılabilir. Bu gibi projeler için konular: Hasarlı hücreler serbest radikalleri neden salıyorlar ve bu radikaller neden hücrelere zararlıdır? Serbest radikallerle hangi moleküller öncelikli olarak reaksiyona giriyor? Niçin kan ve omurilik hücreleri arasındaki besin ve moleküllerin değişimiyle ödem etkisi azalır? Hangi tip moleküller omurilik tamirini teşvik edebilir?
Bu makale kavrama ve genişletilmiş etkinliklerin temeli olarak kullanılabilir:
- Özel nöral hücreler yaratmaktaki potansiyellerini göz önüne alarak, pluripotent kök hücrelerin nöral olmayan yetişkin kök hücrelerden ve nöral kök hücrelerden (yetişkinlerden veya embriyolardan) farkını belirle. Bunu gen düzenlenmesi mekanizmasıyla ilişkilendir.
- “Pluripotent kök hücreler embriyolardan (embriyonik kök hücreler) elde edilebilir veya deri hücreleri gibi özelleşmiş hücrelerden laboratuvarda (indüklenmiş pluripotent kök hücreler) oluşturulabilir.” “Pluripotent kök hücrelerin hayvanlara transplantasyonu tümör oluşması gibi çeşitli ciddi yan etkilere yol açar.” Bu cümleleri hücre farklılaşması ve genetik düzenleme süreçleriyle ilişkilendir.
- “Kök hücrelerin transplantasyonu hassas bir cerrahi prosedür gerektirdiği ve embriyonik ve nöral kök hücre durumlarında immün sistemin yeni tanıtılan hücreleri reddedebileceği risklere sahiptir.” Bu risk için sorumlu biyolojik mekanizmayı açıklayın.
Betina da Silva Lopes, Portekiz





