El legado oscuro de Van Gogh Understand article
Traducido por Jorge J. Pérez-Maceira. Los brillantes amarillos de la pintura de Van Gogh se están convirtiendo en un desagradable color marrón. Andrew Brown revela cómo gracias a sofisticadas técnicas de rayos X cortesía del Instalación Europea de Radiación Sincrotrónica (ESRF o…
Junto con sus amplias pinceladas, Vicent van Gogh (1853-1890) elegía vibrantes y a menudo poco realistas colores para transmitir su estado de ánimo o la emoción lo que hizo que fueran el centro de su estilo único, con gran influencia en el desarrollo de la pintura moderna. La nueva generación de pigmentos del siglo 19 hizo posible que Van Gogh creara, por ejemplo, los ricos amarillos utilizados en su célebre Girasoles. Estos colores llamativos, que utiliza en muchas de sus obras, contienen uno de esos nuevos pigmentos denominado Amarillo de Cromo. Desafortunadamente, más de 100 años después de que Van Gogh abandonara su pincel, el amarillo de cromo ha oscurecido visiblemente en algunos casos a un menos sorprendente color marrón, un fenómeno que recientemente captó el interés de un grupo de científicos.

Imagen cortesía de the Van Gogh Museum, Amsterdam

Imagen cortesía de the Van Gogh Museum, Amsterdam

Imagen cortesía de Acacia217; origen de la imagen: Wikimedia Commons

Imagen cortesía de the Van Gogh Museum, Amsterdam
Un equipo internacional dirigido por Koen Janssens de la Universidad de Amberes, Bélgica, cree que los cambios químicos del amarillo de cromo (PbCrO4 · xPbO), son debidos a la exposición a los rayos ultravioleta (UV), responsables de su transformación de color (Monico et al., 2011). El oscurecimiento de los pigmentos por la luz solar se conoce desde su invención. Los estudios realizados en la década de 1950 demostraron que es causada por la reducción del cromo de Cr(VI) a Cr(III) (ver Figura 1, a continuación). Hasta ahora, sin embargo, el mecanismo exacto se desconocía, y los productos de degradación estaban sin caracterizar.
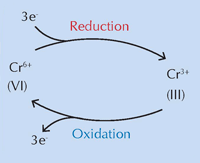
Imagen cortesía de Nicola Graf
Tubos de pintura históricos
Para hacer frente a estas incógnitas, el equipo de Janssens comenzó recogiendo muestras de los tubos de pintura pertenecientes a un contemporáneo de van Gogh, el pintor flamenco Rik Wouters (1882-1913). Algunos tubos de pintura contenían pintura amarillo de cromo sin mezclar, mientras que otros contenían pintura de un tono más claro de amarillo, formado por la mezcla de amarillo de cromo con una sustancia blanca. Los investigadores envejecieron artificialmente las muestras con luz UV, con la esperanza de observar un cambio de color después de varios meses. Para su sorpresa, en sólo tres semanas, una fina capa superficial de la pintura de color amarillo más claro había oscurecido significativamente a un marrón chocolate. Las muestras sin mezclar han cambiado comparativamente poco o nada. “Nos sorprendió”, dice Janssens.

Una vez identificadas las muestras más probabilidades de ser sometidas a la reacción química fatal, el equipo las sometió a análisis sofisticados basados en rayos X. Gran parte del trabajo se llevó a cabo en el Instalación Europea de Radiación Sincrotrónica (ESRF o European Synchrotron Radiation Facility en inglés)w1 en Grenoble, Francia, donde dos técnicas, la XRF y XANES, fueron utilizadas para detectar, con extrema sensibilidad, la distribución espacial y el estado de oxidación de los elementos seleccionados en las muestras de pintura (ver cuadro).
Los análisis revelaron que el oscurecimiento de la fina capa superficial del pigmento se relacionaría con una reducción del cromo en el amarillo de cromo de Cr(VI) a Cr(III), lo que concuerda con lo observado para las pinturas industriales basadas en cromato de plomo. Además, el producto de degradación que contiene Cr(III) fue identificado por primera vez como Cr2O3 · 2H2O, más conocido como el pigmento verde viridiana. Pero, ¿Cómo puede la presencia de un pigmento verde explicar la coloración marrón observada en los experimentos de los investigadores? Los científicos sospechan que el cromo reducido en verde Viridiana se forma durante la oxidación del componente del aceite de la pintura. Esta forma oxidada del aceite, junto con la mezcla de verde y ningún pigmento amarillo remanente, puede ser la raíz de la coloración marrón.
Utilizando las técnicas de rayos X, los investigadores también pudieron demostrar que la mezcla de pintura, de color más claro contiene compuestos de azufre. Llegaron a la conclusión de que estos compuestos estaban involucrados de alguna manera en la reducción del cromo, explicando así por qué había comparativamente poco oscurecimiento en las muestras de pintura sin mezclar.
Un brillante haz de rayos X sobre van Gogh

Haga clic sobre la imagen
para ampliarla
Imagen cortesía de the Van
Gogh Museum, Amsterdam
Después de haber descubierto la química de la reacción en las muestras de pintura aisladas, los científicos trataron de responder a si el oscurecimiento de la capa superficial de pintura amarilla en las muestras tomadas de dos de los cuadros de Van Gogh, Vista del Arlés con Lirios (1888) y Ribera del Sena (1887), podría atribuirse al mismo fenómeno.
La espectroscopia XRF se utilizó para mapear la química de la región que abarca la interfase entre la capa superficial oscura y la capa subyacente de pintura sin amarillo alterado. Los espectros XANES se recogieron en puntos específicos dentro de estas regiones. Los hallazgos reflejan los del experimento anterior: la forma reducida del cromo, Cr(III), fue encontrada en la capa superficial oscura, lo que sugiere que su presencia en ellas es la responsable de la coloración marrón. Además, Cr(III) no se distribuyó uniformemente, encontrándose lugares donde también aparecían compuestos que contenían sulfato y bario.
Químicamente, estas regiones se parecían a las muestras de pintura amarilla más clara del experimento anterior, más apoyo para las conclusiones de los investigadores de que los compuestos de azufre estarían envueltos en la reducción de cromo (ver ecuación a continuación). Debido a su color blanco, van Gogh mezclo los polvos que contienen dichos compuestos con el amarillo de cromo para crear los tonos más claros que fueron vitales en la creación de la brillante iluminación de las escenas característico de un determinado período de su vida.
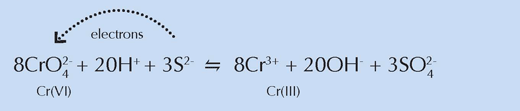
Falta una importante pregunta: ¿Qué se supone que el detonante de la reacción, la luz ultravioleta, realmente hace? En pocas palabras, suministra a los reactivos la energía necesaria para superar la barrera de la energía de activación, permitiendo que la reacción tenga lugar (ver Figura 6, a continuación).
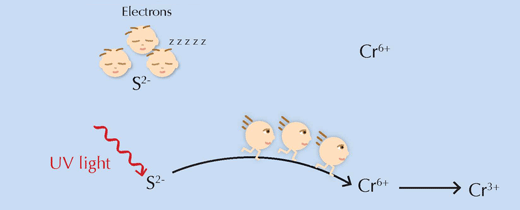
Imagen cortesía de Nicola Graf
¿Qué puede hacerse?
El equipo de Janssens ha puesto de manifiesto la química que subyace en el oscurecimiento de las pinturas de Van Gogh. Pero, ¿Podemos usar este conocimiento para rescatar la obra del artista? Ella Hendriks del Museo Van Goghw3 en Ámsterdam, Países Bajos, tiene sus dudas: “La luz ultravioleta…ya se filtra en los museos modernos. Mostramos las pinturas en un ambiente controlado para mantenerlas en las mejores condiciones posibles”. Parte de lo que constituye un ambiente controlado es el mantenimiento de una baja temperatura en el museo. Como regla general, un incremento de 10 ºC aumenta la velocidad de reacción por un factor de entre 2-4, y la reducción del cromo no es una excepción.
Así que si los niveles de UV y temperatura están ya controlados, ¿Qué más se puede hacer con las cuadros de Van Gogh? Hay una alternativa más radical: en lugar de retrasar el proceso de degradación, tratar de revertirlo por completo. “Nuestros experimentos siguientes ya están en ese camino”, dice Janssens. “Obviamente, queremos entender que condiciones favorecen la reducción del cromo, y si hay alguna esperanza de revertir los pigmentos a su estado original en las pinturas.”w4
Aunque volver atrás las manecillas del reloj de esta manera sería la mejor solución, Janssens admite que la posibilidad de revertir el pigmento alterado a su color original es en la actualidad bastante improbable. Sin embargo, el trabajo de los científicos nos ofrece la seguridad de que estamos haciendo todo lo posible para preservar las pinturas de van Gogh, y esperamos que las futuras generaciones puedan apreciar lo que este gran artista logró.
Estudiando arte con un sincrotrón
La determinación química de valiosas obras de arte puede ser problemático. Sólo es posible tomar algunas muestras muy pequeñas para el análisis, y éstos a menudo consisten en una mezcla diversa de complejos compuestos en los estados heterogéneos de material. Para superar estos retos, los científicos utilizan técnicas basadas en rayos X. Cuanto más potentes y precisos son, mejor será la calidad del análisis. El más potente de los rayos X disponibles son los producidos por una fuente sincrotrónw2 (ver Figura 2, a continuación). En este estudio, dos técnicas espectroscópicas en el ESRF fueron usadas en las muestras de pintura: XRF y XANES.
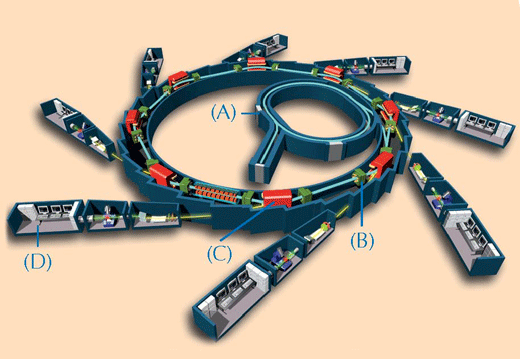
Imagen cortesía de EPSIM 3D / JF Santarelli, Synchrotron Soleil; origen de la imagen: Wikimedia Commons
XANES
La espectroscopia XANES se basa en la física de la absorción de rayos X. los átomos de un elemento en particular absorben los rayos X de una forma característica. Al observar el espectro de absorción de rayos X, que es el patrón de absorción de rayos X de una muestra particular (eje Y) contra el rango de energía de los rayos X (eje X), por lo que es posible identificar elementos constituyentes de la muestra. El espectro de absorción de alta resolución de rayos X se recogen normalmente en las regiones específicas de energía (denominadas XANES) que están cerca de un borde de absorción de un elemento de interés (ver Figuras 3, a continuación, y 4). Tales espectros detallados pueden mostrar el estado de oxidación del elemento de interés. Esta información ha sido de gran interés para los investigadores.
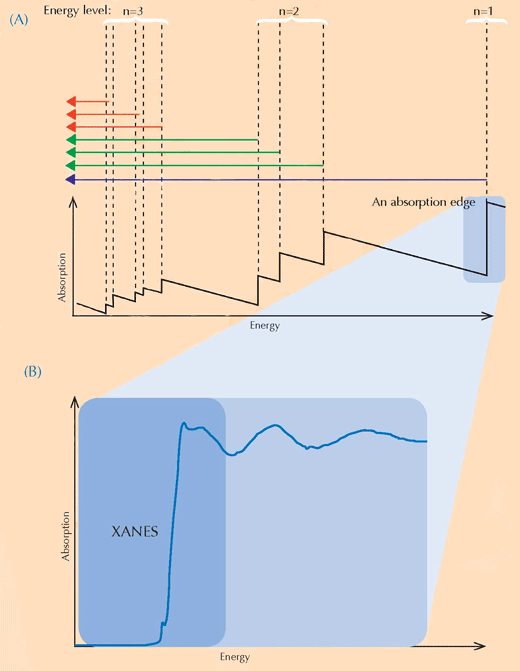
Imagen cortesía de Atenderhold; origen de la imagen: Wikimedia Commons (B) Un borde de absorción en detalle. Cuando nos centramos en un borde de absorción aparentemente fácil, encontramos que está decorado con una serie de pequeñas impresiones relativas a absorciones correspondientemente menores. La región en el borde principal (sombreada en azul) del borde de absorción se conoce como absorción de rayos X cerca del borde de la estructura (X-ray Absorption Near-Edge Structure o XANES, el cuadro azul) y corresponde a las transiciones de los electrones a niveles de energía desocupados cercanos a los que se fueron. La región XANES fue utilizada por los científicos que analizan los cuadros de Van Gogh, ya que proporciona información sobre el estado de oxidación de los átomos en una muestra: los átomos que tienen diferentes estados de oxidación contienen diferente número de electrones (ver Figure 1 anterior). Esto altera los valores de sus niveles de energía y por lo tanto su espectro XANES
Imagen cortesía de M Blank: origen de la imagen; Wikimedia Commons
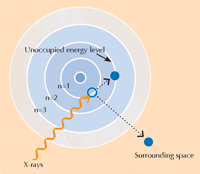
Imagen cortesía de Nicola Graf
XRF
Cuando absorben los rayos X, los átomos entran en un estado excitado inestable. Cuando vuelven al estado más estable, emiten rayos X secundarios en un proceso llamado fluorescencia de rayos X (ver Figura 5). El patrón de fluorescencia de rayos X (XRF) producido por una muestra en particular, denominado espectro XRF, puede ser usado para determinar la distribución de elementos en un área determinada. En contrate, XANES que sólo puede realizarse en un punto aislado de la muestra. Al combinar la información obtenida con XRF y XANES, los autores fueron capaces de formar una imagen detallada de la composición química de las muestras de la pintura.
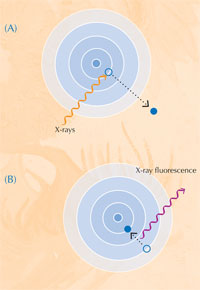
Imagen cortesía de Nicola Graf
Ciencia en el arte
¿Qué es lo que tú y tus estudiantes pensáis? ¿Debe la ciencia utilizarse para detener la degradación de importantes obras de arte, o incluso devolverlas a su estado original? o ¿deberían aceptarse los estragos del tiempo e incluso valorarse como evidencia histórica?
References
- Monico L et al. (2011) Degradation process of lead chromate in paintings by Vincent van Gogh studied by means of synchrotron X-ray spectromicroscopy and related methods. 2. Original paint layer samples. Analytical Chemistry 83: 1224-1231. doi: 10.1021/ac1025122
Web References
- w1 – La Instalación Europea de Radiación Sincrotrónica (ESRF o European Synchrotron Radiation Facility en inglés) es un instituto de investigación internacional para la ciencia de vanguardia con fotones. El ESRF es un miembro de EUROforum, el editor de Science in School. Para obtener más información, visite: www.esrf.eu
- w2 – Para más detalles de cómo la radiación del sincrotrón se utiliza en investigación, véase:
- Capellas M, Cornuéjols D (2006) Shipwreck: science to the rescue! Science in School 1: 26-29.
- Capellas M (2007) Recuperando Pompeya. Science in School 6: 14-19.
- w3 – Para más información sobre Vincent van Gogh y su arte, visite el excelente sitio web del Museo Van Gogh: www.vangoghmuseum.nl
- Una sección del sitio web del museo también contiene recursos para la enseñanza primaria y secundaria: www.vangoghmuseum.nl/vgm/index.jsp?page=110&lang=en
- w4 – Para escuchar una entrevista con Koen Janssens hablando de su investigación en las pinturas de van Gogh, grabación de la BBC Radio 4, consulte: www.bbc.co.uk/programmes/b00yjs49
- w5 – CLEAPSS es un servicio de asesoramiento del Reino Unido para apoyar a la ciencia y la tecnología en la enseñanza, en los temas de salud y seguridad, evaluación de riesgos, fuentes y uso de químicos, y organismos vivos y equipamiento. Para más información, consulte: www.cleapss.org.uk
- Para consejos de seguridad sobre el uso del plomo, cromo y sus compuestos, véanse las hojas de seguridad de los estudiantes que se pueden descargar gratis aquí: http://www.cleapss.org.uk/free-publications/general-publications
Resources
- Imágenes y una animación de la investigación de muestras históricas de pintura se encuentran en: www.vangogh.ua.ac.be
- Para aprender más sobre la ciencia de la preservación del arte, véase:
- Leigh V (2009) La ciencia de preservar el arte. Science in School 12: 70-75.
Institutions
Review
En este artículo se ven muy bien los vínculos de la ciencia con el arte y los estudios de conservación. Las sofisticadas técnicas usadas por los científicos revelan cambios químicos en los pigmentos, que se producen muchas décadas después de que los cuadros de Van Gogh fueran terminados.
Este artículo es una forma útil de mostrar a los estudiantes que siempre hay una explicación científica de por qué los objetos cambian con el tiempo. Lo mejor sería utilizarlo como material didáctica en las clases de química y para estudiantes de entre 16-18 años. El artículo también se podría utilizar para enseñar en temas de química, como oxidación y reducción.
Para desarrollar la comprensión de los estudiantes de la química detrás de la investigación, se podrían formular las siguientes preguntas:
- El trabajo de los científicos descrito en este artículo muestra que los iones de sulfuro pueden ser la especie química responsable de la reducción del cromo. Escribe las ecuaciones separadas para la reducción del cromato de plomo (PbCrO4) por compuestos que contienen iones sulfuro como H2S y PbS. Sugerencia: Los compuestos Cr(VI) son agentes oxidantes.
- Los científicos sugieren que los compuestos que contienen sulfato en la pintura usada por van Gogh podrían ser una fuente de iones sulfuro. Trata de pensar en otras maneras en que las obras podrían estar expuestos a los iones sulfuro.
- Las joyas con plata se oscurecen con el tiempo en contacto con el aire. Escribe la ecuación para la reacción responsable de esto. Ten en cuenta que esto no es una reacción de desplazamiento simple.
Para demostrar que oscurece el cromato de plomo cuando se expone a los iones sulfuro, se puede realizar el siguiente experimento en clase:
- Síntesis de cromato de plomo en un vaso de precipitados por la adición de cualquier sal soluble en agua de plomo, como el acetato de plomo (II), Pb(CH3COO)2, o el nitrato de plomo, Pb(NO3)2, en un volumen igual que la solución de cromato potásico, K2CrO4. Las soluciones diluidas (~ 0.03 M) será suficiente.
- Un precipitado Amarillo de cromato de plomo se forma al instante. Filtrar el líquido residual con un embudo y un filtro de papel. En una campana de extracción, suavemente secar el precipitado con un secador de pelo, asegurándose de que no se seque por completo.
- Preparar una disolución acuosa diluida de ácido sulfhídrico (H2S) mediante la disolución de 50 mg de sulfuro de sodio (Na2S) en 90 mL de agua. Añadir a la solución resultante 10 mL de ácido clorhídrico (HCl, 0,1 M). Revolver la mezcla.
- Llenar un globo con aire y conectarlo a una pequeña botella Drechsel de vidrio que contenga unos mililitros de la solución de sulfuro de hidrógeno diluida (ver imagen a continuación). Apuntar el flujo resultante de aire con gas de sulfuro de hidrógeno hacia la superficie del precipitado de cromato de plomo.
- El precipitado al instante se vuelve marrón. Hemos simulado y acelerado el proceso de oscurecimiento observado en los cuadros de van Gogh en varios órdenes de magnitud.
Nota de seguridad: Todas las sales solubles de plomo son tóxicas, y el cromato soluble es tóxico (por encima de 0.003 M) y se sospecha que son cancerígenos. El cromato de potasio puede causar sensibilización y/o úlceras después del contacto con la piel. Existen pruebas limitadas de que el cromato de plomo es cancerígeno. También puede causar daño a los niños no natos, por lo que no debe ser utilizado si la profesora o cualquier otras estudiante están, o pueden estar embarazadas. El sulfuro de hidrógeno es un gas tóxico con u olor muy desagradable.
Se debe realizar el experimento anterior en una campana de humas y con gafas de seguridad y guantes. Usar todos los productos químicos de acuerdo a sus normas de seguridad locales. Véase también la hoja de seguridad escolar general en Science in School. Tal vez le resulta útil consultar las hojas de seguridad para estudiantes de CLEAPSS sobre cromo y plomow5.
Vladimir Petruševski, Antigua República Yugoslava de Macedonia






