Recuperando Pompeya Understand article
Traducido por Maria Chueca. ¿Encuentran tus estudiantes difícil relacionar la aplicación de la ciencia en otras materias? Montserrat Capellas, de la Instalación Europea de Radiación Sincrotrónica (ESRF o European Synchrotron Radiation Facility en inglés) de Grenoble, Francia, explica…

(1827-1833) por Karl Pavlovich
Briullov
Imagen de dominio público;
Fuente: Wikimedia Commons
Hace 2000 años los artistas de la antigua ciudad de Pompeya, Italia, la pintaron en rojo usando un pigmento carmesí brillante que dominaba la mayoría de sus murales. El 24 de agosto del año 79, el volcán Vesuvio entró en erupción y enterró en piedra pómez y cenizas los pueblos y ciudades cercanos. Paradójicamente, la erupción en lugar de destruir Pompeya, conservó la ciudad y los cuerpos de sus habitantes dejándolos bajo tierra. Incluída en la Lista del Patrimonio Mundial por la UNESCO en 1997, la antigua ciudad de Pompeya es ahora el lugar arqueológico más visitado de Europa.
En la cercana ciudad de Torre del Greco unos trabajos de excavación revelaron hace 20 años las ruinas de Villa Sora, una casa que hasta entonces había permanecido enterrada. Desde el descubrimiento de estos restos, el característico color rojo de los frescos se ha vuelto negro en muchos puntos, en un rápido proceso de degradación que todavía no está científicamente bien entendido. La fuente del color rojo en Torre del Greco y en Pompeya es sulfuro de mercurio (HgS), comúnmente llamado cinabrio. Se trata de un pigmento rojo intenso usado comúnmente para cubrir el fondo de las pinturas, confiriéndoles así un fondo rojo uniforme. A pesar de todo, en ciertas circunstancias, se puede volver inestable, proporcionando apagadas sombras negro-grises.

Hace muchos años que los científicos se preguntan el porqué del ennegrecimiento de los muros rojos de Pompeya. Ya en el siglo I a. C., Vitruvio en su tratado De Architectura mencionaba el problema, y dio la receta de una especie de barniz protector basado en cera púnica (un jabón ceroso hecho de cera de abejas y cal sodada): “Pero si otro mas experto quisiere que el bermellón retenga su color en el enlucido, quando la pared estuviere ya pintada y enxuta se le dará con brocha un baño de cera Púnica derretida al fuego con un poco de aceyte. Luego poniendo fuego en un braserillo de hierro, se irá llevando con destreza cerca de la cera, obligandola á sudar é igualarse. Finalmente se estregará con una candela, y con pedazos de trapo limpio, como se hace con las estatuas de mármol desnudas. De este modo la mano de cera Púnica no dexará que los reflejos de la luna, ni los rayos del sol chupen el color de las paredes pintadas.”
Aún a pesar de la cera púnica, las antiguas paredes de Pompeya han perdido sus colores en los años recientes. La explicación más común es que la exposición al sol transforma el cinabrio en otra fase (en que los mismos átomos, mercurio y azufre, se distribuyen de forma diferente), metacinabrio, que es negro. Sin embargo las causas y los mecanismos han seguido siendo un misterio hasta ahora y los conservadores han seguido perdiendo la carrera contra el tiempo para prevenir la degradación.
Nuevos resultados

Pompeya, por un artista pompeyo
alrededor del 40 a.c.
Imagen de dominio público; Fuente:
Wikimedia Commons
Con el fin de controlar los procesos químicos que tienen lugar en los muros, un equipo de investigadores franco-italiano ha estudiado cuatro muestras de pinturas murales de Villa Sora usando laInstalación Europea de Radiación Sincrotrónica (ESRF) de Grenoble, Francia. Se tomaron muestras tanto de zonas alteradas como de zonas no alteradas y se sometieron a microananálisis para tratar de entender las causas de este ennegrecimiento espectacular.
El equipo identificó los elementos presentes tanto en las muestras bien conservadas (rojas) como en las alteradas (gris-negras). Además de azufre y mercurio, originados por el pigmento y de calcio, presente en la calcita del mortero, se detectaron bajos niveles de otros elementos como aluminio, sílice y potasio. Sin embargo, el elemento más interesante que se encontró fue el cloro, el cual puede proporcionar respuestas al misterioso proceso de ennegrecimiento.
Gracias al mapeo de señales de micro fluorescencia de rayos X (ver cuadro) sobre superficies rojas, grises o negras, los científicos pudieron correlacionar la distribución de elementos con la apariencia visible de las pinturas. Esta es una técnica que se usa frecuentemente en pinturas, aunque empleando microscopía electrónica en lugar del más sensible análisis con luz sincrotrón. El mapeado de elementos con luz sincrotrón de una de las muestras mostró como la distribución de cloro encajaba perfectamente con un área gris degradada.
Se encontró cloro asociado con sodio y mercurio, demostrando que el cloro había reaccionado con el pigmento y que la sal común (NaCl) estaba involucrada en el proceso de degradación.
Es conocido que el cloro provoca el oscurecimiento del cinabrio en presencia de luz. Los científicos pensaron que el cloro de las pinturas podría estar originado a partir de dos fuentes de sal . Al estar Pompeya y Torre del Greco junto al mar, se pensó que las pinturas podían absorber sal del aire. Irónicamente, la segunda fuente de sal podría ser la cera púnica “protectora”, la cual, según Plinio el Viejo se hacía usando agua de mar.
¿Qué significa todo esto?
De momento, los descubrimientos del ESRF han servido para confirmar la explicación tradicional de que el cinabrio rojo se transforma en metacinabrio negro. Sin embargo los análisis de otra parte más oscura de la pintura revelaron una alta acumulación de azufre en áreas donde el cloro no estaba presente. Se investigó la especiación, o ambiente químico, del azufre para descubrir cuáles son los átomos que lo rodean. Esto es importante ya que aunque cinabrio y metacinabrio tengan la misma composición (Hg y S) se pueden distinguir por sus diferentes distribuciones atómicas. Este análisis desveló la ausencia de metacinabrio, refutando así la hipótesis de que el cinabrio había sufrido una transformación de fase en metacinabrio.

Reimpreso con permiso de Cotte et al., 2006. Copyright 2007 American Chemical Society

Reimpreso con el permiso de Cotte et al., 2006. Copyright 2007 American Chemical Society
Para sorpresa de los científicos incluso apareció otro compuesto: sulfato de calcio, también conocido como yeso. Este constituía el compuesto de azufre encontrado en las áreas negras donde no había cloro. Así que, en lugar de una simple transición de fase el azufre había sufrido un oxidación real, transformándose desde azufre en estado reducido (S(-II)) hasta azufre en estado oxidado (S(+IV)). Lo más probable es que el yeso (CaSO4.2H2O) haya resultado de la reacción entre el dióxido de azufre (SO2) en el aire con la calcita (CaCO3) en el mortero:
SO2(g) + CaCO3(s) + 2H20(g) + ½ O2 → CaSO4.2H20(s) + CO2
Esta explicación está avalada por el hecho de que el cloro puede catalizar la reacción de rotura
HgS → Hg + S
en la cual el cinabrio se disocia en mercurio y azufre en presencia de luz, proporcionando una fuente de azufre para posteriores reacciones con el oxígeno del aire y la subsiguiente formación de SO2. Así pues, aunque el segundo trozo más oscuro contenía azufre sin cloro, el cloro de otras áreas (como el primer trozo gris) fue suficiente para generar dióxido de azufre que degradó el pigmento en otras áreas.
De esta manera los análisis con luz sincrotron arrojan dudas sobre la teoría tradicional de que el pigmento rojo cinabrio se degrada directamente en metacinabrio en presencia de luz, y apoya la teoría más reciente de que el cinabrio se disocia en presencia de cloro para producir azufre, el cual entonces (en forma de dióxido de azufre) reacciona con la calcita del mortero para formar sulfato de calcio. Esto explica por qué las áreas que no fueron pintadas con pigmento rojo cinabrio no se decoloraron.
Estudios de sección transversal
Los científicos fueron más allá e investigaron la sección transversal de una de las muestras para trazar la profundidad de la alteración en la pintura. Se impregnó una muestra de resina y se pulió perpendicularmente a la capa de pintura. De esta manera se pudo acceder a todas las capas de la pintura, desde el mortero hasta la superficie. Los científicos descubrieron que la capa degradada, conteniendo especies oxidadas de azufre y sulfatos, sólo tenía un espesor de 5 µ y que por debajo de la superficie el cinabrio había permanecido intacto.
Estas pinturas antiguas eran frescos en que la pintura era aplicada sobre la escayola húmeda permitiendo al pigmento hundirse en ella, dejando una capa de pigmento de unas 100 µ. De esta manera los estudios de sección transversal proporcionan dos tipos de información. Primero, fue posible distinguir entre los elementos presentes en la pintura original (calcio, mercurio y azufre) y aquellos que procedían del ambiente (potasio, sílice, aluminio, cloro y yeso). Esto era importante ya que como el yeso se detectó solamente en las capas superficiales quedó claro que no había sido usado en el mortero de esas pinturas. Segundo, las secciones transversales demostraron que la degradación del color estaba limitada a las capas muy superficiales, ofreciendo la esperanza de que las pinturas se puedan restaurar para volver a su completa colorida gloria.
“La investigación llevada a cabo en el ESRF es de extraordinaria importancia, no sólo para la conservación de las pinturas murales de Villa Sora sino para la preservación de pinturas murales romanas descubiertas en los lugares arqueológicos romanos más importantes (como Pompeya y Herculano)”, explica Corrado Gratziu, miembro del equipo de investigación y profesor emérito en geología en la universidad de Pisa, Italia, especializado en petrología y rocas sedimentarias.
Investigación futura
A pesar de haber refutado la explicación clásica sobre el ennegrecimiento del cinabrio, la investigación acerca del antiguo pigmento rojo está lejos de haber finalizado. Las complejas rutas que implican la reacción del cloro y del dióxido de azufre han planteado nuevas preguntas. “La distribución química de las muestras no es uniforme, lo cual implica que las condiciones atmosféricas probablemente influyen en los cambios de colores,” explica Marine Cotte, una de las investigadoras. “Es seguro que el sol influye en el proceso, pero es probable que la lluvia también lo haga,” añade. “La luz del sol acelera algunas reacciones, mientras que la lluvia puede lavar las pinturas y disolver los compuestos más solubles.” La contaminación atmosférica o actividades bacterianas también pueden contribuir a mecanismos de captura de azufre.
El siguiente paso para el equipo es el de examinar más muestras, no sólo de los frescos de los sitios arqueológicos sino también de lugares ya excavados y expuestos en museos. “De esta manera tendremos más datos y podremos comparar los resultados entre pinturas expuestas a diferentes condiciones atmosféricas y así poder establecer mejor las causas de su degradación, “ explica Marine.
Rayos X como herramienta para el estudio de Pompeya
Los experimentos llevados a cabo en el ESRF necesitan un haz muy pequeño (desde 100 μm a menos de 1 μm) e intenso de rayos X para detectar bajas concentraciones de elementos y proporcionar información química detallada. Se realizaron en la línea de microscopía de rayos X (ID21) combinando las técnicas de mapeo de micro fluorescencia de rayos X y espectroscopia de microabsorción de rayos X.
Principio de la fluorescencia de rayos X
Una manera simple de entender el principio de la fluorescencia de rayos X es considerar que los átomos (los pequeños elementos que componen la materia) son como casas cuyos habitantes se llaman electrones. Estos ocupantes son bastante perezosos y no les gusta vivir en los pisos altos. Así que primero ocupan la planta baja, cuando está llena ocupan el primer piso y así sucesivamente. Como en la vida existen casas pequeñas (átomos pequeños con pocos electrones) y casas grandes (grandes átomos con muchos electrones).
El principio de la fluorescencia de rayos X es proyectar luz de rayos X sobre esos átomos. La luz se comportará como el ascensor de la casa que transfiere los electrones que viven en los pisos inferiores a pisos superiores; este proceso se denomina ‘absorción’ ya que la luz es absorbida por el átomo (el electrón es absorbido por el ascensor). A medida que los electrones se van yendo va quedando espacio libre en los niveles bajos. Como consecuencia los electrones que viven en lo alto están contentos de bajar. Durante esta transición van a expresar su alegría emitiendo algo de luz, o fluorescencia. En una casa pequeña la transición será pequeña, así que la expresión de alegría será poca, mientras que en una casa grande algunas de las transiciones (y las correspondientes expresiones de alegría) pueden ser grandes. Midiendo la señal de fluorescencia (la energía de fluorescencia, que es la distancia entre los pisos de partida y de llegada) se puede distinguir entre átomos pequeños y grandes, y más precisamente, identificar cada átomo de acuerdo a su característica expresión de alegría.
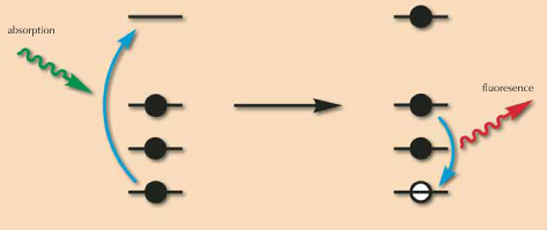
Imagen cortesía de Calvero; fuente de la imagen: Wikimedia Commons
Principio de la espectroscopía de rayos X
Este método se basa en la variación de la energía de rayos X en la luz necesaria para excitar los átomos, la cual corresponde a la altura del ascensor. Imaginemos que el átomo es iluminado con una energía baja, es decir, que la casa tiene un ascensor pequeño que va sólo desde la planta baja a la planta primera. Si ambos pisos están llenos ningún electrón de la planta baja tomará el ascensor ya que no hay espacio en el primer piso. Así pues, hay una condición que debe ser satisfecha antes de que un electrón tome el ascensor (o que un átomo absorba luz): el ascensor debe ser lo suficientemente alto como para permitir la transición desde pisos bajos vacíos a pisos vacíos superiores. Por ejemplo, un ascensor cuya altura sea mayor que la de la casa siempre conducirá a la absorción.
Hay un caso crítico en que la altura del ascensor es justo la suficiente para llevar los electrones al ático o desván. De hecho los electrones prefieren ir al desván antes que ser completamente expulsados de la casa. Así que la probabilidad de que un electrón tome el ascensor al desván es mayor que la probabilidad de que salga fuera. Midiendo la absorbancia medimos la probabilidad de que un electrón tome el ascensor. Se mide la absorbancia para cada altura de ascensor (energía de rayos X). La razón por la que los científicos están interesados en los electrones viajando al desván (siendo excitados al más alto nivel sin abandonar el átomo) es que la altura del desván nos habla sobre el entorno químico del átomo.
En otras palabras, consideremos una casa aislada. Podemos identificar esta casa usando fluorescencia. Ahora supongamos que esa casa está rodeada por otras casas (átomos). Se crearán algunas conexiones entre ellas, como pasarelas, en lo alto de las casas. Para acomodar de una forma segura la pasarela, la casa será ligeramente reformada cambiando un poco el nivel del desván en cada casa. El resultado es que la altura del desván depende de las casas circundantes (qué casas hay en el área, cómo están de lejos, etcétera). Midiendo la altura de la subida al desván podemos deducir la naturaleza del puente y, en consecuencia, el entorno químico de la casa (qué otros átomos la rodean, por ejemplo). Este proceso se llama especiación atómica.
Resources
- Cotte M, Susini J, Metrich N, Moscato A, Gratziu C, Bertagnini A, Pagano M (2006) Blackening of Pompeian cinnabar paintings: X-ray microspectroscopy analysis. Analytical Chemistry 78: 7484-7492. doi:10.1021/ac0612224
Institutions
Review
Este artículo es particularmente adecuado para profesores buscando nuevas ideas para mostrar a sus alumnos la importancia de la química y la física en diferentes campos (por ejemplo arqueología, conservación del patrimonio,…) y para los estudiantes de secundaria entusiastas del estudio de la edad antigua.
Recuperando Pompeya se puede usar en clase para tratar diferentes temas de ciencia (química: estructura atómica y molecular, redox, catálisis; física: estructura atómica, radiación electromagnética; ciencias de la tierra: meteorología, vulcanismo) como una actividad de calentamiento para despertar interés en las aplicaciones de la investigación científica. Se puede emplear como una lectura de fondo antes de la visita a un lugar arqueológico o a una instalación de investigación como una planta de radiación sincrotrónica. El artículo es adecuado para examinar el grado de comprensión de los estudiantes en torno al lenguaje y contenido científicos.
Por ejemplo se les puede hacer las siguientes preguntas:
- Los colores de los frescos estudiados eran:
- rojo, gris y verde
- rojo, marrón y gris
- rojo, gris y negro
- rojo, negro y marrón
- ¿Cuál de los siguientes compuestos no contiene azufre?
- cinabrio
- calcita
- metacinabrio
- yeso
- Escoge la expresión correcta acerca del estudio de los frescos mediante rayos X:
- la fluorescencia de rayos X mide absorción de luz y la espectroscopia de rayos X mide emisión
- la fluorescencia de rayos X mide emisión de luz y la espectroscopia de rayos X mide absorción
- tanto la fluorescencia de rayos X como la espectroscopia de rayos X miden emisión de luz
- tanto la fluorescencia de rayos X como la espectroscopia de rayos X miden absorción de luz
Los profesores pueden usar el artículo para discutir;
- el rol de la química y la física en diferentes campos (investigación, industria, conservación del patrimonio,…)
- la importancia del trabajo en equipo en investigación así como en otras situaciones
- el enfoque interdisciplinario de la arqueología moderna.
Finalmente este material puede ser muy útil para empezar un proyecto interdisciplinario conectando ciencia y humanidades, para ayudar a los estudiantes a entender la fundamental unidad de la cultura.
Giulia Realdon, Italia





