Brillante futuro para la microscopía de luz Understand article
Traducido por Antonio Gallego. ¿Quieres captar una enzima en acción? ¿O contemplar un cerebro embrionario creando sus propias conexiones? Russ Hodge, del Laboratorio Europeo de Biología Molecular de Heidelberg, Alemania, explica cómo los últimos desarrollos de la microscopía nos dejan ver…

Karsenti y Philipp
Niethammer con un
microscopio láser usado en
estudios de FRET
Entre las décadas de 1830 y 1870, una serie de mejoras en los microscopios basados en la luz condujeron a una nueva era en biología. Los anteriores microscopios adolecían de una resolución baja y de distorsionar la imagen por estar diseñados con una sola lente. La adición de una segunda lente resolvió parte de ese problema; y en 1830 el óptico inglés Joseph Jackson Lister descubrió que, separando las dos lentes una distancia adecuada, se eliminaba un tipo de distorsión denominado aberración esférica. El resultado fue un avance enorme en el poder de resolución; lo que permitió al fisiólogo alemán Theodor Schwann y a Matthias Jacob Schleiden, un botánico alemán, demostrar que los tejidos animales se componían de células.
En la era molecular, el interés de la mayoría de los biólogos se volvió hacia las proteínas y otras moléculas, demasiado pequeñas para ser observadas individualmente con el microspio de luz. En ciertas condiciones, con el microscopio electrónico sí pueden observarse moléculas o complejos moleculares muy grandes, pero como formas borrosas; los detalles más importantes siguen perdiéndose; además es imposible usar este método en células o tejidos vivos.
A mediados de los años 90 del siglo pasado, los científicos descubrieron que una molécula de las medusas denominada proteína fluorescente verde, que produce la fluorescencia del animal, podía insertarse en determinadas proteínas de otros organismos. Este procedimiento de marcado dio origen a unas nuevas moléculas, luminosas, cuya pista podía seguirse con el microscopio de luz mientras se desplazaban por las células y tejidos vivos. Ello proporcionó a los investigadores un medio muy sencillo de obtener información sobre cuándo y en qué parte del cuerpo se producen determinadas proteínas, a qué sitio de las células van y qué papel podrían jugar allí.
En la actualidad, los biólogos y los físicos han desarrollado métodos para obtener aún más información de las proteínas fluorescentes. Y un nuevo invento está permitiendo a los investigadores contemplar los procesos biológicos en el momento de producirse y en tres dimensiones. Científicos del Laboratorio Europeo de Biología Molecular (EMBL, en sus siglas inglesas) en Heidelberg, Alemania, están usando esas técnicas para obtener una nueva visión de algunas de las cuestiones más fascinantes de la biología.
FRET, FRAP y FLIM
El microscopio de Philippe Bastiaens presenta un aspecto entre mesa de cocina y show de luz láser. El instrumento está montado sobre una tabla de metal suficientemente larga para dar asiento a diez personas. Cuando el joven científico holandés da el interruptor, un rayo de luz azul, del espesor de una aguja, zigzaguea a toda velocidad entre espejos y lentes.
La tarea del láser es iluminar una muestra que contiene proteínas fluorescentes. Su luz excita los átomos de la molécula marcada, lo que acto seguido libera energía y hace visible la molécula. Eso ocurre una sola vez antes de consumirse la fluorescencia de la molécula. Cuando se excita un gran número de moléculas marcadas, idénticas, emiten un dibujo o patrón energético exclusivo de ellas. Los instrumentos de Philippe le permiten medir esa energía con extrema precisión, lo que puede proporcionarle importante información sobre la actividad de la proteína.
«Por ejemplo, el patrón de emisión cambia cuando la proteína se une a otra molécula», dice Philippe. «Así podemos detectar la velocidad con que las proteínas se unen y separan unas de otras. Muchas veces estas reacciones son tan rápidas que no podrías detectarlas de ninguna otra forma.» Esta técnica se denomina FLIM, siglas de fluorescence lifetime imaging microscopy : microscopía por visualización de la vida media de fluorescencia.
«Pueden detectarse también otras diferencias», dice Philippe. «Supón que la proteína que has marcado interactúa con otra molécula y origina un cambio químico en ella . Cuando esto sucede, detectas ya otro patrón de fluorescencia. Puedes construir perfiles de los distintos sucesos y decir cuál de ellos está teniendo lugar. Eso nos coloca en disposición de poder no sólo contemplar los contactos estrechos entre dos moléculas, sino también observar lo que se hacen una a la otra. Hasta ahora, si querías decir que una molécula estaba activando a otra, tenías que fiarte de evidencias mucho menos directas.»
Si iluminas una región de una muestra durante mucho tiempo (por ejemplo, una parte del núcleo de una célula u otro compartimento celular), se gasta toda la energía de fluorescencia y la región queda «blanqueada». Philippe y sus colegas han usado esta técnica de blanqueo para ver cómo las moléculas se mueven en la célula. Por ejemplo, las proteínas receptoras situadas en la membrana exterior ayudan a la célula a recibir señales de sus vecinas y del entorno. Los científicos estaban convencidos de que estas moléculas son llevadas al interior de la célula para su reciclado; pero era difícil de probar. Podían detectar proteínas receptoras en el interior de la célula, pero era difícil decir si esas moléculas se dirigían hacia la membrana o estaban de vuelta.
Philippe y sus colegas enfocaron el láser para blanquear una pequeña región del interior de la célula en la que se sabe que se concentran las proteínas receptoras. Luego bloquearon la producción de nuevas proteínas para detener el flujo de moléculas en movimiento hacia fuera. Cuando la zona blanqueada volvió a llenarse de proteínas fluorescentes, los científicos supieron que esas moléculas provenían de la membrana. Este método se denomina FRAP, siglas de fluorescence recovery after photobleaching : recuperación de la fluorescencia tras el fotoblanqueo.
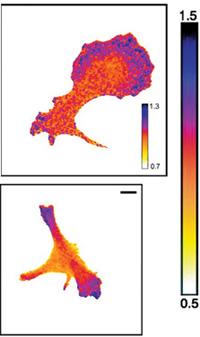
células es el resultado de la
interacción entre moléculas.
La célula de arriba está
quieta; la de abajo se desliza
por una superficie. Con la
técnica FRET, los científicos
pueden descubrir dónde se
unen determinadas proteínas,
explicando los cambios en la
estructura y comportamiento
de la célula. El azul muestra
las zonas donde muchas
proteínas estathmina se
están uniendo a moléculas de
tubulina. Eso está ocurriendo
en mucha menor proporción
en las zonas rojas
Durante la década última, los científicos han añadido el rojo, el amarillo y nuevos tonos de verde a la paleta de marcado por proteínas fluorescentes. Una de las más importantes nuevas técnicas de microscopía se refiere a observar el comportamiento de dos moléculas marcadas con distinto color. Philippe compara la FRET (fluorescence resonance energy transfer : transferencia de energía por resonancia en la fluorescencia) con el comportamiento de un cubo de arena.
«Si dos moléculas se aproximan tanto que interactúan físicamente entre ellas, detectas cambios en la fluorescencia que emiten», dice él. «Supón que haces un agujero en tu cubo. La arena se sale a una cierta velocidad. Si haces un segundo agujero, la velocidad a la que el cubo se vacía es distinta. Eso es un poco lo que pasa en la FRET. La segunda molécula fluorescente absorbe una parte de la energía emitida por la primera. Al detectar la variación en la emisión de fluorescencia, estás observando algo que los científicos han estado durante mucho tiempo intentando ver: las interacciones directas entre proteínas.»
El laboratorio de Philippe ha usado la técnica FRET para resolver algunas cuestiones cruciales. ¿Cuántas proteínas receptoras se necesitan para captar una señal? ¿Y qué sucede cuando lo hacen? Un estudio demostró que, para determinado receptor, bastaba con que se activaran un pequeño número de moléculas para desencadenar una rápida reacción en cadena de señales químicas dentro de la célula. (Sólo un pequeño punto de la superficie de la célula brilló con el código de fluorescencia que marcaba la activación de ese receptor.) El último trabajo del grupo muestra cómo las concentraciones de proteínas dentro de zonas concretas de la célula ayudan a crear estructuras llamadas husos, necesarias para la división celular. «Los científicos se habían convencido de que los diferentes subentornos químicos de la célula juegan algún papel en la estructuración de la misma», dice Philippe. «Pero ha sido muy difícil probarlo. Es una de las cosas que la FRET nos está ayudando a hacer, dibujándonos un cuadro de las concentraciones de las diferentes moléculas en el momento de interactuar unas con otras.»
SPIM
El grupo de microscopía de Ernst Stelzer, en el EMBL, ha inventado o ayudado a mejorar muchos tipos de microscopios. Su último instrumento, llamado microscopio de iluminación plana selectiva (SPIM: selective plane illumination microscope), permite a los científicos observar directamente el interior de los cuerpos de los organismos vivos, durante su desarrollo.
Ernst y sus colegas habían construido ya miscroscopios confocales, que usan un láser para escanear una muestra por capas a una velocidad impresionante; un ordenador ensambla luego las imágenes de cada una de esas capas apilándolas en una figura tridimensional. «Eso no lleva muy lejos», dice él, «porque es un método restringido sólo a la observación de tejidos sobre superficies lisas y no en el contexto real de las células y los organismos.» Así que comenzó a buscar un modo de escanear organismos enteros en sus entornos tridimensionales.
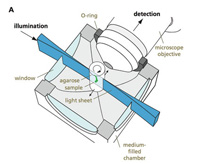
SPIM
La primera innovación fue poner la muestra -un embrión de pez- dentro de un tubo lleno de líquido, de forma que pudiera ser vista desde cualquier lado. Pero eso no salvaba uno de los problemas cruciales en el poder de resolución de los microscopios. La mayoría de los microscopios de luz iluminan la muestra a lo largo del eje óptico: o bien enviando luz desde la posición del detector (un ojo o la cámara) y mirando lo que se refleja o bien enviando luz que atraviese la muestra en dirección al detector.
El SPIM, por el contrario, hace pasar a través de la muestra una estrecha franja de luz procedente de un lateral. Sólo los objetos -por ejemplo, las proteínas fluorescentes- situados en esa franja son iluminados. El tubo se hace girar rápidamente, de forma que las imágenes se tomen desde distintos ángulos. Como en el caso del microscopio confocal, un ordenador ensambla esas franjas en imágenes de tres dimensiones; en este caso, en una película que pasa lentamente.
«La ventaja de introducir la luz lateralmente tiene mucho que ver con la resolución que consiguen los microscopios», dice Ernst. «Si envías luz a un objeto y lo miras en esa dirección, hay situaciones en que no existe un método sencillo para juzgar qué está delante y qué está detrás; o sea, cuánto de lejos está exactamente. Tú puedes obtener una buena resolución para la superficie bidimensional que está frente a tí; y puedes estudiar diferentes capas de una muestra moviendo el plano focal arriba y abajo; pero el hecho simple es que sigues iluminando objetos que están por encima y por debajo del plano focal; lo que distorsiona la imagen bidimensional. Las capas inevitablemente salen borrosas: en la tercera dimensión quedan movidas.»
Las imágenes obtenidas con el SPIM son tan nítidas que es posible observar dentro de los tejidos diseños extremadamente sutiles. Los biólogos especializados en el desarrollo, por ejemplo, esperan captar las explosiones momentáneas de actividad genética, que desempeñan un papel importante en la creación de estructuras corporales, pero que ocurren tan deprisa que se observan en muy contadas ocasiones.
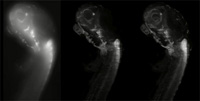
microscopio confocal
estándar. Compárese con la
imagen del mismo tipo de
muestra tomada con un SPIM
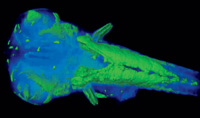
alta resolución de las
proteínas de los peces
La aplicación más inmediata es la oportunidad de observar el desarrollo y la fisiología de los órganos internos. El laboratorio de Jochen Wittbrodt, por ejemplo, está estudiando el desarrollo de un pequeño pez llamado medaka. Un proyecto es observar su corazón. Con el SPIM puede conseguirse una visión sin precedentes de su desarrollo en el espacio y el tiempo. Los científicos pueden visualizar los primeros latidos del corazón en un organismo mirando directamente los tejidos del músculo a través del cuerpo. Están consiguiendo también una perspectiva completamente nueva de cosas que han sido estudiadas durante mucho tiempo, tales como el modo en que la retina se hace redonda para formar el globo ocular. Observando cómo funciona eso, lo mismo en peces sanos que en los que han sufrido mutaciones, han descubierto que la versión de los textos -obtenida de fotos estáticas- debe cambiarse.
Otro proyecto, con claras aplicaciones médicas, sirvió para atraer el interés de Zeiss, uno de los mayores fabricantes de microscopios, con vistas a seguir desarrollando y comercializar el instrumento. «Los peces tienen una sorprendente capacidad para regenerar los caminos nerviosos dañados. Y nosotros podemos observar en tiempo real cómo sus axones restablecen la conexión», dice Jochen. «Así, el nuevo microscopio se ha convertido en una herramienta de rastreo para ayudar a encontrar los genes que afectan a ese proceso. Un día esa información puede que nos ayude a volver a despertar ese poder regenerativo en nuestros propios tejidos.
Institutions
Review
En las últimas décadas ha habido avances significativos en microscopía. Este interesante artículo informativo describe las nuevas técnicas en microscopía – transferencia de energía por resonancia en la fluorescencia (FRET); recuperación de la fluorescencia tras el fotoblanqueo (FRAP) y microscopía por visualización de la vida media de la fluorescencia (FLIM) – y sus fascinantes aplicaciones. La proteína fluorescente verde, una molécula que produce fluorescencia, se está utilizando para marcar proteínas y poder visualizar así el comportamiento de las moléculas; por ejemplo, la interacción de una proteína receptora o la estructura y síntesis de un huso en la división celular. Nuevos desarrollos del microscopio confocal han derivado en el microscopio de iluminación plana selectiva (SPIM), que puede escanear tejidos enteros y no tratados, utilizando un láser para tomar imágenes por capas que se ensamblan con un programa de ordenador para formar una imagen tridimensional. Eso se ha usado para rastrear el desarrollo del globo ocular, lo que ha proporcionado nueva información que anula el actual modelo.
Generalmente, los estudiantes de biología de niveles avanzados y sus profesores están interesados en las aplicaciones de la microscopía – sea de luz, sea electrónica – y en analizar sus limitaciones. Este artículo les informará de los fascinantes desarrollos que están haciendo avanzar esas técnicas y que están ayudando a los científicos a descubrir mecanismos en el oculto mundo de la interacción molecular. El artículo está bien escrito y realzado por ilustraciones que le dan vida, tanto para profesores como para estudiantes.
Shelley Goodman, Reino Unido





