Ένα λαμπρό μέλλον για την οπτική μικροσκοπία Understand article
Μετάφραση από Ευαγγελία Παπαδοπούλου (Evangelia Papadopoulou). Θέλεις να πιάσεις ένα ένζυμο «στα πράσα»; Ή να παρακολουθήσεις έναν εμβρυικό εγκέφαλο να αυτό-συνδέεται; Ο Russ…

Philippe Bastiaens,
Eric Karsenti και
Philipp Niethammer
Μεταξύ της δεκαετίας του 1830 και του 1870, μια σειρά από βελτιώσεις στα οπτικά μικροσκόπια οδήγησε σε μία νέα εποχή για την βιολογία. Τα προηγούμενα μικροσκόπια πλήττονταν από χαμηλή διακριτική ικανότητα και παραμόρφωση της εικόνας διότι βασίζονταν σε έναν μόνο φακό. Η προσθήκη ενός δεύτερου φακού έλυσε μέρος του προβλήματος και το 1830, ο Άγγλος οπτικός Joseph Jackson Lister ανακάλυψε ότι η τοποθέτηση των δύο φακών σε συγκεκριμένη απόσταση μεταξύ τους εξάλειφε ένα είδος παραμόρφωσης που ονομάζεται σφάλμα σφαιρικής εκτροπής. Το αποτέλεσμα ήταν ένα τεράστιο άλμα στην διακριτική ικανότητα που επέτρεψε στον Γερμανό φυσιολόγο Theodor Schwann και τον Matthias Jacob Schleiden, Γερμανό βοτανολόγο, να αποδείξουν ότι οι ζωικοί ιστοί αποτελούνταν από κύτταρα.
Στην μοριακή εποχή, η προσοχή των περισσότερων βιολόγων έχει στραφεί στις πρωτεΐνες και άλλα μόρια που είναι πολύ μικρά για να παρατηρηθούν ως ξεχωριστές οντότητες με το οπτικό μικροσκόπιο. Κάτω από το ηλεκτρονικό μικροσκόπιο, πολύ μεγάλα μόρια ή σύμπλοκα μπορούν να παρατηρηθούν ως θολά σχήματα, αλλά οι πιο σημαντικές λεπτομέρειες εξακολουθούν να λείπουν και είναι αδύνατο να χρησιμοποιηθεί αυτή η μέθοδος σε ζωντανά κύτταρα ή ιστούς.
Στα μέσα της δεκαετίας του 1990, οι επιστήμονες ανακάλυψαν ότι ένα μόριο που εντοπίζεται στις μέδουσες με το όνομα «πράσινη φθορίζουσα πρωτεΐνη», το οποίο κάνει το ζώο να φθορίζει, μπορεί να προσδεθεί σε συγκεκριμένες πρωτεΐνες σε άλλους οργανισμούς. Η διαδικασία αυτή της σήμανσης δημιούργησε νέα, λαμπυρίζοντα μόρια που θα μπορούσαν να εντοπιστούν στο οπτικό μικροσκόπιο καθώς μετακινούνται μέσα στα ζωντανά κύτταρα και τους ιστούς. Έδωσε στους ερευνητές έναν αρκετά απλό τρόπο να αποκτήσουν πληροφορίες σχετικά με το που και το πότε συγκεκριμένες πρωτεΐνες παράγονται στο σώμα, που καταλήγουν στα κύτταρα και τι θα μπορούσαν να κάνουν εκεί.
Τώρα βιολόγοι και φυσικοί έχουν αναπτύξει μεθόδους για να αποκτήσουν ακόμα περισσότερες πληροφορίες από φθορίζουσες πρωτεΐνες. Και μια ακόμα εφεύρεση επιτρέπει στους ερευνητές να παρακολουθούν βιολογικές διεργασίες καθώς συμβαίνουν, στις τρεις διαστάσεις. Επιστήμονες στο Ευρωπαϊκό Εργαστήριο Μοριακής Βιολογίας (EMBL) στη Χαϊδελβέργη της Γερμανίας, χρησιμοποιούν τις τεχνικές αυτές για να ρίξουν μια νέα ματιά στα πιο συναρπαστικά ερωτήματα της βιολογίας.
FRET, FRAP και FLIM
Το μικροσκόπιο του Philippe Bastiaens μοιάζει σαν μια διασταύρωση πάγκου κουζίνας και σόου με φώτα λέιζερ. Το όργανο είναι τοποθετημένο πάνω σε ένα μεταλλικό τραπέζι αρκετά μεγάλο για δέκα άτομα. Όταν ο νεαρός Ολλανδός επιστήμονας γυρίζει τον διακόπτη, μια δεσμίδα μπλε φωτός λεπτή σα βελόνα τρέχει μεταξύ καθρεπτών και φακών σε μοτίβο ζιγκ ζαγκ.
Η δουλειά του λέιζερ είναι να φωτίσει ένα δείγμα που περιέχει φθορίζουσες πρωτεΐνες. Διεγείρει τα άτομα του σημασμένου μορίου, το οποίο στη συνέχεια απελευθερώνει ενέργεια και κάνει το μόριο ορατό. Αυτό συμβαίνει μόνο μία φορά πριν ο φθορισμός του μορίου εξαντληθεί. Αν ένας μεγάλος αριθμός όμοιων, σημασμένων μορίων διεγερθεί, εκπέμπουν ένα μοναδικό μοτίβο ενέργειας. Τα μηχανήματα του Philippe του επιτρέπουν να μετρήσει την ενέργεια αυτή με εξαιρετική ακρίβεια, το οποίο μπορεί να αποδώσει σημαντικές πληροφορίες σχετικά με την δραστηριότητα μιας πρωτεΐνης.
«Για παράδειγμα, το μοτίβο της εκπομπής αλλάζει όταν η πρωτεΐνη προσδένεται σε ένα άλλο μόριο», λέει ο Philippe. «Έτσι μπορούμε να ανιχνεύσουμε το ρυθμό με τον οποίο οι πρωτεΐνες προσδένονται και απελευθερώνονται η μία από την άλλη. Αυτές είναι συχνά αντιδράσεις που συμβαίνουν τόσο γρήγορα που δεν μπορούμε να τις ανιχνεύσουμε με άλλον τρόπο.» Η τεχνική ονομάζεται FLIM (fluorescence lifetime imaging microscopy = μικροσκοπία απεικόνισης φθορισμού ημιζωής).
«Υπάρχουν και άλλες διαφορές που μπορούν επίσης ν’ ανιχνευθούν,» λέει ο Philippe. «Ας υποθέσουμε ότι η πρωτεΐνη που έχεις σημάνει αλληλεπιδρά με ένα άλλο μόριο και προκαλεί μια χημική αλλαγή σε αυτό. Όταν συμβαίνει αυτό, βρίσκεις ένα ακόμη μοτίβο φθορισμού. Μπορείς να φτιάξεις προφίλ για όλα αυτά τα διαφορετικά πράγματα και να πεις πιο από αυτά συμβαίνει. Αυτό μας φέρνει σε θέση να είμαστε ικανοί όχι μόνο να παρακολουθούμε κοντινές αλληλεπιδράσεις μεταξύ μορίων αλλά και να παρατηρήσουμε τι κάνει το ένα στο άλλο. Πιο παλιά, αν ήθελες να πεις ότι ένα μόριο ενεργοποιεί το άλλο, έπρεπε να βασιστείς σε λιγότερο άμεσες ενδείξεις.»
Αν “φωτίσεις” μια περιοχή ενός δείγματος για μεγάλο χρονικό διάστημα (για παράδειγμα, ένα τμήμα του πυρήνα του κυττάρου ή ένα άλλο κυτταρικό διαμέρισμα), όλη η φθορίζουσα ενέργεια εξαντλείται και η περιοχή αποχρωματίζεται. Ο Philippe και οι συνεργάτες του έχουν χρησιμοποιήσει αυτή την τεχνική αποχρωματισμού για να παρατηρήσουν πώς τα μόρια κινούνται δια μέσου του κυττάρου. Για παράδειγμα, οι πρωτεΐνες υποδοχείς στην εξωτερική μεμβράνη βοηθούν τα κύτταρα να δέχονται σήματα από τα γειτονικά και το περιβάλλον. Οι επιστήμονες πίστευαν ότι τα μόρια αυτά εισέρχονται στο κύτταρο για ανακύκλωση, αλλά ήταν δύσκολο να αποδειχτεί. Μπορούσαν να δουν πρωτεΐνες υποδοχείς στο εσωτερικό του κυττάρου, αλλά ήταν δύσκολο να καταλάβουν εάν αυτά τα μόρια ταξίδευαν προς τη μεμβράνη ή αν είχαν μπει πάλι μέσα.
Ο Philippe και οι συνεργάτες του εστίασαν το λέιζερ έτσι ώστε να αποχρωματίσει μια μικροσκοπική περιοχή μέσα στο κύτταρο, όπου είναι γνωστό ότι συλλέγονται οι πρωτεΐνες υποδοχείς. Μετά μπλοκάρανε την παραγωγή νέων πρωτεϊνών, για να σταματήσουν την ροή μορίων που κινούνται προς τα έξω. Όταν η αποχρωματισμένη περιοχή γέμισε ξανά με φθορίζουσες πρωτεΐνες, οι επιστήμονες ήξεραν ότι προέρχονταν από την μεμβράνη. Η μέθοδος αυτή ονομάζεται FRAP (fluorescence recovery after photobleaching = ανάκτηση φθορισμού μετά από φωτοαποχρωματισμό).
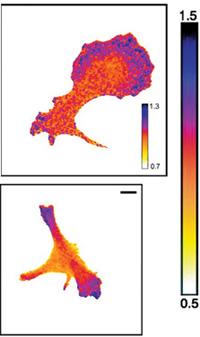
μέσα στα κύτταρα είναι
αποτέλεσμα αλληλεπιδράσεων
μεταξύ μορίων. Το κύτταρο
επάνω είναι σε ακινησία: το
κύτταρο κάτω σέρνεται
πάνω σε μια επιφάνεια.
Χρησιμοποιώντας FRET, οι
επιστήμονες μπορούν να
αποκαλύψουν που
συγκεκριμένες πρωτεΐνες
συνδέονται μεταξύ τους,
εξηγώντας αλλαγές στην
κυτταρική δομή και
συμπεριφορά. Το μπλε
δείχνει περιοχές όπου
πρωτεΐνες σταθμίνης
προσδένονται σε μόρια που
ονομάζονται τουμπουλίνη.
Αυτό συμβαίνει με πολύ
χαμηλότερο ρυθμό στις
κόκκινες περιοχές
Μέσα στην τελευταία δεκαετία, οι επιστήμονες έχουν προσθέσει κόκκινες, κίτρινες και καινούργιες αποχρώσεις του πράσινου στην παλέτα των φθοριζουσών ετικετών πρωτεϊνών. Μία από τις πιο σημαντικές καινούργιες τεχνικές στην μικροσκοπία περιλαμβάνει την παρατήρηση της συμπεριφοράς δύο μορίων με ετικέτες διαφορετικών χρωμάτων. Ο Philippe συγκρίνει τη FRET (fluorescence resonance energy transfer = συντονισμένη μεταφορά ενέργειας φθορισμού) με τη συμπεριφορά ενός κουβά με άμμο.
«Αν δύο μόρια πλησιάσουν το ένα το άλλο τόσο κοντά ώστε να αλληλεπιδρούν μεταξύ τους φυσικά, ανιχνεύεις αλλαγές στον φθορισμό που εκπέμπουν», λέει. «Ας υποθέσουμε ότι ανοίγεις μιας τρύπα στον κουβά σου: η άμμος βγαίνει έξω με έναν συγκεκριμένο ρυθμό. Αν ανοίξεις μια δεύτερη τρύπα, ο ρυθμός με τον οποίο αδειάζει ο κουβάς είναι διαφορετικός. Κάτι παρόμοιο συμβαίνει και στη FRET. Το δεύτερο φθορίζον μόριο απορροφά μέρος της ενέργειας που εκπέμπεται από το πρώτο. Ανιχνεύοντας τη διαφορά στην εκπομπή φθορισμού, παρατηρείς κάτι που οι επιστήμονες προσπαθούσαν να δουν εδώ και πολύ καιρό – άμεσες αλληλεπιδράσεις μεταξύ των πρωτεϊνών.»
Το εργαστήριο του Philippe έχει χρησιμοποιήσει τη FRET για να επιλύσει μερικές σημαντικές επιστημονικές ερωτήσεις. Πόσες πρωτεΐνες υποδοχείς χρειάζονται για να ληφθεί ένα σήμα και τι συμβαίνει όταν το λάβουν; Μία μελέτη έδειξε ότι για έναν συγκεκριμένο υποδοχέα, μόνο ένας πολύ μικρός αριθμός μορίων χρειάστηκε να ενεργοποιηθεί για να ενεργοποιήσει ένα γρήγορο καταρράκτη αντιδράσεων χημικής σηματοδότησης μέσα στο κύτταρο. (Μόνο ένα μικρό σημείο πάνω στην επιφάνεια του κυττάρου έλαμψε με την φθορίζουσα υπογραφή που υποδείκνυε την ενεργοποίηση ενός υποδοχέα.) Και η πιο πρόσφατη δουλειά της ομάδας δείχνει πώς οι συγκεντρώσεις πρωτεϊνών μέσα σε συγκεκριμένες περιοχές του κυττάρου βοηθούν να δημιουργηθούν δομές που ονομάζονται άτρακτοι και είναι απαραίτητες για την κυτταρική διαίρεση. «Οι επιστήμονες πίστευαν πως διαφορετικά χημικά υπο-περιβάλλοντα μέσα στο κύτταρο παίζουν ρόλο στη δομή του» λέει ο Philippe. «Αλλά ήταν δύσκολο να αποδειχτεί. Αυτό είναι ένα από τα πράγματα που μας βοηθάει να κάνουμε η FRET, με το να ζωγραφίζει μια εικόνα των συγκεντρώσεων των διάφορων μορίων καθώς αλληλεπιδρούν μεταξύ τους.»
SPIM
Η ομάδα μικροσκοπίας του Ernst Stelzer στο EMBL έχει εφεύρει ή βοηθήσει να βελτιωθούν πολλοί τύποι μικροσκοπίων. Το πιο πρόσφατο εργαλείο τους, που ονομάζεται μικροσκόπιο φωτισμού επιλεκτικού πεδίου (SPIM), επιτρέπει στους επιστήμονες να κοιτάξουν απευθείας μέσα στα σώματα ζωντανών οργανισμών καθώς αναπτύσσονται.
Ο Ernst και οι συνεργάτες του είχαν ήδη κατασκευάσει συνεστιακά μικροσκόπια που χρησιμοποιούν λέιζερ για να σκανάρουν ένα δείγμα στιβάδα – στιβάδα με απίστευτη ταχύτητα: ένας υπολογιστής μετά συναρμολογεί τα κομμάτια των εικόνων σε μία τρισδιάστατη στοίβα. «Αυτό δεν είναι αρκετό,» λέει, «γιατί εξακολουθεί να περιορίζεται αρκετά στο να κοιτά ιστούς σε επίπεδες επιφάνειες – και όχι στις πραγματικές συνθήκες των κυττάρων και των οργανισμών.» Έτσι ξεκίνησε να ψάχνει έναν τρόπο να σκανάρει ολόκληρους οργανισμούς στα τρισδιάστατα περιβάλλοντά τους.
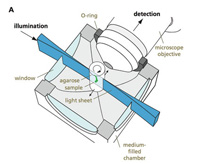
Η πρώτη καινοτομία ήταν να βάλει το δείγμα – λόγου χάρη ένα εμβρυϊκό ψάρι – σε έναν υγρό σωλήνα, έτσι ώστε να μπορεί να παρατηρηθεί απ’ όλες τις πλευρές. Αυτό όμως δεν έλυσε ένα κρίσιμο πρόβλημα της διακριτικής ικανότητας. Τα περισσότερα οπτικά μικροσκόπια ρίχνουν φως σε ένα δείγμα κατά μήκος του οπτικού άξονα – ρίχνοντας φως από τη θέση του ανιχνευτή (μάτι ή κάμερα) και κοιτώντας την αντανάκλαση, ή ρίχνοντας φως μέσα από ένα δείγμα στην κατεύθυνση του ανιχνευτή.
Το SPIM, από την άλλη, περνά μια πολύ λεπτή δέσμη φωτός μέσα από το δείγμα από το πλάι. Μόνο τα αντικείμενα σε εκείνο το κομμάτι – όπως για παράδειγμα φθορίζουσες πρωτεΐνες – φωτίζονται. Ο σωλήνας περιστρέφεται γρήγορα έτσι ώστε να τραβηχτούν εικόνες από διαφορετικές γωνίες. Όσο για το συνεστιακό μικροσκόπιο, ένας υπολογιστής συνθέτει τα κομμάτια σε τρισδιάστατες εικόνες – αυτή τη φορά σε μια συγχρονισμένη ταινία/φιλμ.
«Το πλεονέκτημα του να φέρνεις το φως από το πλάι σχετίζεται στενά με το πώς τα μικροσκόπια επιτυγχάνουν την διακριτική ικανότητα,» λέει ο Ernst. «Αν ρίξεις φως σε ένα αντικείμενο και το εξετάσεις από την ίδια διεύθυνση, υπάρχουν περιπτώσεις όπου απλά δεν υπάρχει απλός τρόπος να κρίνεις τι είναι μπροστά και τι είναι πίσω, ή πόσο μακριά είναι ακριβώς. Μπορείς να αποκτήσεις καλή διακριτική ικανότητα κατά μήκος της δισδιάστατης επιφάνειας που βλέπει προς τα εσένα, και μπορείς να μελετήσεις διαφορετικές στιβάδες ενός δείγματος μετακινώντας το εστιακό επίπεδο πάνω και κάτω, αλλά είναι γεγονός ότι εξακολουθείς να φωτίζεις αντικείμενα επάνω και κάτω από το εστιακό επίπεδο, το οποίο παραμορφώνει την δισδιάστατη εικόνα. Είναι αναπόφευκτα θολές – επιμηκυμένες στην τρίτη διάσταση.»
Οι εικόνες του SPIM είναι τόσο ευκρινείς που είναι δυνατό να παρατηρήσεις εξαιρετικά ανεπαίσθητα μοτίβα μέσα στους ιστούς. Για παράδειγμα, οι αναπτυξιακοί βιολόγοι ελπίζουν να απαθανατίσουν στιγμιαίες εκρήξεις γενετικής δραστηριότητας που παίζουν σημαντικό ρόλο στην δημιουργία δομών μέσα στο σώμα, αλλά συμβαίνουν τόσο γρήγορα που σπανίως παρατηρούνται.
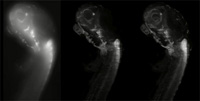
συνεστιακό μικροσκόπιο.
Συγκρίνετε με τις εικόνες
από τον ίδιο τύπο δείγματος
από SPIM (κέντρο και δεξιά)
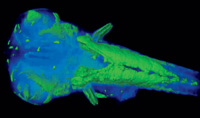
χρωματική ανακατασκευή
των πρωτεϊνών στο ψάρι
Η πιο άμεση εφαρμογή είναι η ευκαιρία να παρακολουθήσεις την ανάπτυξη και την φυσιολογία των εσωτερικών οργάνων. Το εργαστήριο του Jochen Wittbrodt, για παράδειγμα, μελετά την ανάπτυξη ενός μικρού ψαριού που ονομάζεται ρυζόψαρο (ιαπωνικό ρυζόψαρο). Ένα πρότζεκτ περιλαμβάνει την μελέτη της καρδιάς, και με τη χρήση του SPIM, μπορεί να ληφθεί μια πρωτοφανής οπτική της ανάπτυξής της στο χώρο και στο χρόνο. Οι επιστήμονες μπορούν να οπτικοποιήσουν τους πρώτους χτύπους της καρδιάς ενός οργανισμού – με το να κοιτάζουν μέσα από το σώμα κατευθείαν στους μυϊκούς ιστούς. Επίσης αποκτούν μια εντελώς καινούργια αντίληψη για πράγματα που μελετώνται εδώ και καιρό, όπως για παράδειγμα ο τρόπος που ο αμφιβληστροειδής μαζεύεται έτσι ώστε να σχηματίσει το πίσω εσωτερικό τοίχωμα του οφθαλμού. Με την παρατήρηση της διαδικασίας αυτής τόσο σε υγιή ψάρια όσο και σε ψάρια με μεταλλάξεις, ανακάλυψαν ότι η εκδοχή των βιβλίων – που έχει αποκτηθεί από στατικές εικόνες – πρέπει να αλλάξει.
Ένα άλλο πρότζεκτ με άμεσες ιατρικές εφαρμογές βοήθησε να προσελκύσει το ενδιαφέρον της Zeiss, μιας από τις μεγαλύτερες κατασκευάστριες εταιρίες μικροσκοπίων παγκοσμίως, με σχέδια για την περαιτέρω ανάπτυξη και προώθηση του εργαλείου. «Τα ψάρια έχουν μια απίστευτη ικανότητα να αναγεννούν νευρικά μονοπάτια που έχουν υποστεί βλάβη, και μπορούμε να παρακολουθήσουμε σε πραγματικό χρόνο καθώς οι άξονές τους αποκαθιστούν την επαφή τους,» λέει ο Jochen. «Έτσι το καινούργιο μικροσκόπιο έχει γίνει ένα εργαλείο διαλογής για να μας βοηθήσει να βρούμε τα γονίδια εκείνα που επηρεάζουν αυτή τη διαδικασία. Κάποια μέρα η πληροφορία αυτή μπορεί να μας βοηθήσει να αφυπνίσουμε την αναγεννητική αυτή ικανότητα στους δικούς μας ιστούς.»
Institutions
Review
Έχει παρατηρηθεί αξιοσημείωτη πρόοδος στην μικροσκοπία την τελευταία περίπου δεκαετία, ειδικά με την εισαγωγή της συνεστιακής μικροσκοπίας. Αυτό το ενδιαφέρον και ενημερωτικό άρθρο περιγράφει νέες τεχνικές μικροσκοπίας – τη συντονισμένη μεταφορά ενέργειας φθορισμού (FRET), την ανάκτηση φθορισμού μετά από φωτοαποχρωματισμό (FRAP), και την απεικόνιση του χρόνου ημιζωής του φθορισμού (FLIM) – και τις συναρπαστικές τους εφαρμογές. Η πράσινη φθορίζουσα πρωτεΐνη, ένα μόριο που φθορίζει, χρησιμοποιείται για να σημάνει πρωτεΐνες έτσι ώστε η μοριακή συμπεριφορά, π.χ. η αλληλεπίδραση υποδοχέα πρωτεΐνης και η δομή και η σύνθεση της ατράκτου κατά την κυτταρική διαίρεση, μπορεί να οπτικοποιηθεί. Περαιτέρω ανάπτυξη του συνεστιακού μικροσκοπίου οδήγησε στο μικροσκόπιο φωτισμού επιλεκτικού πεδίου (SPIM), το οποίο μπορεί να σαρώσει ολόκληρο, ακατέργαστο ιστό χρησιμοποιώντας λέιζερ για να πάρει κομμάτια εικόνων τα οποία στη συνέχεια επανασυναρμολογούνται από ένα πρόγραμμα υπολογιστή για να σχηματίσουν μία τρισδιάστατη εικόνα. Έχει χρησιμοποιηθεί για την παρακολούθηση της ανάπτυξης του βολβού του ματιού, που οδήγησε σε νέες πληροφορίες που ανατρέπουν το υπάρχον μοντέλο.
Φοιτητές βιολογίας προχωρημένου επιπέδου και οι καθηγητές τους συνήθως λαμβάνουν υπόψιν την εφαρμογή της οπτικής και ηλεκτρονικής μικροσκοπίας, εξετάζοντας τους περιορισμούς τους. Αυτό το άρθρο θα τους ενημερώσει για τις συναρπαστικές εξελίξεις που πάνε αυτές τις τεχνικές ένα βήμα παραπέρα και βοηθούν τους επιστήμονες να ανακαλύψουν μηχανισμούς στον κρυμμένο κόσμο της μοριακής αλληλεπίδρασης. Το άρθρο είναι καλογραμμένο, και έχει βελτιωθεί με εικόνες που το ζωντανεύουν τόσο για καθηγητές όσο και μαθητές.
Shelley Goodman, UK





