Titanic und die eisenfressenden Bakterien Understand article
Eine Bakterienart, die auf dem zerfallenden Wrack der Titanic entdeckt wurde, gewährt neue Einblicke, wie lebende Zellen vor Schaden geschützt werden können.
Das Wrack der Titanic liegt auf dem Grund des Ozeans, fast 4 km unter der Oberfläche des dunklen, salzhaltigen Wassers des Nordatlantiks. Auf Expeditionen zum Fundplatz bemerkten Taucher „Rusticels“ – eiszapfenartige Auswüchse reich an Rost – die Teile des beschädigten und korrodierten Schiffkörpers bedecken. Forscher, die von der Titanic stammende Rusticels untersuchten, entdeckten 2010 eine neue Bakterienart innerhalb dieser Auswüchsew1. Sie nannten die neue Art Halomonas titanicae

Wikimedia Commons (public domain)
Die Wissenschaftler haben auch entdeckt, dass Halomonas titanicae Bakterien an dem Rostvorgang beteiligt sind und den Zerfall des Wracks beschleunigen. Der Zerfall verläuft ziemlich schnell: Schätzungen nach könnte das Wrack gegen 2030 vollständig verschwunden sein. Diese Bakterien könnten daher eine erhebliche Bedrohung für Ölbohrplattformen und andere sich in der Tiefsee befindlichen Eisenstrukturen darstellen. Allerdings sind diese Organismen jetzt aus einem anderen Grund in den Fokus der wissenschaftlichen Forschung gerückt: Um herauszufinden, wie sie es schaffen, unter Bedingungen mit hohen und schwankenden Salzkonzentrationen gut zu wachsen.
Salze und die lebende Zelle
Der Begriff halo bedeutet Salz auf Griechisch. Bakterien der Gattung Halomonas leben in salzigem Umfeld wie Meerwasser oder in der Marsch, wo die Salzkonzentrationen über einen großen Bereich schwanken. Alle Vertreter dieser Gattung sind stark „halotolerant“: Sie haben Wege entwickelt, mit unbändig fluktuierenden Salzkonzentrationen außerhalb der Zelle umzugehen, sodass sie über eine riesige Bandbreite an Salzgehalt von 0.5% bis zu 25% Gewichtsprozent Kochsalz überleben können. Dies mag trivial klingen, ist es aber nicht.

Mit freundlicher Genehmigung von Lori Johnston, RMS Titanic Expedition 2003, NOAA-OE
Sehr dünne Membranen, die den Verkehr in die und aus der Zelle kontrollieren und somit große Unterschiede in der Zusammensetzung zwischen innerhalb und außerhalb der Zelle unterstützen, schützen die Zelle vor der Außenwelt. Zum Beispiel halten Zellen ein elektrisches Potenzial von etwa 100 Millivolt über die Membran, die typischerweise nur 10 Nanometer breit ist, aufrecht. Für alle Zelltypen ist Natriumchlorid (NaCl) das dominante Salz außerhalb der Zelle (zum Beispiel im Blutserum), wohingegen Kaliumchlorid (KCl) innerhalb der Zelle dominant ist. Dennoch, während die Salztypen unterschiedlich sind, sollte sich die Gesamtsalzkonzentration auf beiden Seiten der Zelle genau entsprechen. Der Grund hierfür ist Osmose: Wenn zwei Lösungen mit unterschiedlichen Konzentrationen durch eine Membran, die für Wasser aber nicht für die gelösten Stoffe durchlässig ist, getrennt sind, wird das Wasser von der verdünnten Seite zu der konzentrierten Seite fließen.
Zellmembranen können osmotischen Druckunterschieden nicht standhalten. Dass rote Blutzellen platzen, wenn sie in reines Wasser platziert werden, veranschaulicht die Wirkung von osmotischem Druck – und die Zerbrechlichkeit von Zellmembranen. Offensichtlich müssen Halomonas Bakterien, um ihre Membranen intakt zu halten, in der Lage sein, die Konzentration von gelösten Stoffen im Zytoplasma als Antwort auf sich ändernde äußere Salzkonzentrationen zu regulieren, ohne die Biochemie innerhalb der Zelle zu zerstören (siehe Zaccai 2009). Wie machen sie das?
Halomonas Bakterien produzieren große Mengen einer Substanz namens Ectoin (siehe Abbildung 1). Um die äußere Salzkonzentrationen auszugleichen, passen sie die Konzentration dieser löslichen Verbindung innerhalb ihrer Zellen an. Das hält die Flüssigkeiten der Zelle in osmotischem Gleichgewicht mit der äußeren Seite, sodass die Zelle sogar unter extremen Bedingungen vor dem Schrumpeln oder Platzen geschützt ist. Bemerkenswerterweise scheint sich Ectoin anders als die meisten Salze und gelösten Stoffe, die mit der Rolle von Wasser in metabolischen Prozessen interferieren, zu verhalten. Ectoin ist ein sogenanntes „Extremolyt“ oder „Kompatible Solute“, ein schützendes Molekül, das in der Zelle vorkommt und dort, trotz extremer Umweltbedingungen, den normalen Ablauf biochemischer Prozesse ermöglicht. Es erhöht auch die Stabilität von Proteinen und Membranen. Also wie erreicht dieser ungewöhnliche Stoff diese Ergebnisse?
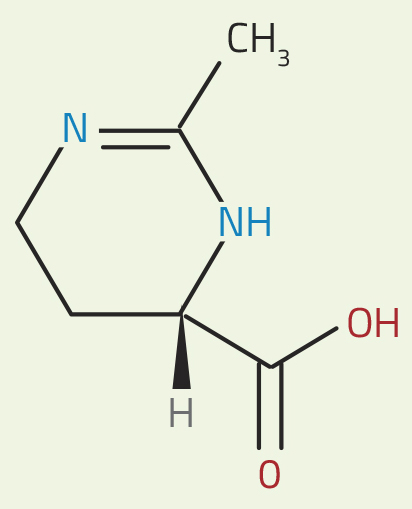
Struktur von Ectoin. In
Wasser wird die rote Gruppe
negativ geladen (durch den
Verlust eines H+ Ions) und
die blaue Gruppe wird positiv
geladen (durch die Erlangung
eines H+ Ions). Die geladenen
Gruppen bilden dann
Wasserstoffbindungen mit
angrenzenden
Wassermolekülen.
Nicola Graf
Ectoin und das Netzwerk von Wasserstoffbindungen
Hinweise wie genau Ectoin auf der molekularen Ebene funktioniert, wurden kürzlich unter Verwendung der fortgeschrittenen experimentellen Technik der Neutronenstreuung entdeckt (siehe Textbox). Durchgeführt von der internationalen Kollaborationw2 unter Einbeziehung des Institut Laue-Langevin (ILL)w3, zeigten die Experimente, wie Ectoin die Schichten von Wasser um Proteinmoleküle und auf Membranoberflächen beeinflusst (Zaccai et al., 2016). Normalerweise interagieren Wassermoleküle über ein Netzwerk von Wasserstoffbindungen miteinander. Die Atome in einem Wassermolekül interagieren mit benachbarten Molekülen, wobei jedes Sauerstoffatom als Empfänger von zwei Wasserstoffbindungen und jedes Wasserstoffatom als Spender einer Bindung agiert. Dies resultiert in einem höchstdynamischen Netzwerk von intramolekularen Bindungen, wobei die Moleküle Milliarden (109) mal pro Sekunde die Partner wechseln.
Die Anziehung zwischen Wassermolekülen stellt also die Grundlage des “hydrophobischen Effekts” dar, der Öl und Wasser trennt. Der hydrophobische Effekt ist in vielen biologischen Prozessen wichtig, darunter die dreidimensionale Faltung von Proteinmolekülen und die Bildung von Membranen. Wasserstoffbindungsdynamiken sind daher ein essentieller Faktor dafür, wie lebende Zellen organisiert sind.
Andere Substanzen in Wasser, wie zum Beispiel Salze, können diese Organisation behindern. Aber, wie die Neutronenexperimente enthüllt haben, scheint Ectoin Wasserstoffbindungsdynamiken eher zu verstärken – zumindest teilweise – als sie zu behindern. Dieses Molekül enthält eine positiv geladene Gruppe (in Abbildung 1 in blau dargestellt) und eine negativ geladene Gruppe (dargestellt in rot). Diese geladenen Gruppen interagieren mit Wassermolekülen, sodass das naheliegende Netzwerk von Wasserstoffbindungen etwas weniger dynamisch gemacht wird – aber es entsteht dadurch auch ein etwas weiter entferntes dynamischeres Netzwerk von Wassermolekülen.
Außerhalb des bakteriellen Kontexts erweist sich Ectoin als ein nützlicher Bestandteil in Kosmetika und klinischen Behandlungen, weil es Entzündungen in Säugetierzellen reduzieren kann. Der wahrscheinliche Grund hierfür ist, dass Ectoin, indem es Proteine und Membranen stabilisiert, menschliche Zellen vor Schaden schützt, und somit Entzündungen reduziert und ein Mittel für Konditionen wie Allergien, Ekzeme, und Husten und Erkältungssymptome liefert.
Zurück zur Titanic
Obwohl die Neutronenexperimente den Wissenschaftlern geholfen haben, zu verstehen, wie Halomonas Bakterien in der potentiell feindlichen Umgebung der versunkenen Titanic überleben, bleibt die genaue Rolle von Halomonas titanicae für die Rostbildung ungeklärt. Aber es hier gibt gute Nachrichten: Diese eisenfressenden Bakterien könnten eine Rolle in zukünftigem Abfallmanagement spielen, indem sie den Abbau von Metallschrott –neben historischen Wracks – auf dem Ozeangrund beschleunigen.
Neutronenstreuung
Neutronenstreuung ist eine leistungsfähige Methode, um die Struktur von Materialien, einschließlich Wasser und seine Interaktionen mit anderen Verbindungen, zu untersuchen.
Der Kern eines Wasserstoffatoms ist ein einzelnes Proton. Neutronen und Protonen sind sehr ähnliche Partikel (abgesehen von ihrer elektrischen Ladung), und Neutronen stoßen Protonen stark ab, so wie Snookerbälle voneinander abprallen. Das Neutronenstreuungsmuster liefert Informationen über die Lage der Sauerstoff- und Wasserstoffatome in benachbarten Wassermolekülen, und damit über das dynamische Netzwerk von Wasserstoffbindungen, die sie verbinden.
Bei der Neutronenstreuung wird ein anderer nützlicher Trick genutzt. Der Kern von Deuterium Atomen (ein Wasserstoffisotop mit einem Proton und einem Neutron in seinem Kern) streut Neutronen in einer ganz anderen Weise als ein normaler Wasserstoffkern. Indem man den Wasserstoff in einer spezifischen Verbindung (zum Beispiel Ectoin) durch Deuterium ersetzt, ist es möglich, den Beitrag an dem Streuungssignal von nur dieser Verbindung, in Abgrenzung zu dem von umliegenden Wassermolekülen, zu sehen. Dies hilft wiederum dabei, die Details ihrer Interaktionen zu enthüllen.Neutronenstreuung mit Deuterium Markierung lieferte eine reiche Ernte an Ergebnissen in der Strukturbiologie. Diese beinhaltet Einblicke in die komplexen Interaktionen zwischen Proteinmolekülen, und denen zwischen Proteinen und Nukleinsäuren (DNA, RNA).

©ILL/L. Thion
References
- Zaccai G (2009) The intracellular environment: not so muddy waters. Science in School 13: 19-23.
- Zaccai G et al. (2016) Neutrons describe ectoine effects on water H-bonding and hydration around a soluble protein and a cell membrane. Scientific Reports 6: 31434. doi:10.1038/srep31434
Web References
- w1 – Halomonas titanicae Bakterien wurden von Wissenschaftlern der Universitäten in Sevilla, Spanien, und Toronto und Halifax, Kanada, entdeckt. Lesen Sie einen wissenschaftlichen Bericht über die Entdeckung auf der UNESCO Webseite.
- w2 – Die kollaborierenden Organisationen schlossen das Institut Laue-Langevin und das Institut de Biologie Structurale in Grenoble, Frankreich, und das Max Planck Institut für Biochemie und das Biotechnologie-Unternehmen Bitop in München, Deutschland, ein. Schauen Sie für mehr Informationen in den Abschnitt mit weiterführenden Informationen in Zaccai et al. (2016).
- w3 – Das Institut Laue-Langevin (ILL) ist ein internationales Forschungszentrum an der Spitze der Neutronenwissenschaft und -technologie, mit Sitz in Grenoble, Frankreich.
Resources
- Finden Sie mehr über Mikroben, die auf Schiffwracks leben, und über die Rolle von Ectoin in einem offen zugänglichen Artikel auf der BBC Webseite heraus.
Institutions
Review
Das Wrack der Titanic ist sehr bekannt, sodass dieser Artikel dafür genutzt werden kann, Schüler für Wissenschaft zu begeistern. Er kann auch als Anreiz dienen, tiefer in die Welt der Bakterien und deren Nutzen für Menschen –trotz ihrer normalerweise negativen Assoziationen – einzutauchen.
Der Artikel könnte nützlich für den Biologieunterricht sein, um zu erkunden, wie prokaryotische Organismen extreme Umweltbedingungen überleben können, und wie Substanzen über die Zellmembran übertragen werden. Er könnte auch im Chemieunterricht genutzt werden, um über Wasserstoffbindungen und ihre Interaktionen zwischen Wasser und anderen Molekülen zu unterrichten. Schließlich ist Recycling unter Verwendung von Halomonas titanicae für Ökologie und die Erforschung der Energiebilanz zwischen Ökosystemen relevant.
Alina Giantsiou-Kyriakou, Biologielehrerin, Livadia High School, Zypern





