Uracil u DNK: greška ili signal? Understand article
Prevela: Aleksandra Zečić, Biološki fakultet, Beograd. Uracil je poznat kao jedna od baza koja ulazi u sastav u RNK, ali zašto ne ulazi u sastav DNK – ili ipak ulazi? Angéla Békési i Beáta G Vértessy istražuju.
Timin naspram uracila
Naša genetička informacija je uskladištena u vidu DNK, korišćenjem četiri slova abecede. Četiri ‘slova’ predstavljaju četiri hemijske baze koje svaki gradivni blok DNK – zvani nukleotid – može imati: adenin (A), timin (T), citozin (C) i guanin (G; vidi Sliku 1). Kao što su James Watson i Francis Crick slavno otkrili, DNK obrazuje dvolančani heliks u kojem se četiri baze uvek sparuju na isti način, putem specifičnih vodoničnih veza: adenin se vezuje sa timinom, a guanin sa citozinom ( vidi Slike 2 i 3).
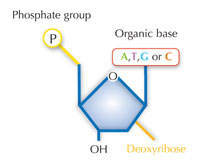
Slika dobijena od Nicola Graf
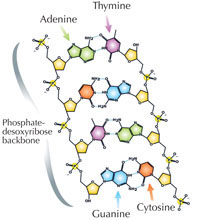
Slika dobijena od Madeleine Price Ball; izvor: Wikimedia Commons
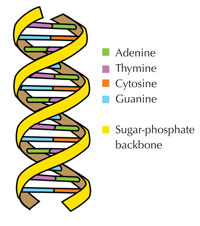
Slika dobijena od Forluvoft; izvor: Wikimedia Commons
Međutim, postoji alternativno peto slovo: uracil (U), koje obrazuje vodoničnu vezu sa adeninom (A) po istom obrazcu (vidi Sliku 4). Ali, premda je uracil uobičajeno prisutan u RNK, to nije slučaj u DNK, gde je umesto njega prisutan timin. Zašto bi to moglo biti? Zbog čega je to tako?
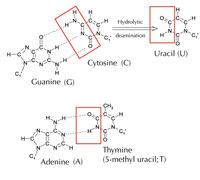
Slika dobijena od Angéla Békési
Hemijski, timin je molekul uracila sa dodatnom metil grupom. Šta bi, u evolutivnom smislu, bila prednost prisustva ovog kompleksnijeg gradivnog bloka u DNK? Odgovor možda leži u tome kako ćelije popravljaju oštećenja DNK.
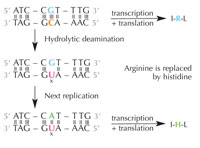
deaminacija citozina može
promeniti aminokiseline
kodirane sekvencom. Kliknite
da uvećate sliku
Slika dobijena od Nicola Graf
Citozin se može spontano transformisati u uracil putem procesa označenog kao hidrolitička deaminacija (vidi Sliku 4). Kada se ovo desi, guanin, koji je prvobitno bio vezan za molekul citozina, sada umesto nasuprot citozinu dolazi nasuprot uracilu (setite se da se uracil uobičajeno vezuje za adenin). Kada ćelija sledeći put replicira svoju DNK, na poziciji nasuprot molekula uracila biće adenin umesto guanina koji je trebao da bude tamo, menjajući poruku koju ovaj segment DNK kodira (vidi Sliku 5). Ovaj process deaminacije citozina je jedan od najčešćih oštećenja DNK, ali se obično uspešno ispravlja. Kako ćelija ovo radi?
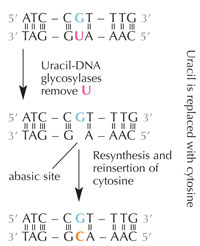
deaminacije. Kliknite da
uvećate sliku
Slika dobijena od Nicola Graf
Ćelije imaju reparacioni sistem koji može otkriti da se uracil nalazi tamo gde bi trebao da bude citozin, i koji ispravlja grešku pre nego što se ona replicira i prosledi. Ova složena mašinerija se sastoji od nekoliko enzima: prvo uracil – DNK glikozilaza prepoznaje uracil i iseca ga iz DNK. Potom nekoliko enzima doprinose eliminaciji i ponovnoj sintezi ostećenog segmenta DNK, tokom kojih se ‘prazno’ mesto (bez baze) u DNK zamenjuje citozinom (vidi Sliku 6).
Međutim, uobičajena forma uracil – DNK glikozilaze ne može znati sa kojom bazom je sparen uracil, npr. bilo da je uracil očekivano tamo (ako je vezan sa adeninom) ili se radi o mutiranom citozinu (i nasuprot njemu guaninu), pa će prepoznati i iseći oba tipa uracila. Očigledno, ovo bi moglo prouzrokovati probleme. Smatra se da rešenje ovog potencijalnog problema leži u evolucionom mehanizmu zahvaljujući kome su ‘ispravni’ uracili (spareni sa adeninom) bili označeni metil grupom – dajući timin. Ovako, ako bi ćelijska mašinerija pronašla uracil, ona bi ga isekla i popravila, ali ukoliko bi našla uracil označen metil grupom – timin (vidi Sliku 4) – ostavila bi ga u lancu. Stoga je tokom vremena timin u DNK standardno zamenio uracil, pa većina ćelija sada ima uracil samo u RNK.
Zašto je uracil sačuvan u RNK? RNK je kraćeg veka od DNK i – sa par izuzetaka – nije skladište za dugotrajno čuvanje genetičke informacije, tako da citozinski molekuli koji se spontano transformišu u uracile u RNK ne predstavljaju veliku pretnju ćeliji. Stoga verovatno nije bilo evolutivnog pritiska da se uracil zameni složenijim (i po svoj prilici skupljim) timinom u RNK.
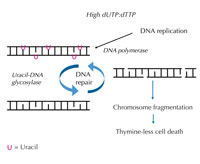
poraste, DNK polimeraza
često ugrađuje uracil umesto
timina i tokom replikacije i
tokom popravke. Uracil-DNK
glikozilaza uklanja uracil i
inicira dalju popravku
uključujući prekide DNK
lanca u međukoraku.
Međutim, ponovna sinteza
može ponovo uvesti uracil,
dovodeći do bezuspešnog
ciklusa popravke DNK. Sistem
je na kraju preopterećen i
događa se fragmentacija
hromozoma, dovodeći do
ćelijske smrti. Kliknite da
uvećate sliku
Slika dobijena od Angéla Békési
Ćelijska smrt usled nedostatka timina
Kada se DNK sintetiše, enzimi DNK polimeraze (koji katalizuju sintezu) ne mogu razlikovati timin od uracila. Oni samo proveravaju da li se vodonične veze pravilno obrazuju, npr. da li su bazni parovi pravilno spareni. Ovim enzimima nije bitno da li se za adenin vezuje timin ili uracil. Naravno, količine deoksiuridin trifosfata (dUTP, izvor uracila) u ćeliji se održavaju niskim u poređenju sa nivoom deoksitimidin trifosfata (dTTP, izvor timina), sprečavajući ugradnju uracila prilikom sinteze DNK.
Ukoliko se ova precizna kontrola poremeti i odnos dUTP prema dTTP poraste, količina uracila koji je pogrešno ugrađen u DNK takođe raste. Sistem za popravke – koji, za razliku od DNK polimeraza, može razlikovati uracil od timina – tada pokušava da iseče uracil uz pomoć uracil-DNK glikozilaze i da ponovo sintetiše DNK, što uključuje privremeno razmicanje (raskidanje) DNK lanca. Međutim, ukoliko je odnos dUTP prema dTTP još uvek povišen, pri toj ponovnoj sintezi može se ponovo ugraditi uracil umesto timina. Kada se ova privremena isecanja u DNK dešavaju jedno nakon drugog i veoma blizu jedno drugom, ovaj ciklus na kraju dovodi do kidanja delova DNK i fragmentacije hromozoma (vidi Sliku 7). Ovo za posledicu ima specifičan tip programirane ćelijske smrti zvane ćelijska smrt usled nedostatka timina.
Procesi ćelijske smrti usled nedostatka timina mogu biti iskorišćeni u lečenju raka. Kako se kancerogene ćelije razmnožavaju sa jako visokom stopom u poređenju sa normalnim ćelijama, one sintetišu veću količinu DNK za dati vremenski period i stoga zahtevaju znatne količine dUTP. Povećanjem odnosa dUTP prema dTTP, ove kancerogene ćelije mogu biti selektivno ciljane i eliminisane.
Uracilska DNK još uvek postoji
Premda većina ćelija poseduje uracil u RNK i timin u DNK, postoje izuzeci. Neki organizmi imaju uracil umesto timina u svim svojim DNK, a drugi organizmi imaju uracil samo u nekim od svojih DNK. Šta bi mogla biti evolutivna prednost toga? Pogledajmo neke primere.
Uracil u virusnoj DNK
faga koji inficira bakterijsku
ćeliju
Slika dobijena od: cdascher /
iStockphoto
Za dve vrste faga (virusa koji inficiraju bakterije) se zna da imaju DNK genome samo sa uracilom, bez timina. Još uvek ne znamo da li su ovi fagi predstavnici jedne prastare životne forme koja nikad nije razvila timinsku DNK, ili su njihovi genomi sa zamenjenim uracilom novorazvijena strategija. Niti mi znamo zašto ovi fagi koriste uracil umesto timina, a to može igrati ključnu ulogu u životnom ciklusu ovih virusa. Ukoliko je to slučaj, imalo bilo bi smisla da se virusi osiguraju da uracil u njihovoj DNK neće biti zamenjen timinom. I za jedan od ovih faga se i pokazalo da ima gene koji kodiraju specifičan protein koji inhibira uracil-DNK glikozilazu domaćina, sprečavajući tako da uracil virusnog genoma bude ‘popravljen’ od strane enzima domaćina.
Programirana ćelijska smrt u životnim ciklusima insekata

lack the enzyme capable of
removing uracil from their
DNA
Image courtesy of spxChrome
/ iStockphoto and Nicola Graf
Čini se da uracil-DNK takođe igra ulogu u razvoju endopterigota – insekata koji prolaze kroz stadijum lutke u svojim životnim ciklusima (mravi i leptiri da; skakavci i termiti ne). Ovim insektima nedostaje glavni gen za uracil-DNK glikozilazu, koja bi inače uklonila uracil iz njihove DNK.
Štaviše, naše sopstveno istraživanje je pokazalo da je u larvi voćne mušice Drosophila melanogaster odnos dUTP i dTTP regulisan na neobičan način: u svim tkivima koja neće biti potrebna odraslom insektu je mnogo manji nivo enzima koji razgrađuje dUTP i generiše prekursor za produkciju dTTP. Otuda se značajne količine uracila ugrađuju u ova tkiva tokom sinteze DNK.
Dakle, tokom larvalnih stadijuma uracil-DNK se proizvodi, ali izgleda da ne biva ispravljena u tkivima koja će biti razgrađena tokom stadijuma lutke. Kako ovim insektima na stadijumu lutke nedostaje glavni enzim uracil-DNK glikozilaza,dodatni uracil-DNK-specifični faktori mogu prepoznati ovaj akumulirani uracil kao signal da se inicira ćelijska smrt. Već smo identifikovali protein specifičan za insekte koji je izgleda sposoban za degradaciju uracil-DNK i istražujemo da li se ovaj enzim i koristi za iniciranje ćelijske smrti.
Blagotvorne greške: kičmenjački imuni sistem

sekvencama gena antitela
izaziva odgovor za popravku
DNK, što ima efekat
povećanja raznolikosti
proteina antitela. Obiman pul
antitela povećava šansu da
imuni sistem prepozna
neželjene napadače
Slika dobijena od: taramol /
iStockphoto
Uracil u DNK, međutim, može biti nađen i mnogo bliže – u imunom sistemu kičmenjaka kao što smo mi. Deo našeg imunog sistema, adaptivni imuni sistem, produkuje veliki broj različitih antitela koja su zadužena da nas štite od specifičnih patogena. Da bi povećali broj različitih antitela koja mogu biti stvorena, mi mešamo DNK sekvencu u regionima koji kodiraju data antitela, ne samo rekombinovanjem postojećih sekvenci u ćelijama već i stvaranjem novih putem veoma povećanih stopa mutacija, poznatih kao hipermutacije.
Hipermutacija počinje specifičnim enzimom (aktivacijom-indukovana deaminaza) koja menja citozin u uracil (vidi Sliku 4) na specifičnom DNK lokusu, izazivajući reparativni odgovor sklon greškama, koji organizam koristi za sopstvenu korist: ‘greške’ generišu nove sekvence koje mogu biti iskorišćene da se naprave različita antitela. Ovaj sistem je veoma precizno regulisan, ali, ako bi se izmakao kontroli, to bi moglo dovesti do pojave raka.
Kad razmatramo pitanje zašto uracil ili zašto timin, potrebno je da to stavimo u evolutivni kontekst. Živi organizmi su evoluirali u neprekidno promenljivom okruženju, suočavajući se sa dinamičnim setom izazova. Stoga, rešenje kojim se izbegava da se greške ugrađuju u DNK je korisno za većinu organizama i ćelija, što objašnjava zašto je timinska DNK postala pravilo. Međutim, pod određenim okolnostima, ‘greške’ same po sebi mogu biti blagotvorne, zbog čega neke ćelije još uvek koriste uracil u svojoj DNK.
Resources
- Da biste saznali više o radu istraživačke grupe Beáta Vértessy, posetite: www.enzim.hu/~vertessy
- Za preuzimanje rezimea doktorske disertacije Villő Muha, koja je napisana pod mentorstvom Beáta Vértessy na temu uracil- DNK u Drosophila melanogaster, koristite link: http://teo.elte.hu/minosites/tezis2010_angol/v_muha.pdf
-
Kompletna disertacija je dostupna ovde: http://teo.elte.hu/minosites/ertekezes2010/muha_v.pdf
-
Review
Ovaj članak pokazuje da nauka nikad ne spava, dovodeći u pitanje dogmu da uracil postoji samo u RNK. Kako članak objašnjava, ovo nije uvek slučaj. Čak i kada jeste, zašto bi to trebalo biti tako?
Da bi se pomoglo studentima da razumeju članak, propratna pitanja bi mogla biti:
- Opišite vezivne strukture između dva komplementarna bazna para u DNK.
- Koja baza je zamenjena u RNK?
- Opišite i nacrtajte grafikon puta enzima za reparaciju, aktiviranog kada je uracil pronađen u DNK.
- Odnos kojih molekula bi mogao biti prilagođen da bi se sprečio rast i deljenje kancerogenih ćelija?
- Zašto se uracil ‘toleriše’ u RNK?
- Koji živi organizmi koriste uracilsku DNK i kako?
Friedlinde Krotscheck, Austrija





