Uracyl w DNA: błąd czy znak? Understand article
Tłumaczenie: Karina Derewenda. Uracyl to powszechnie znana zasada chemiczna występująca w RNA. Dlaczego więc nie pojawia się w DNA? A może jednak można ją tam spotkać? Angéla Békési i Beáta G Vértessy starają się znaleźć odpowiedź.
Tymina vs. uracyl
Informacja genetyczna przechowywana jest w postaci DNA, przy użyciu czteroliterowego alfabetu. Cztery 'litery' odpowiadają czterem zasadom chemicznym, mogącym tworzyć każdą cząstkę DNA, zwaną także nukleotydem: adenina (A), tymina (T), cytozyna ( C ) i guanina (G; patrz rys. 1). Jak zostało odkryte przez Jamesa Watsona i Francisa Cricka, DNA tworzy podwójną helisę w której wspomniane zasady łączą się w pary w ściśle określony, jednakowy sposób, poprzez specyficzne wiązania wodorowe: adenina łączy się z tyminą, a guanina z cytozyną (patrz rys. 2 i 3).
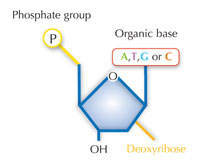
Zdjęcie dzięki uprzejmości Nicola Graf
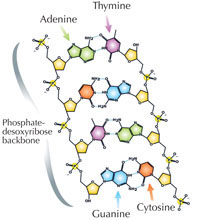
Zdjęcie dzięki uprzejmości Madeleine Price Ball; źródło: Wikimedia Commons
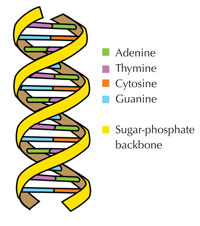
Zdjęcie dzięki uprzejmości Forluvoft; źródło: Wikimedia Commons
Istnieje jednak jeszcze alternatywna, piąta litera: uracyl (U), posiadająca taki sam system wiązań wodorowych z adeniną (patrz rys. 4). Jednak, pomimo powszechnego występowania uracylu w RNA, w DNA zamiast niego występuje tymina. Dlaczego tak się dzieje?
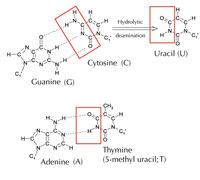
Zdjęcie dzięki uprzejmości Angéla Békési
Pod względem chemicznym, tymina to cząsteczka uracylu posiadająca dodatkową grupę metylową. Jaka korzyść, z ewolucyjnego punktu widzenia, mogłaby płynąć z obecności bardziej złożonego budulca w DNA? Odpowiedź może tkwić w sposobie, w jakim komórki naprawiają uszkodzenia DNA.
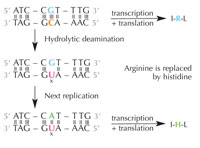
deamination of cytosine can
change the amino acids
encoded by the sequence.
Kliknij na obrazek aby
powiększyć
Zdjęcie dzięki uprzejmości
Nicola Graf
Cytozyna może spontanicznie przemienić się w uracyl w procesie zwanym deaminacją hydrolityczną (patrz rys. 4). W jego trakcie guanina, która początkowo związana była z cząsteczką cytozyny, znajduje się naprzeciw uracylu (pamiętaj, że uracyl zwykle łączy się z adeniną). W trakcie replikacji DNA przez komórkę, miejsce naprzeciw cząsteczki uracylu byłoby zajęte przez adeninę zamiast guaniny, która powinna się tam znajdować, zmieniając informację kodowaną przez ten fragment DNA (patrz rys. 5). Deaminacja cytozyny jest jednym z najczęstszych rodzajów uszkodzenia DNA, jednak w normalnych przypadkach jest ono skutecznie naprawiane. Jak komórki tego dokonują?
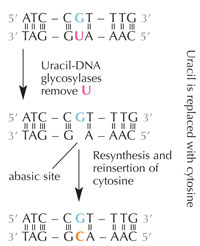
deaminacji hydrolitycznej.
Kliknij na obrazek aby
powiększyć
Zdjęcie dzięki uprzejmości
Nicola Graf
Komórki posiadają system naprawy, który wykrywa obecność uracylu w miejscu cytozyny i eliminuje błąd zanim zostanie on zreplikowany i przekazany dalej. System ten jest skomplikowany i składa się z kilku enzymów: najpierw glikozylazy uracylo-DNA rozpoznają uracyl i usuwają go z DNA. Następnie poszczególne enzymy pomagają w eliminacji i ponownej syntezie uszkodzonej części DNA, kiedy to miejsce AP (puste) w DNA zastąpione zostaje cytozyną (patrz rys. 6).
Jednak najpowszechniejsza forma glikozylazy uracylo-DNA nie rozpoznaje, z którą zasadą łączy się uracyl, tj. czy to właśnie uracyl miał się tam znaleźć (i połączyć z adeniną), czy jest to może zmutowana cytozyna (połączona z guaniną). Zamiast tego, rozpoznałaby i wycięła oba rodzaje uracylu. Spowodowałoby to oczywiście komplikacje. Wydaje się, że rozwiązaniem tego potencjalnego problemu był rozwój mechanizmu, w trakcie którego “właściwe” cząsteczki uracylu (połączone z adeniną) otrzymywały grupę metylową, zmieniając się w tyminę. Dzięki temu, jeśli system naprawczy komórki natrafiał na uracyl, wycinał go i naprawiał, lecz gdy znajdywał uracyl z metylowym oznaczeniem – tyminę (patrz rys. 4) – zostawiał go. Dlatego, z czasem, tymina stała się, w przeciwieństwie do uracylu, standardowym składnikiem DNA, a większość komórek wykorzystuje uracyl tylko w RNA.
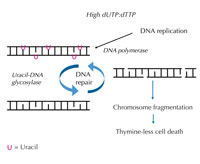
dUTP do dTTP wzrasta,
polimeraza DNA, zarówno w
trakcie replikacji, jak i
naprawy, często zamiast
tyminy przyłącza uracyl.
Glikozylaza uracylo-DNA
usuwa uracyl i rozpoczyna
dalszą naprawę, w trakcie
której dochodzi do
rozerwania łańcucha DNA.
Synteza naprawcza może
jednak na nowo wprowadzić
uracyl, co powoduje, że cykl
naprawczy DNA jest
nieudany. Doprowadza to do
przeciążenia całego systemu
i wystąpienia fragmentacji
chromosomów, co kończy się
śmiercią komórki. Kliknij na
obrazek aby powiększyć
Zdjęcie dzięki uprzejmości
Angéla Békési
Dlaczego uracyl został zatrzymany w RNA? RNA żyje krócej niż DNA i – poza nielicznymi wyjątkami – nie jest ono miejscem długotrwałego przechowywania informacji genetycznej. Cząsteczki cytozyny, które spontanicznie zamieniają się w uracyl, nie stanowią więc dużego zagrożenia dla komórki. Dlatego też, w trakcie ewolucji nie wystąpiła potrzeba zastąpienia uracylu w RNA bardziej złożoną (i prawdopodobnie wymagającą zużycia większej ilości energii) tyminą.
Śmierć komórki przy braku tyminy
W trakcie syntezy DNA, enzymy polimerazy DNA (katalizujące syntezę) nie potrafią odróżnić tyminy od uracylu. Weryfikują one jedynie, czy wiązania wodorowe powstają poprawnie, tj. czy pary zasad łączą się odpowiednio. Dla enzymów tych nie ma znaczenia czy to tymina, czy uracyl łączy się z adeniną. W normalnym przypadku, zawartość trójfosforanu deoksyurydyny (dUTP, źródło uracylu) w komórce jest bardzo niska w porównaniu do trójfosforanu deoksytymidiny (dTTP, żródło tyminy), co zapobiega włączeniu uracylu w trakcie syntezy DNA.
Jeśli ten ściśle określony proces zostanie zaburzony, a stosunek dUTP do dTTp wzrośnie, ilość uracylu, który został błędnie włączony także się zwiększy. System naprawczy – który, w przeciwieństwie do polimerazy DNA, odróżnia uracyl od tyminy – stara się wyciąć uracyl przy pomocy glikozylazy uracylo-DNA oraz ponownie zsyntezować DNA, co wiąże się z czasowym rozdzieleniem szkieletu DNA. Jednak, jeśli stosunek dUTP do dTTp jest ciągle wysoki, ponowna synteza może jeszcze raz przyłączyć uracyl zamiast tyminy. Gdy wymienione cięcia w DNA zdarzają się jedne po drugich i blisko siebie, cykl ten prowadzi do zerwania nici DNA i fragmentacji chromosomów (patrz rys. 7). Doprowadza to do specyficznej programowanej śmierci komórki, zwanej śmiercią komórki przy braku tyminy.
Proces umierania komórki przy braku tyminy może być wykorzystywany w leczeniu nowotworów. Ponieważ komórki nowotworowe namnażają się w tempie znacznie szybszym, niż normalne komórki, syntezują one większą ilość DNA w danym czasie i dlatego wymagają większej ilości dUTP. Zwiększając stosunek dUTP do dTTP, komórki te mogą być selektywnie wychwytywane i eliminowane.
Uracylo-DNA ciągle występuje
Mimo, iż w większości komórek w RNA występuje uracyl, a w DNA tymina, istnieją wyjątki. Niektóre organizmy posiadają zamiast tyminy uracyl w całym swoim DNA, a u jeszcze innych uracyl pojawia się tylko w części ich DNA. Jaka ewolucyjna korzyść może z tego płynąć? Przyjrzyjmy się niektórym przykładom.
Uracyl w wirusowym DNA
infekującego komórkę
bakteryjną
Zdjęcie dzięki uprzejmości
cdascher / iStockphoto
Jak odkryto, u dwóch rodzajów fagów (wirusów infekujących bakterie) występują genomy DNA posiadające jedynie uracyl, bez tyminy. Nie wiemy na razie, czy fagi te reprezentują pradawne formy życia które nigdy nie wykształciły DNA z tyminą, czy też ich genomy z podstawionym uracylem stanowią nowo wykształconą strategię. Nie wiemy także, dlaczego fagi te wykorzystują uracyl zamiast tyminy, choć może to odgrywać znaczącą rolę w ich cyklu życiowym. Jeśli tak jest, upewnienie się przez wirusy, że uracyl w ich DNA nie jest zastąpiony tyminą byłoby sensowne. U jednego z powyższych fagów dowiedzione zostało istnienie genu kodującego białko w celu zahamowania glikozylazy uracylo-DNA gospodarza, co powoduje zablokowaie 'naprawy' uracylu przez enzymy komórki.
Programowana śmierć komórki w cyklu życiowym owadów

Endopterygota, jak np.
mrówki, nie posiadają
enzymu zdolnego do
usuwania uracylu z ich DNA
Zdjęcie dzięki uprzejmości
spxChrome / iStockphoto i
Nicola Graf
DNA wyposażone w uracyl wydaje się także odgrywać rolę w rozwoju Endopterygota – owadów, w których cyklu życiowym występuje stadium larwalne (mrówki i motyle; w przeciwieństwie do koników polnych i termitów). Owady te nie posiadają głównego genu kodującego glikozylazę uracylo-DNA, który mógłby usunąć uracyl z ich DNA.
Co więcej, nasze własne badanie wykazało, że u larwy muszki owocowej (Drosophila melanogaster) współczynnik dUTP do dTTP jest regulowany w osobliwy sposób: we wszystkich tkankach, które nie będą potrzebne u dorosłego owada, poziom enzymu, który hamuje dUTP i wytwarza prekursor dTTP, jest znacznie niższy. W rezultacie pokaźne ilości uracylu zostają włączone do ww. tkanek w trakcie syntezy DNA.
Tak więc w stadium larwalnym wytwarzane jest uracylo-DNA, które nie jest korygowane w przypadku tkanek mających ulec zniszczeniu w trakcie tego stadium. Jako, że owady te nie posiadają głównego enzymu glikozylazy uracylo-DNA, w okresie larwalnym dodatkowe czynniki specyficzne dla uracylo-DNA mogą zidentyfikować skumulowany uracyl jako sygnał do zainicjowania śmierci komórki. Udało się nam wyodrębnić białko specyficzne dla owadów, które może niszczyć uracylo-DNA, a dalsze nasze badania mają na celu sprawdzenie, czy enzym ten wykorzystywany jest do zainicjowania programowanej śmierci komórki.

sekwencjach genu
przeciwciała wywołuje
odpowiedź naprawczą DNA,
w wyniku której wzrasta
różnorodność białek
przeciwciała. Kumulacja
przeciwciał zwiększa szanse
na rozpoznanie niechcianych
intruzów przez układ
odpornościowy
Zdjęcie dzięki uprzejmości
taramol / iStockphoto
Dobroczynne błędy: układ immunologiczny kręgowców
Uracylu w DNA nie trzeba jednak szukać tak daleko – można go znaleźć w układzie immunologicznym kręgowców, do których sami należymy. Część naszego układu immunologicznego – adaptacyjny układ odpornościowy – wytwarza dużą ilość różnych przeciwciał wyspecjalizowanych do obrony przed patogenami swoistymi. W celu zwiększenia liczby różnych przeciwciał, jakie można wytworzyć, mieszamy sekwencję DNA w rejonach odpowiedzialnych za ich kodowanie, nie tylko poprzez rekombinację istniejących w komórce sekwencji, lecz także poprzez tworzenie nowych w procesie zwanym hipermutacą.
Hipermutacja rozpoczyna się przy użyciu swoistego enzymu AID (ang. Activation-Induced Deaminase), który w swoistych loci DNA przemienia cytozynę w uracyl (patrz rys. 4), wywołując reakcję naprawczą podatną na błędy, co działa na korzyść organizmu: 'błędy' generują nowe sekwencje, które mogą być wykorzystywane w wytwarzaniu innych przeciwciał. System ten jest ściśle regulowany, jednak utrata kontroli nad nim mogłaby prowadzić do powstania nowotworu.
Rozważając kwestię uracylu i tyminy, powinniśmy uwzględnić kontekst ewolucyjny. Organizmy żywe rozwijały się w nieustannie zmieniającym się środowisku, stawiając czoła różnego rodzaju wyzwaniom. Dlatego też rozwiązania, które zapobiegają błędom w strukturze DNA, są korzystniejsze dla większości organizmów i komórek. Tłumaczy to, dlaczego to tymina w DNA stała się normą. W pewnych okolicznościach, 'pomyłki' mogą być pożyteczne, co tłumaczy obecność uracylu w DNA niektórych komórek.
Resources
- Aby dowiedzieć się więcej o dokonaniach grupy badawczej Beáty Vértessy, odwiedź: www.enzim.hu/~vertessy
- Aby pobrać streszczenie pracy doktorskiej Villő Muhy, dotyczącej uracylu w DNA u Drosophila melanogaster, napisanej pod kierunkiem Beáty Vértessy, użyj poniższego linku: http://teo.elte.hu/minosites/tezis2010_angol/v_muha.pdf
-
Pełna wersja pracy dostępna jest tutaj: http://teo.elte.hu/minosites/ertekezes2010/muha_v.pdf
-
Review
Artykuł pokazuje, że nauka nigdy nie zasypia, czego dowodem jest obalenie przekonania o istnieniu uracylu tylko w strukturach RNA. Jak wynika z artykułu, nie zawsze jest to prawdą. A nawet jeśli jest, dlaczego nie miało by się to zmienić?
Aby pomóc uczniom w zrozumieniu artykułu, można wykorzystać następujące pytania:
- Opisz strukturę wiązań pomiędzy dwoma komplementarnymi parami zasad w DNA.
- Która z zasad zostaje zastąpiona w RNA?
- Opisz i narysuj wykres inicjowanego w momencie wykrycia uracylu w DNA szlaku enzymu naprawiającego.
- Stosunek jakich cząsteczek może być wykorzystywany do powstrzymania rozwoju i podziału komórek nowotworowych?
- Dlaczego uracyl jest 'tolerowany' w RNA?
- Które organizmy żywe wykorzystują uracyl w DNA i w jaki sposób?
Friedlinde Krotscheck, Austria





