Il limoncello e la scienza delle emulsioni Understand article
Come si fa a mescolare olio e acqua?La curiosità di uno scienziato su un liquore al limone, ha rivelato come farlo con alcune promettenti applicazioni industriali.

Jorge Royan/Wikimedia Commons, CC BY-SA 3.0
Il limoncello, il profumato liquore italiano fatto con i limoni, sta diventando sempre più famoso in tutto il mondo. Questo dolce digestivo agli agrumi è un prodotto icona della cultura gastronomica italiana ma è anche un complesso sistema colloidale fatto di oli essenziali, etanolo, saccarosio e acqua.
Mentre lavoravo come chimico italiano presso l’Istituto Laue-Langevin (ILL) w1 , ero curioso di scoprire cosa avrebbe rivelato la tecnologia avanzata dell’ILL a proposito di questo complesso sistema. Così, all’inizio di quest’anno, io e i miei colleghi abbiamo fatto domanda per il beamtime per svolgere un piccolo studio, ed è emerso che oltre a essere delizioso , il limoncello possiede alcune caratteristiche scientifiche piuttosto particolari.
Cos’è il limoncello?
Nella tradizionale ricetta del limoncello, la scorza di agrumi (ottenuta raschiando la parte esterna della buccia del limone) è macerata nell’alcool (etanolo) per diverse settimane. La scorza contiene la maggior parte degli olii essenziali nei limoni e produce il caratteristico sapore e colore del liquore. L’etanolo e l’estratto di limone vengono poi mescolati con uno sciroppo di zucchero. Il limoncello contiene tipicamente circa il 30% di alcool e circa il 20% di saccarosio (zucchero) per volume ma dato che il limoncello è spesso fatto in casa, il metodo di preparazione e la composizione finale varia da famiglia a famiglia.
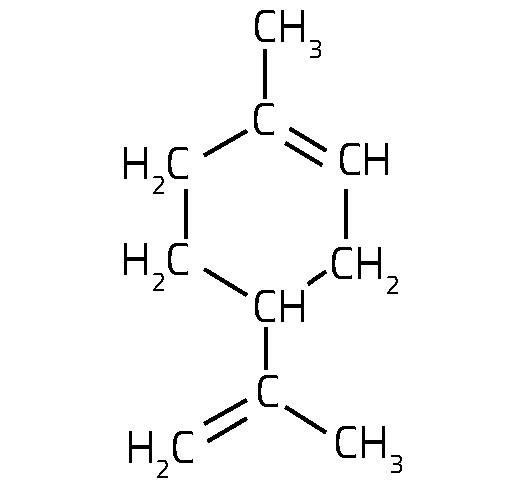
limonene
Nicola Graf
Gli oli essenziali che conferiscono un sapore così forte al limoncello si trovano nelle piccole tasche della buccia degli agrumi, che esplode e libera quel forte tipico sentore che avvertiamo quando sbucciamo questo frutto. Questi oli essenziali hanno una composizione molto complessa: sono state identificate più di 60 molecole differenti, delle quali i componenti principali sono costituiti da una classe di molecole organiche dette monoterpeni. Nei limoni, il composto più abbondante è il limonene (immagine 1).
Il limoncello viene preparato mescolando due soluzioni: l’estratto etanolico che contiene gli oli e la soluzione acquosa di saccarosio. Ciascuna di queste soluzioni iniziali è completamente trasparente; il limoncello in sè, tuttavia è “torbido”, con un aspetto opaco e melmoso. I sistemi torbidi sono presenti nella vita di tutti i giorni: altri esempi sono i cristalli di ghiaccio nelle nuvole, le goccioline grasse nel latte e le alghe nello stagno. Tutti questi diversi sistemi contengono tutti particelle o goccioline della scala di centinaia di nanometri, che è paragonabile alla lunghezza d’onda della luce visibile. Sono queste “eterogeneità”, piccole quantità di solido o liquido sospeso in un mezzo fluido che dà a questi sistemi l’aspetto torbido.
L’effetto ouzo
Quindi, da dove proviene questa torbidità del limoncello? L’acqua e l’etanolo sono completamente miscibili (solubili l’un l’altro) come lo sono il limonene e l’etanolo ma il limonene e l’acqua lo sono appena. Nel limoncello, questa combinazione di tre liquidi produce spontaneamente una “emulsione”: una sospensione di minuscole goccioline di un liquido nell’altro. Tuttavia, questo accade in alcuni specifici intervalli di composizione (vedi casella di testo).
Questo fenomeno di formazione spontanea di emulsioni è detto “effetto ouzo”, dal nome del famoso liquore chiamato ouzo che diventa subito torbido quando viene mescolato con l’acqua, formando un’emulsione. Infatti, l’ouzo è, da un punto di vista scientifico, abbastanza simile al limoncello, poichè è fatto con acqua, etanolo e il componente aromatizzante, l’anetolo, che come il limonene è altamente solubile nell’etanolo ma solo leggermente solubile in acqua.

canbilgic/Shutterstock.com
In contrasto con questi sistemi ouzo, le emulsioni tipiche richiedono un input energetico molto elevato come lo shakerare o il mescolare per produrre l’emulsione che noi chiamiamo maionnese. Un’altra differenza molto importante fra i sistemi ouzo e le emulsioni classiche è l’assenza di qualsiasi agente stabilizzante. Ad esempio, la maionnese è preparata emulsionando un olio vegetale con l’acqua contenuta in un tuorlo d’uovo. Il procedimento è lungo e noioso e richiede una quantità sostanziale di energia fornita da un vigoroso shekerare e mescolare per far sì che la miscela dei due liquidi produca l’emulsione. La lecitina e le proteine contenute nel tuorlo d’uovo sono altresì necessarie per stabilizzare l’emulsione.
Quindi perchè i sistemi ouzo sono importanti al di fuori della cucina? Alcuni processi industriali hanno luogo nelle emulsioni, per esempio, la polimerizzazione, nella quale delle piccole molecole (monomeri) si combinano per formare delle grandi macromolecole o polimeri. Qui, le emulsioni sono spesso prodotte per portare i reagenti nelle immediate vicinanze affinchè la reazione possa procedere velocemente. Se le emulsioni di questo tipo si formano spontaneamente (come nel limoncello) richiedendo un piccolissimo apporto energetico, se presente, ciò rende il procedimento più efficiente e sostenibile. Inoltre, il prodotto polimerico deve essere recuperato dal mezzo di reazione al termine della reazione, che è spesso il passo più difficile dell’intero processo. Tuttavia, se il sistema non contiene stabilizzatori, l’estrazione del polimero e dei catalizzatori è molto più semplice, dato che i componenti si possono separare facilmente una volta che l’emulsione-la composizione che si sta formando non esiste più. Un’altra applicazione di emulsioni usata largamente è nei pesticidi, per consentire a questi prodotti insolubili in acqua di essere diluiti e sparsi sui terreni. Utilizzando un emulsione di tipo ouzo eviterebbe anche di spargere tensioattivi, che sono spesso dannosi per l’ambiente.
Il limoncello al microlivello

utilizzato per lo studio del limoncello.
A Chezière/ILL
Come accennato, il modo in cui il limoncello disperde la luce rivela abbastanza bene la struttura del liquido a livello microscopico. Utilizzando la radiazione di una lunghezza d’onda più corta, i raggi X o i fasci di neutroni ci permettono di guardare più al dettaglio le strutture e le interazioni all’interno di questo liquido e a una scala persino più piccola.
Speravamo di usare gli impianti di diffusione dei neutroni presso l’ILL per capire cosa avrebbero potuto dirci sul limoncello e fortunatamente ci è stato assegnato del tempo sulla linea di diffusione dei nuetroni ad angolo piccolo ( detti SANS). Il proposito della nostra ricerca era di scoprire da dove proviene la straordinaria stabilità del limoncello. A questo fine, abbiamo studiato il liquore in condizioni diverse: quando l’acqua è aggiunta all’estratto etanolico; in diverse temperature; e a diverse concentrazioni di saccarosio (Chiappisi & Grillo, 2018). I neutroni sono sensibili alla composizione isotopica del sistema, e interagiscono molto diversamente con i due isotopi stabili dell’idrogeno: protio, 1H (idrogeno normale) e il più raro deuterio, 2 H. Nella ricerca, l’olio essenziale è stato estratto da un limone acquistato nel mercato locale (contenente quindi nuclei di protio), mentre l’etanolo e l’acqua sono stati invece arricchiti molto dai nuclei di deuterio.
L’analisi ha rivelato che, nel limoncello, la misura dei domini ricchi di olio si aggira sempre attorno ai 100 nanometri di diametro, a prescindere dal contenuto di acqua, di zucchero o di temperatura. Questi risultati sono sorprendenti: la tipica dimensione dei domini ricchi di olio nei sistemi ouzo è normalmente più grande, di parecchie centinaia o persino migliaia di nanomentri di dimensione (Grillo, 2003). Inoltre la loro dimensione è di solito molto sensibile alla composizione o la temperatura del sistema diversamente dal limoncello.
Questo rende il limoncello un liquido molto interessante a livello scientifico. La dimensione piccola delle goccioline di olio sembra fornire la sua eccezionale stabilità in rapporto ai cambiamenti di temperatura e composizione e anche nel tempo. Infatti, il limoncello può essere conservato nella bottiglia per anni: non è così male per un sistema metastabile! Invece, le bevande come il pastis o l’ouzo tendono a separare la fase entro poche ore di preparazione (motivo per il quale il pastis è sempre diluito con l’acqua nel bicchiere appena prima della consumazione).
Quindi mentre non comprendiamo appieno perchè il limoncello agisce in modo così diverso rispetto agli altri liquori di tipo ouzo, abbiamo adesso una maggiore comprensione della scienza dei sistemi autoemulsionanti e come progettarli per l’uso nei prodotti e processi futuri.
I diagrammi fase e la stabilità del limoncelllo
I diagrammi fase sono un modo conveniente di rappresentare gli stati fisici in mutamento dei sistemi di due o più componenti in condizioni diverse. Una tipologia comune di diagrammi fase mostra come un’unica sostanza (come l’acqua, ad esempio) cambierà lo stato fra solido, liquido e gassoso in diverse combinazioni di temperatura e pressione (immagine 2)
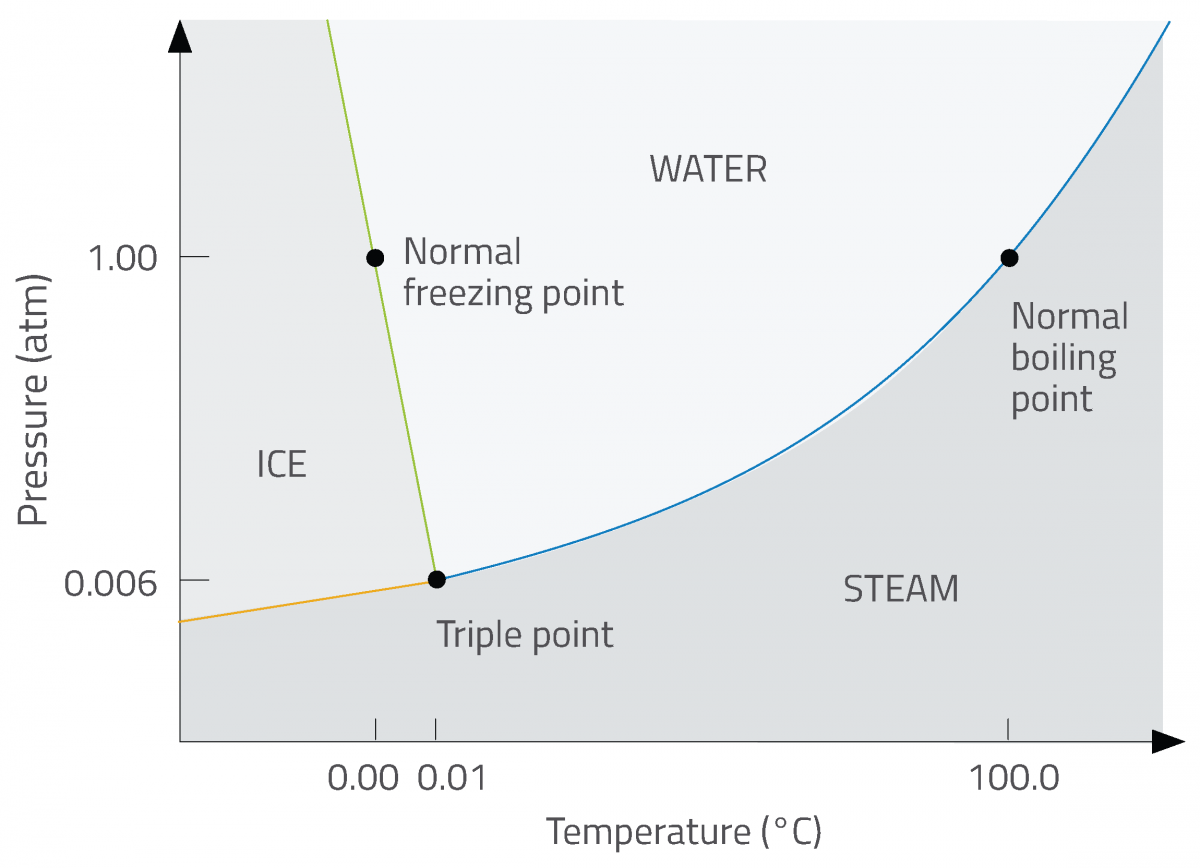
Nicola Graf/Leonardo Chiappisi
Nei sistemi come il limoncello, che è fatto di tre componenti (acqua, etanolo e olio essenziale), i diagrammi fase ci permettono di rappresentare le possibili composizioni all’interno del sistema e le caratteristiche fisiche (come la solubilità e la stabilità) associata a ciascuna composizione. Un tipico diagramma di fase triplo è rappresentato nell’immagine 3. Qui, ciascuno dei componenti puri è rappresentato da un vertice del triangolo principale dove le scale adiacenti leggono il 100% e lo 0% per due componenti diversi.
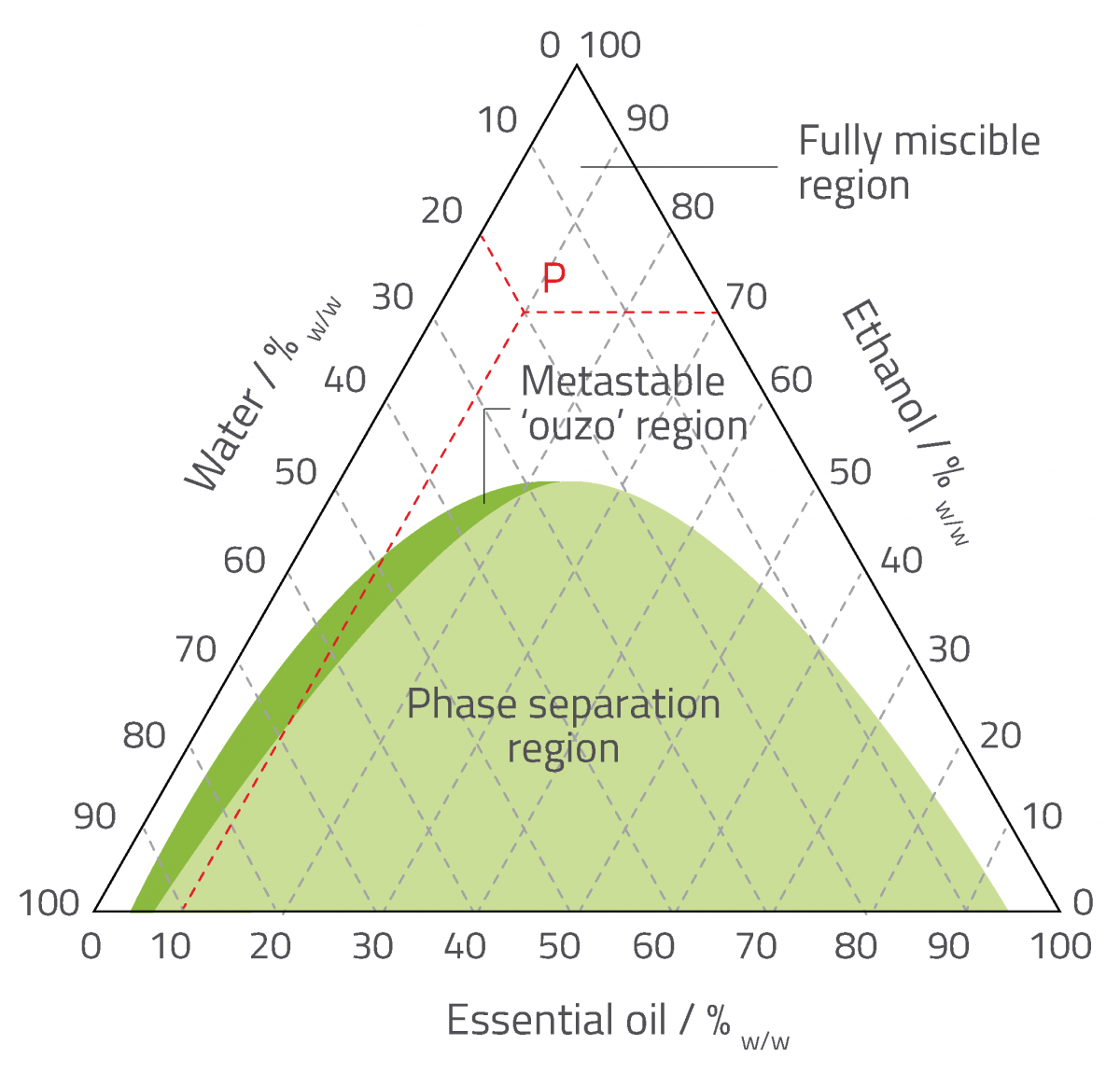
che rappresenta un sistema ouzo
Nicola Graf/Leonardo Chiappisi
Come illustrano gli esempi, la composizione di un punto all’interno del diagramma di fase può essere letto disegnando tre linee che iniziano dal punto e terminano a ogni asse ( notare la griglia triangolare usata per disegnare le linee). In questo caso, un campione rappresentato dal punto rosso P avrà una composizione formata dal 20% di acqua, 70% di etanolo e dal 10% di olio essenziale (w/w).
Da questo diagramma di fase, possiamo vedere che l’acqua e l’etanolo sono completamente mescolabili, così come lo sono l’etanolo e l’olio essenziale. Tuttavia, la solubilità dell’olio essenziale nell’acqua è di solo 5% w/w e la solubilità dell’acqua nell’olio essenziale è inferiore al 10%. Il digramma mostra inoltre un’area nella quale i componenti si separano in almeno due fasi e non si mescolano (la regione di separazione di fase). La piccola “regione ouzo metastabile” è presente dove la composizione consente la formazione spontanea di emulsione come è stato trovato nei sistemi ouzo. La separazione di fase avverrà finalmente in questa regione, ma lo scadenziario può essere molto lungo perchè lo stato metastabile richiede energia da superare.
References
- Chiappisi L, Grillo I (2018) Looking into Limoncello: the structure of the Italian liquor revealed by small-angle neutron scattering. ACS Omega 3: 15407-15415. doi: 10.1021/acsomega.8b01858
- Grillo I (2003) Small-angle neutron scattering study of a world-wide known emulsion: Le Pastis. Colloids and Surfaces A: Physicochemical and Engineering Aspects 225: 153-160. doi: 10.1016/S0927-7757(03)00331-5
Web References
- w1 – Con sede a Grenoble, Francia, l’ILL è un centro di ricerca internazionale all’avanguardia nella scienza e tecnologia dei neutroni.
Resources
- Lo studio della struttura microscopica del limoncello è stato condotto utlizzando lo strumento SANS D11 presso l’ILL. Impara a usare questo strumento sul sito dell’ILL.
- Scopri di più sul funzionamento dello scattering di neutroni attraverso un articolo dell’ILL su uno studio che riguarda come alcuni batteri riescano a vivere negli ambienti marini salini. Vedi:
- Zaccai G (2018) Titanic and the iron-eating bacteria. Science in School 43: 8-11.
- Leggi come SANS è stato usato per sviluppare une nuovo, recuperabile tensioattivo presso l’ILL. Vedi:
- Eastoe J et al. (2012) Magnetic science: developing a new surfactant. Science in School 25: 22-27.
Institutions
Review
La maggior parte degli studenti riconosceranno che l’olio e l’acqua non si mescolano e avranno potuto sentire la parola “emulsione” quando hanno aiutato un familiare a dipingere una stanza; ma nonostante questi esempi tratti dal mondo reale, pochissimi avranno messo in discussione la chimica dietro queste esperienze. Incoraggiando gli studenti a chiedersi cosa sia successo a livello macro e ispirandoli con la chimica che avviene a livello micro, questo articolo fornisce un portale accessibile ad alcuni concetti fondamentali.
Inoltre, esiste un’opportunità per interpretare un diagramma fase triplo che consente agli studenti di usare le loro competenze matematiche per trarre conslusioni sulle caratteristiche fisiche dimostrando che tali abilità sono essenziali per la ricerca scientifica.
Alcune domande di comprensione che possono essere utlizzare in classe sono:
- La molecola di limonene ha due possibili enantiomeri. Identifica l’atomo di carbonio chirale.
- Quale volume di etanolo ti aspetti che contenga 5 litri di limoncello?
- I sistemi torbidi contiene particella su una scala paragonabile alla lunghezza d’onda della luce visibile. Qual è il campo di misura della lunghezza d’onda della luce visibile?
- Per quale motivo la scienza del limoncello si rivela utile per progettare sistemi auto emulsionanti?
- Il diagramma fase contiene una “regione ouzo metastabile”. Cosa si intende con il termine “metastabile”?
Caroline Evans, capo del dipartimento di chimica, Wellington College, Regno Unito





