Più veloce, più economica, più incisiva. È CRISPR, la nuova rivoluzione dell’ingegneria genetica Understand article
Tradotto da Cristina Florean. Una nuova e molto discussa tecnologia sta rendendo la manipolazione genetica sempre più abbordabile e facile- troppo facile, forse?

concessione di Nicola Graf
Mentre stai digitando una frase, ti rendi conto di un errore di battitura. Dato che l’errore altera il significato della frase, dirigi il cursore sulla lettera sbagliata, premi il tasto backspace e inserisci il carattere corretto. È qualcosa di estremamente facile. Per quanto incredibile, questo semplice approccio sta venendo ormai usato anche nei laboratori, dove gli scienziati svolgono il ruolo di scrittori e il DNA è il messaggio che viene modificato.
Questa è la realtà offerta da CRISPR-Cas9, una nuova tecnica che ha preso d’assalto la comunità scientifica negli ultimi anni. Oltre a rendere possibili degli importanti progressi in campo biomedico, essa solleva alcuni difficili problemi. I mezzi di comunicazione hanno già discusso tanto di questa controversa tecnica che gli insegnanti di scienze potrebbero presto sentirsi porre delle domande a proposito di CRISPR-Cas9 dai loro studenti. Ecco qui una guida rapida a CRISPR-Cas9 e alle ragioni della sua importanza.
Che cos’è CRISPR-Cas9?
CRISPR-Cas9 è un sistema di difesa usato dai batteri contro gli attacchi dei virus. Recentemente tale sistema è stato utilizzato come tecnica per tagliare il genoma in punti precisi. Il sistema comprende due elementi: CRISPR e Cas9. CRISPR è l’acronimo di “clustered regularly interspaced short palindromic repeats”, ossia “brevi ripetizioni palindrome raggruppate e separate a intervalli regolari”, e si riferisce a delle posizioni in un genoma in cui la sequenza di DNA è ripetuta. Vicino a tali ripetizioni si trovano i geni Cas, che codificano per importanti enzimi del sistema. Uno di questi, Cas9, è una nucleasi, ossia un enzima che taglia gli acidi nucleici (DNA o RNA).
Quando un virus attacca un batterio, inietta in esso il suo acido nucleico. Il batterio risponde producendo enzimi Cas, per tagliare pezzi del genoma virale e incorporarli nel proprio genoma alla posizione CRISPR (figura 1). Ciò fornisce al batterio una vantaggiosa immunità acquisita: al successivo attacco della stessa specie di virus, la sequenza CRISPR e quella dell’acido nucleico virale sono trascritte in brevi molecole di RNA. Queste in un primo tempo si legano all’enzima Cas9, poi guidano il complesso risultante verso l’acido nucleico invasore, identificandolo per appaiamento di sequenza. In seguito Cas9 taglia l’acido nucleico bersaglio, rendendo il virus incapace di servirsi del batterio per la sua replicazione.
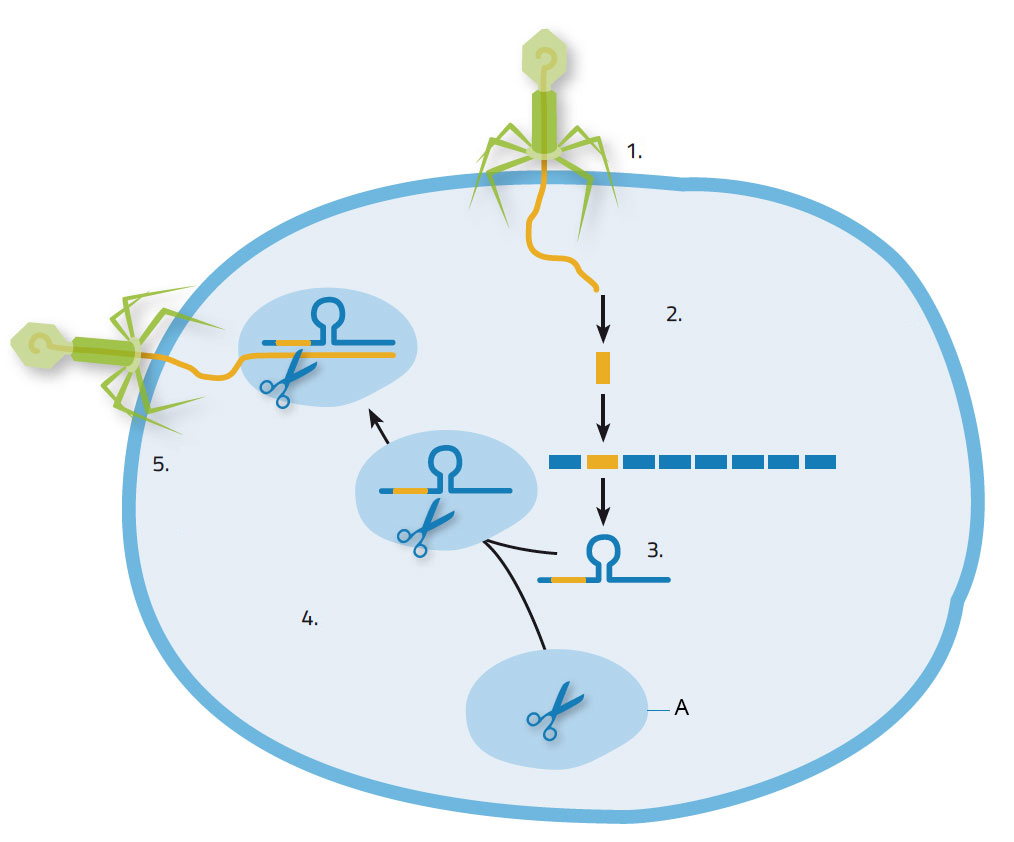
1.Un virus invade una cellula batterica; 2.Un acido nucleico derivato dal virus è integrato nell’acido nucleico del batterio in una posizione CRISPR; 3. Si forma un RNA CRISPR; 4. L’RNA CRISPR si attacca all’enzima Cas9; 5. L’RNA CRISPR dirige l’enzima Cas9 verso il virus, dove esso taglia e distrugge il genoma virale.
Immagine per gentile concessione di Nicola Graf
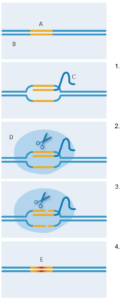
genoma per mezzo di
CRISPR-Cas9. A: Sequenza
bersaglio; B: DNA; C: RNA
guida; D: Cas9; E: Nuova
sequenza di DNA
1. L’RNA guida si lega alla
sequenza DNA bersaglio;
2. L’enzima Cas9 si lega
all’RNA guida: 3. L’enzima
Cas9 taglia entrambi i
filamenti di DNA; 4. Il sistema
di riparazione batterico
introduce un nuovo DNA al
sito di rottura dei filamenti,
sostituendo la sequenza di
DNA originale.
Immagine per gentile
concessione di Nicola Graf
Vediamo in che modo questo sistema batterico è stato modificato in modo da far nascere una nuova tecnologia della genetica. Nel 2012, il team di Jennifer Doudna all’Università di California Berkeley, negli USA, e Emmanuelle Charpentier, allora all’Università Umea in Svezia, hanno modificato e messo insieme le piccole molecole di RNA in un singolo “RNA guida” (figura 2). Esso conserva un’estremità capace di legarsi a Cas9, ma la sequenza all’altra estremità può essere modulata in modo da appaiarsi a qualsiasi sequenza bersaglio nota. Grazie a questa capacità di adattamento, CRISPR-Cas9 può tagliare specificamente sequenze di DNA a scelta. Poco tempo dopo, il laboratorio di Feng Zhang all’Istituto di Tecnologia del Massachusetts ha ulteriormente sviluppato CRISPR-Cas9, rivelandone la capacità di indurre tagli precisi nel genoma di cellule umane e di topo (Cong et al, 2013). Inoltre, il gruppo ha modificato Cas9 in modo da tagliare il DNA in un modo leggermente diverso, stimolando uno specifico meccanismo di riparazione del DNA nelle cellule. Ciò significa che i ricercatori sono riusciti ad inserire con successo una nuova sequenza di DNA precisamente nel sito di taglio, sostituendo la sequenza di origine (figura 2).
Grazie a questi sforzi pioneristici, un argomento di nicchia della microbiologia come CRISPR-Cas9 è stato trasformato in un interessante strumento di ricerca, che permette ai ricercatori di modificare i geni per diversi scopi, con grande facilità e specificità.
A cosa serve?
Per studiare la funzione di un gene, spesso gli scienziati provano a produrre linee cellulari o organismi modello nei quali il gene d’interesse è mutato o inattivato (una tecnica nota come knockout di un gene). CRISPR-Cas9 permette di farlo rapidamente e con precisione. Inoltre, l’enzima Cas9 può essere modificato in modo da perdere l’abilità di tagliare il DNA, mantenendo quella di riconoscere e legare specifiche sequenze di DNA. Ciò ha l’effetto di impedire il legame della RNA polimerasi al DNA, permettendo agli scienziati di controllare la trascrizione genica (il punto di partenza dell’attività di un gene).
Oltre a queste pratiche, fondamentali per la ricerca biomedica, CRISPR-Cas9 promette anche applicazioni più dirette in campo medico. Gli scienziati hanno già usato la manipolazione genetica via CRISPR-Cas9 per tagliare sequenze dell’ HIV, così da impedirgli di replicarsi in cellule umane. La tecnica è stata usata anche per rimuovere sequenze mutate in topi afflitti dalla distrofia muscolare di Duchenne, una malattia che causa debolezza muscolare, dando speranza terapeutica ai pazienti e alle famiglie che soffrono di questa e di simili malattie genetiche. Recentemente, degli embrioni di maiale sono stati modificati geneticamente usando CRISPR-Cas9, con la speranza di ottenere organi più sicuri per il trapianto nell’uomo.
Il fatto che tali manipolazioni siano state eseguite su embrioni di maiale, porta a pensare che possano esserlo anche su embrioni umani. Questo è precisamente quello che alcuni ricercatori cinesi hanno fatto nel 2015, quando hanno usato CRISPR-Cas9 per modificare il gene della β-talassemia in 86 embrioni umani (Cyranoski & Reardon, 2015). La tecnica si è rivelata piuttosto inefficace, dato che la sequenza di DNA è stata modificata in meno di un quarto degli embrioni. In ogni caso, l’annuncio di questi dati ha generato molta discussione per le loro implicazioni etiche.
Questioni etiche… e il futuro
Le preoccupazioni etiche riguardano non solo gli esperimenti sugli embrioni umani, ma anche l’inquietante prospettiva di modificazioni genetiche nelle cellule germinali. Con CRISPR-Cas9 è in teoria possibile effettuare delle modificazioni genetiche nelle cellule germinali (spermatozoi e cellule uovo), che possono quindi essere trasmesse alle generazioni successive. Anche se ciò potrebbe permettere di eradicare le malattie genetiche, porta anche a chiedersi quali modifiche debbano essere permesse in futuro come trattamento medico. Possono essere considerati appropriati per trattamento medico dei caratteri quali l’intelligenza o il colore degli occhi? Queste possono sembrare paure improbabili, ma c’è un’altra preoccupazione: che le modifiche ai geni delle cellule germinali possano avere effetti completamente imprevisti e irreversibili sulle generazioni future. Ciò è particolarmente rilevante, dato che recenti ricerche hanno scoperto che le interazioni tra la genetica e altri meccanismi ereditari sono molto più complesse di quanto si pensasse in precedenza.
Queste implicazioni non sono sfuggite all’attenzione degli scienziati. Alcuni sono d’accordo nel dire che l’ingegneria genetica delle cellule germinali è un terreno minato, e credono che ogni tipo di ricerca che usi CRISPR-Cas9 su embrioni umani debba essere arrestata. Altri, invece, credono che una moratoria assoluta sarebbe non solo difficile da far rispettare, ma ostacolerebbe anche i progressi della ricerca. Nonostante questi punti di vista differenti, la comunità scientifica sembra avere adottato la via del dialogo e della trasparenza, come si evidenzia dai molti convegni e conferenze su questo tema in tutto il mondo.
Nel frattempo, lo sviluppo di CRISPR-Cas9 continua ad avanzare. Alcune aziende farmaceutiche stanno investendo in questa tecnologia, per supportare la ricerca verso lo sviluppo di nuovi farmaci, e alcuni difetti tecnici stanno venendo affrontati e migliorati- mentre un’amara disputa sul brevetto si sta svolgendo tra i pionieri della tecnica (Doudna/Charpentier e Zhang). A prescindere da chi l’avrà vinta, l’ascesa meteorica di CRISPR-Cas9 è solamente al suo inizio.
References
- Cong L et al. (2013) Multiplex genome engineering using CRISPR/Cas systems. Science 339: 819–23. doi: 10.1126/science.123
- Cyranoski D, Reardon S (2015) Chinese scientists genetically modify human embryos. Nature 22 April, doi:10.1038/nature.2015.17378
Resources
- Leggi di più sui potenziali usi di CRISPR per modificare l’RNA.
- Leggi di più sulla disputa per il brevetto riguardante la tecnologia CRISPR-Cas9.
- Informati su come la tecnologia CRISPR-Cas9 può venire usata per trattare la distrofia muscolare di Duchenne.
- Leggi su come CRISPR-Cas9 è usata per produrre organi di maiale trapiantabili nell’uomo.
- Leggi un articolo abbordabile sulle questioni etiche delle modificazioni geniche in cellule germinali.
- Per un articolo con commenti di genetisti di livello internazionale sulle questioni etiche delle modificazioni geniche in cellule germinali, vedi:
- Bosley K et al. (2015) CRISPR germline engineering – the community speaks. Nature Biotechnology 33: 478–86
- Leggi di più sulla rivoluzionaria tecnica per modificare i geni di Emmanuelle Charpentier, e ascoltala mentre discute del suo lavoro.
Review
CRISPR-Cas9 è uno potente strumento per modificare i geni con la precisione di un GPS. Ha il potenziale di aprire le porte a molte applicazioni scientifiche, mediche e agricole. La relativa semplicità e il basso costo della tecnica sollevano questioni etiche importanti. La tecnica ha anche suscitato una battaglia legale tra scienziati sui preziosi diritti per il brevetto.
L’articolo descrive chiaramente l’identificazione delle ripetizioni palindrome come sistema di difesa batterico di base, nella sua applicazione al sistema riprogrammabile di modificazione genica CRISPR-Cas9. L’articolo può essere usato, con le relative animazioni, per spiegare le tecniche di biologia molecolare coinvolte, e i motivi per cui CRISPR-Cas9 abbia sostituito i metodi di ingegneria genetica preesistenti. Può anche fornire una base di discussione sulle questioni etiche riguardanti le modificazioni genetiche delle linee germinali, e sulla proprietà intellettuale. Domande per la verifica della comprensione dell’articolo potrebbero includere:
- Cosa significa CRISPR?
- Come funziona CRISPR-Cas9?
- Che tipo di malattie potrebbero venire curate usando CRISPR-Cas9?
- Quali sono i potenziali rischi dell’uso di CRISPR-Cas9?
- Quali sono le questioni etiche riguardanti l’uso di CRISPR-Cas9?
- Chi dovrebbe ricevere il premio Nobel per la scoperta di CRISPR-Cas9?
Mary Brenan, Concord College, UK





