Idrogeno, il vettore energetico verde del futuro? Understand article
Tradotto da Paolo Sudiro. L’idrogeno potrebbe essere il carburante del futuro, ma come possiamo produrlo in modo sostenibile? Ce lo spiega Karin Willquist.

concessa da janeff /
iStockphoto
L’idrogeno è stato chiamato il “vettore energetico del futuro” – perché può venire ossidato in una cella a combustibile per produrre elettricità, per esempio per alimentare le automobili, senza rilasciare anidride carbonica (CO2) e può venire prodotto in località remote prive di un’infrastruttura elettrica. Diversamente dalle risorse disponibili come gas naturale e benzina, l’idrogeno deve essere prodotto, rendendolo un vettore di energia e non un combustibile.
Un sistema energetico nel quale si impiega l’idrogeno per distribuire l’energia – un’economia all’idrogeno – venne proposto da John Bockris nel 1970; nel 1977 venne stipulato un accordo internazionale per l’applicazione dell’idrogeno, con l’obiettivo di lavorare al raggiungimento di tale obiettivow1.
L’idrogeno viene utilizzato principalmente come reagente chimico, piuttosto che come vettore di energia, ma non c’è dubbio che abbia il potenziale per trasformare i nostri sistemi di trasporto ed energetici. Comunque, rilasciare il suo potenziale non è facile. Molti carburanti attualmente in uso sono liquidi, solidi o gassosi, con un’elevata resa di energia per volume (densità di energia). L’idrogeno, al contrario, ha una bassa densità di energia: a parità di pressione, bruciare un litro di idrogeno produce un terzo del’energia che si ottiene bruciando un litro di metano. Questo pone problemi di immagazzinamento, distribuzione e utilizzo che vengono attualmente affrontati dagli scienziati (Schlapbach & Züttel, 2001)w2. Una sfida più fondamentale, comunque, è quella di produrre l’idrogeno in modo sostenibile. Su questo mi concentrerò in questo articolo.

alimentati con celle a
combustibile a idrogeno
Immagine gentilmente
concessa da Felix O; fonte
dell’immagine: Flickr
Metodi di produzione dell’idrogeno
L’idrogeno è un elemento abbondante sulla superficie terrestre, normalmente legato al carbonio nel carboidrati (nelle piante), o all’ossigeno nell’acqua (H2O). L’idrogeno gassoso (H2), al contrario, esiste solo in piccole quantità sulla Terra. Una delle sfide per la produzione sostenibile di idrogeno è la rottura dei legami che H2 forma con carbonio e ossigeno.
Attualmente H2 viene prodotto soprattutto da combustibili fossili (ad esempio il gas naturale), per mezzo della reazione di sintesi con vapore: scaldando i combustibili ad alta temperatura con acquaw2:
CH4 + H2O → CO + 3H2 (1)
CO + H2O → CO2 + H2 (2)
Questo metodo, comunque, si basa su combustibili fossili e rilascia CO2, provocando gli stessi problemi di emissioni della combustione dei carburanti fossili. La reazione di sintesi con vapore è sostenibile solo se vengono utilizzati idrocarburi rinnovabili, come il biogas, poiché la CO2 rilasciata è stata prima assorbita nella produzione degli idrocarburi.
H2 può venire prodotta anche per elettrolisiw2, nel qual caso si usa l’elettricità par spezzare H2O in H2 e ossigeno:
2H2O → 2H2 + O2 (3)

per telefoni cellulari
Powertrekk. Aggiungete
semplicemente dell’acqua e,
dopo pochi minuti, avrete
una batteria carica per il
vostro telefono cellulare
Immagine gentilmente
concessa da David Berkowitz;
fonte dell’immagine: Flickr
Questo metodo può essere sostenibile se l’elettricità proviene da fonti rinnovabili come vento, onde o energia solare. Perciò H2 può venire usato per accumulare energia in giornate ventose, quando le pale eoliche producono più elettricità di quella che può essere consumata.
È interessante il fatto che la scissione di H2O vvenga spontaneamente negli oceani, ad opera di alghe microscopiche e cianobatteri che usano l’energia solare per spezzare l’acqua in un processo chiamato biofotolisi (Equazione 3). Comunque, il tasso di produzione di H2 è estremamente lento.
Sono stati fatti dei tentativi per aumentare il tasso di produzione in condizioni controllate, utilizzando microorganismi modificati, ma il processo è ancora troppo lento e costoso per rappresentare una fonte realistica di H2 nell’immediato futuro (Hallenbeck & Ghosh, 2009).
Infine, il bioidrogeno può venire prodotto da coltivazioni e scarti industriali, forestali e agricoli utilizzando i batteri. Come facciamo anche noi esseri umani, questi batteri ossidano il materiale vegetale come fonte di energia ma, diversamente da noi, vivono in ambienti anerobici (privi di ossigeno). Nella respirazione aerobica noi utilizziamo O2 per ossidare gli zuccheri, ad esempio
C6H12O6 + 6O2 → 6CO2 + 6 H2O (4)
Al contrario, per ossidare quanto più possibile il substrato, e quindi ottimizzare il loro guadagno energetico, questi batteri anerobici riducono ad H2 i protoni rilasciati durante l’ossidazione del substrato (Equazione 6, più sotto).
Animaletti caldi

saccharolyticus al
microscopio elettronico
Immagine gentilmente
concessa da Harald Kirsebom
Durante il mio Dottorato di Ricerca ho studiato la capacità di produrre idrogeno di uno di questi batteri, Caldicellulosiruptor saccharolyticus (Figura 1), che vive in sorgenti termali: ambienti anerobici a 70 °C, con bassi livelli di carboidrati disponibili. Questo batterio è particolarmente interessante, perché è due volte più efficiente di molti batteri impiegati nella produzione di H2.
Diversamente da noi umani, C. saccharolyticus ottiene energia da un ampio spettro di molecole strutturali vegetali: non solo glucosio, ma anche, ad esempio, xylosio (Willquist et al., 2010).
Ciò permette al batterio di produrre H2 da rifiuti come quelli prodotti durante la lavorazione di patate, zucchero e carote, come anche da scarti industriali della produzione di pasta di legno e carta, o rifiuti agricoli come la paglia.
Si tratta di un inizio promettente, ma anche C. saccharolyticus rilascia solo il 33% dell’H2 che potenzialmente potrebbe essere rilasciato dal substrato. L’Equazione 5 mostra la possibile ossidazione completa del glucosio, che rilascia 12H2 per molecola di glucosio. L’Equazione 6 mostra la fermentazione buia eseguita da C. saccharolyticus, che rilascia solo 4H2 (33%) per molecola di glucosio. Il resto dell’energia viene rilasciato come acetato (CH3COOH).
Conversione completa del glucosio ad H2: C6H12O6 + 6H2O → 12H2 + 6CO2 (5)
Fermentazione buia: C6H12O6 + 2H2O → 4H2 + 2CO2 + 2CH3COOH (6)
Per rilasciare il resto di H2 dall’acetato c’è bisogno di energia esterna. In alternativa, dall’acetato si può ottenere metano (CH4), che attraverso la sintesi con vapore può rilasciare H2 (Equazioni 1 e 2). Fortunatamente, ci sono tre metodi interessanti per ottenere questa reazione (Figura 2).
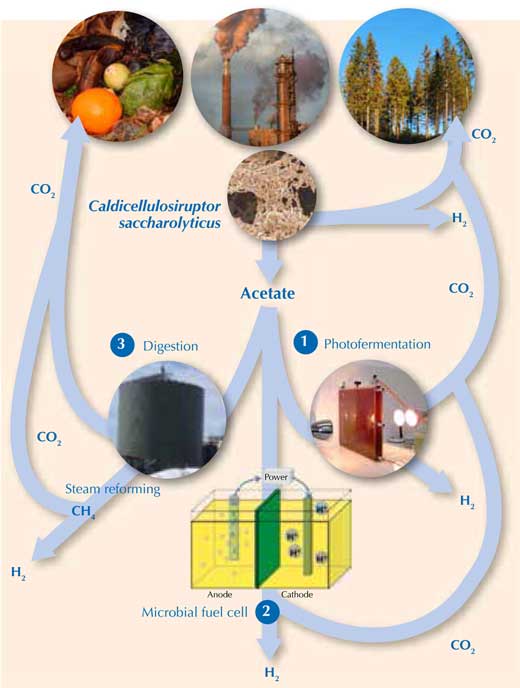
Per gentile concessione di Holger / pixelio.de (rifiuti), Michael Cavén (fabbrica di carta), Keith Bryant (alberi), Marcel Verhaart (C. saccharolyticus), Jakub Gebicki (fotobioreattore), Gokce Avcioglu, METU Biohydrogen Research Lab, Turkey (reattore per la digestione anerobica) e Karin Willquist (cella a combustibile microbica)
- Utilizzare la luce solare per convertire l’acetato ad H2 per mezzo di batteri fotofermentatori (Equazione 7)w3. Comunque, come la produzione algale di H2, questo processo è attualmente troppo lento e costoso per diventare commercialmente economico nel prossimo futuro (Hallenbeck & Ghosh, 2009).
2CH3COOH + 4H2O → 8H2 + 4CO2 (7)
- Utilizzare l’elettricità per accelerare la reazione da acetato a H2 in un una cella a combustibile microbica contenente un miscuglio di specie batteriche (Equazione 7)w4. Questa è un’idea elegante, ma la sua applicazione è attualmente limitata dai bassi tassi di produzione (Hallenbeck & Gush, 2009). (Per imparare come fabbricare la vostra cella a combustibile microbica, vedete Madden, 2010.)
- Utilizzanre batteri produttori di metano (Archaea) per digerire l’acetato, ottenendo metano (Equazione 8). La combinazione di fermentazione buia (Equazione 6) e produzione di metano è nota come processo a itano (idrogeno + metano) e può convertire approssimativamente il 90% del substrato originale in H2 e metano.
CH3COOH → CH4 + CO2 (8)
Il metano può poi venire sottoposto a sintesi con vapore rilasciando H2.

alimentata da una cella a
combustibile a idrogeno
Immagine gentilmente
concessa da Bull-Doser; fonte
dell’immagine: Wikimedia
Commons
Per dare un’idea del processo a itano, considerate che se i componenti di una famiglia di quattro persone mangiano ciascuno 10 kg di patate al mese, i loro rifiuti potrebbero alimentare lo 0.5% della loro richiesta energetica domestica mensile (3500 kWh), nel caso in cui l’H2 prodotto venga utilizzato direttamente (per evitare perdite energetiche) e che la casa venisse attrezzata con una cella a combustibile per produrre energia e calorew5. Ulteriore idrogeno potrebbe ovviamente venire prodotto da altri rifiuti – lo 0.5% proviene semplicemente dalle patate.
Questa è una stima grossolana del potenziale del processo a itano, basato su a) il 30% dell’energia viene perduto nella produzione di H2 e CH4 (itano) e b) il 30% serve per la sintesi con vapore da CH4 ad H2. Il passo (b) della sintesi con vapore viene impiegato nella produzione di idrogeno dal gas naturale ed è una tecnica commerciale ben sviluppata. La produzione dell’itano (a), comunque, non è ancora così efficiente, sebbene siano in corso ricerche per raggiungere il 70% di efficienza (come nell’esempio) e quindi rendere la produzione di bioidrogeno competitiva rispetto alla sintesi con vapore a partire da combustibili fossili per produrre idrogeno.
Sebbene di recente ci siano stati alcuni progressiw6 (vedi riquadro), è ancora troppo presto per fornire una stima del tempo richiesto perché la produzione sostenibile di H2 possa giocare un ruolo significativo nel nostro bilancio energetico. Comunque, come disse il poeta Mark Strand, “Il futuro inizia sempre adesso”.
Ricerca sulla produzione e immagazzinamento dell’idrogeno

Immagazzinare l’idrogeno in sicurezza è una delle principali sfide tecnologiche per adottare l’idrogeno come vettore energetico. L’Istituto Laue-Langevin (ILL)w7 si è oramai saldamente distinto per la sua ricerca di punta nell’economia dell’idrogeno, utilizzando la diffrazione di neutroni per seguire le reazioni di idrogenazione e deidrogenazione in materiali potenzialmente impiegabili per l’immagazzinamento dell’idrogeno. Per saperne di più, visitate il sito web dell’ILLw7.
I potenti fasci di raggi X dello European Synchrotron Radiation Facility (ESRF)w8 hanno recentemente verificato i complessi meccanismi con cui l’idrogeno viene prodotto da parte di enzimi chiamati idrogenasi. Molti di questi enzimi lavorano in condizioni anerobiche e sono, di fatto, inibiti dalla presenza di ossigeno. Gli idrogenasi che rimangono attivi in condizioni aerobiche, perciò, sono di grande interesse per tecnologie come le celle enzimatiche a combustibile e la produzione di idrogeno alimentata dalla luce. Un gruppo di scienziati tedeschi ha risolto di recente la struttura cristallina di uno di questi enzimi s (Fritsch et al., 2011) – forse un passo verso l’economia a idrogeno?
Sia ILL che ESRF sono membri di EIROforumw9, l’editore di Science in School.
References
- Fritsch J et al. (2011) The crystal structure of an oxygen-tolerant hydrogenase uncovers a novel iron-sulphur centre. Nature 479: 249–252. doi: 10.1038/nature10505
-
Scaricate gratuitamente l’articolo da qui, o abbonatevi a Nature: www.nature.com/subscribe
-
- Hallenbeck P, Ghosh D (2009) Advances in fermentative biohydrogen production: the way forward? Trends in Biotechnology 27: 287–297. doi: 10.1016/j.tibtech.2009.02.004
- Madden D (2010) La pila a combustibile microbico: energia elettrica dal lievito. Science in School 14. www.scienceinschool.org/2010/issue14/fuelcell/italian
- Rifkin J (2002) The Hydrogen Economy: the Creation of the Worldwide Energy Web and the Redistribution of Power on Earth. New York, NY, USA: JP Tarker. ISBN: 1585421936
- Schlapbach L, Züttel A (2001) Hydrogen-storage materials for mobile applications. Nature 414(6861): 353–358. doi: 10.1038/35104634
-
Scaricate gratuitamente l’articolo da qui, o abbonatevi a Nature: www.nature.com/subscribe
-
- Willquist K, Zeidan A, van Niel E (2010) Physiological characteristics of the extreme thermophile Caldicellulosiruptor saccharolyticus: an efficient hydrogen cell factory Microbial Cell Factories9: 89. doi: 10.1186/1475-2859-9-89
- Microbial Cell Factories è una pubblicazione open-access, perciò l’articolo è accessibile gratuitamente.
Web References
- w1 – Per saperne di più sugli accordi per l’applicazione dell’idrogeno dell’Agenzie Internazionale dell’Energia (IEA), vedete: http://ieahia.org
- w2 – Per saperne di più sulle prospettive dell’idrogeno, vedete l’analisi di Joseph Romm’s sul sito web di Environmentalists for Nuclear Energy (www.ecolo.org; under ‘documents’) o direttamente attraverso il link: http://tinyurl.com/77dhx8x
-
Vedete anche l’analisi peer-reviewed di Joan Ogden, Hydrogen as an Energy Carrier: Outlook for 2010, 2030 and 2050 sul sitoweb dell’Università della California: http://escholarship.org/uc/item/9563t9tc
-
- w3 – Per un video su come l’idrogeno viene rilasciato dalla biomassa delle patate utilizzando la luce del sole, vedete: www.biohydrogen.nl/hyvolution
- w4 – Per saperne di più sulle celle a combustibile microbiche, vedete: www.microbialfuelcell.org
- w5 – Per trovare dell’altro materiale sulle celle a combustibile termiche ed elettriche, vedete: www.fchea.org/index.php?id=57
- w6 – Per leggere dell’altro sui recenti progressi ottenuti in una centrale a bioidrogeno a Taiwan, vedi il sito web Focus Taiwan (http://focustaiwan.tw) o direttamente attraverso il link: http://tinyurl.com/7jao2tp
- w7 – ILL è un centro di ricerca all’avanguardia nella scienza e tecnologia dei neutroni, con base a Grenoble, in Francia. Per saperne di più, vedete: www.ill.eu
-
Per ulteriori informazioni sulla ricerca dell’ILL sull’economia dell’idrogeno, vedete il sito web dell’ILL oppure utilizzate l’URL: http://tinyurl.com/illhydrogen
-
- w8 – Localizzato nello stesso campus dell’ILL, a Grenoble, in Francia, all’ESRF funziona la più potente sorgente di radiazione di sincrotrone in Europa. Per saperne di più, vedete: www.esrf.eu
-
Per ulteriori informazioni sulla ricerca dell’ESRF sull’immagazzinamento dell’idrogeno, vedete il sito web di ESRF o utilizzate l’URL: http://tinyurl.com/87bnj4c
-
- w9 – Per maggiori informazioni su EIROforum, vedete: www.eiroforum.org
Review
In seguito alla pubblicazione del libro sull’economia dell’idrogeno di Jeremy Rifkin (2002), questo argomento viene affrontato spesso dai mezzi di informazione come una possibilità reale nel prossimo futuro. Un altro frequente tema riguardante l’idrogeno è il suo ipotetico ruolo come fonte di energia pulita. In questo articolo, Karen Willquist offre una visione complessiva dei problemi che coinvolgono la produzione dell’idrogeno e le ricerche in atto – compreso il suo stesso lavoro – per ottenere metodi sostenibili per raggiungere questo obiettivo.
Dato l’approccio chiaro dell’autrice, l’articolo è particolarmente adeguato per insegnanti di scienze e studenti della scuola secondaria superiore (14-19 anni) che vogliono approfondire la loro conoscenza di questo argomento complesso. Inoltre, sia gli studenti che gli insegnanti beneficeranno delle numerose fonti elencate.
L’articolo sarebbe importante per lezioni di biochimica (respirazione, fermentazione e fotosintesi), fisica (celle a combustibile, termodinamica: energia ed efficienza), scienze ambientali (fonti energetiche, combustibili fossili e fonti rinnovabili), biologia (alghe, batteri, cianobatteri e Archaea) e chimica organica (idrocarburi e sintesi con vapore). Potrebbe offrire anche una valida lettura di base prima di una visita ad una centrale elettrica o ad un laboratorio di ricerca sulle celle a combustibile o sulla produzione, uso e immagazzinamento dell’idrogeno.
L’articolo potrebbe essere impiegato per iniziare una discussione sulla differenza tra fonti energetiche e vettori energetici; i problemi dell’uso e immagazzinamento dell’idrogeno ed i possibili scenari per una transizione dalla nostra economia a idrocarburi ad una a idrogeno.
Adeguate domande di verifica comprendono:
- Quali delle seguenti risposte si applica alla respirazione, fermentazione buia, o entrambe?
- La presenza di glucosio
- La presenza di ossigeno
- L’assenza di ossigeno
- Quali dei seguenti processi non è coinvolto nella conversione dell’acetato in idrogeno?
- Fermentazione buia
- L’uso di elettricità in una cella a combustibile microbica
- Il processo a itano
Giulia Realdon, Italia





