Водородът: зеленият енергоносител в бъдеще? Understand article
Превод Емилия Мурзова. Водородът може да бъде горивото на бъдещето, но как можем да го произвеждаме устойчиво? Karin Willquist обяснява.

janeff / iStockphoto
Водородът е наричан „енергийният носител на бъдещето” – тъй като може да се окисли в горивна клетка за да произведе електричество за захранване на автомобил например, при това без освобождаване на въглероден диоксид (CO2), а и може да се произведе и в отдалечени места без изградена енергийна мрежа. За разлика от настоящите ресурси като природен газ и бензин, водородът трябва да бъде произведен, което го прави енергиен носител, а не гориво.
Енергийна система, в която водородът се използва за получаване на енергия – водородна икономика – е предложена от Джон Бокрис през 1970г.; а през 1977 е подписано международно споразумение за въвеждане на водорода, целящо постигането йw1.
В момента водородът се използва предимно като химичен реагент вместо като енергиен носител, но несъмнено носи потенциала да трансформира транспортните ни и енергийни системи. Реализирането на този потенциал обаче на е лесно. Повечето от използваните днес горива са течни, твърди или газообразни и с висока енергия на единица обем (енергийна плътност). Водородът за разлика от тях има ниска енергийна плътност: при определено налягане изгарянето на един литър водород дава една трета от енергията, отделена при изгарянето на метана. Това предполага проблеми при съхранението, транспортирането и използването, които учените описват (Schlapbach & Züttel, 2001)w2. Още по-голямо предизвикателство е устойчивото производство на водород. Върху тази тема ще се фокусирам тук.

задвижван от водородни
горивни клетки
С любезното съдействие на
Felix O; източник: Flickr
Начини за производство на водород
Водородът е често срещан на земната повърхност елемент, обикновено свързан с въглерод във въглеводороди (в растенията) или с кислород във водата (H2O). Газообразният водород (H2), съществува само в малки количества на Земята. Едно от предизвикателствата пред устойчивото производство е добиването на H2 от съединенията му с въглерода и кислорода.
Понастоящем H2 се произвежда основно от изкопаеми горива (напр. природен газ) чрез паров реформинг: горивото се загрява до висока температура чрез използване на водаw2:
CH4 + H2O → CO + 3H2 (1)
CO + H2O → CO2 + H2 (2)
Този метод обаче се основава на изкопаеми горива и освобождава CO2, причиняващ същите проблеми с отделените емисии, както и изкопаемите горива. Паровият реформинг е устойчив само ако се използват възобновяеми въглеводороди като био-газ, тъй като отделеният CO2 преди това е бил погълнат при производството на въглеводородите.
H2 може да бъде произведен и чрез електролизаw2, при която чрез електричество H2O се разделя на H2 и кислород:
2H2O → 2H2 + O2 (3)

мобилен телефон Fuels от
Powertrekk. Просто сипете
вода и след няколко минути
ще имате батерия за
мобилния си телефон
С любезното съдействие на
David Berkowitz; източник:
Flickr
Този метод е устойчив, ако електричеството е от възобновяеми източници като вятърната, водната или слънчевата енергия. По този начин H2 може да се използва за складиране на енергия във ветровитите дни, когато вятърните генератори произвеждат повече енергия, отколкото може да бъде изразходвана.
Итересното е, че разделянето на H2O е естествен процес в океаните, тъй като микроскопичните синьо-зелени водорасли и цианобактериите използват слънчевата енергия за разделянето на водата в процес, наречен биофотолиза (уравнение 3). Скоростта на производство на H2 обаче е екстремно ниска.
Правен са усилия за увеличаването на нивото на производство при контролирани условия, използвайки модифициране микроорганизми, но процесът си остава все така бавен и скъп за да бъде реалистичен източник на H2 в скоро време (Hallenbeck & Ghosh, 2009).
И най-накрая, биоводородът може да бъде произведен от зърнено-житни култури и от индустриални, горски или селскостопански отпадъци, използвайки бактерии. Както и ние, тези бактерии окисляват растителния материал като източник на енергия, но за разлика от нас, те живеят в анаеробна среда (без кислород). При аеробното дишане ние използваме O2 за окисление на захарите, т.е.
C6H12O6 + 6O2 → 6CO2 + 6 H2O (4)
Обратно, за да окислят субстрата колкото е възможно повече и така да оптимизират добива на енергия, тези анаеробни бактерии редуцират протоните, отделени при окислението, до H2 (уравнение 6, по-долу).
Горещи продуценти

микроскопска снимка на
бактерията C.
saccharolyticus
С любезното съдействие на
Harald Kirsebom
Докато подготвях докторската си дисертация, изследвах способността за производство на водород на една от тези бактерии, Caldicellulosiruptor saccharolyticus (фиг. 1), която обитава горещите извори: анаеробна среда при 70 °C, с ниско съдържание на въглеводороди. Тази бактерия е особено интересна, защото е два пъти по-ефективна от повечето бактерии, използвани за производство на H2.
За разлика от хората, C. saccharolyticus произвежда енергия, използвайки широк кръг от растителни градивни елементи: не само глюкоза, а например и ксилоза (Willquist et al., 2010).
Това позволява на бактерията да произвежда H2 от отпадъци като тези от преработката на картофи или моркови, а също и от промишлени отпадъци от производството на хартия, или от отпадъци от селското стопанство като сламата например.
Перспективно начало, но дори C. saccharolyticus извлича едва 33% от потенциалното количество H2, което би могло да бъде произведено от субстрата. Уравнение 5 показва потенциалното пълно окисление на глюкозата, при което се отделят 12H2 от една молекула глюкоза. Уравнение 6 показва ферментацията, която C. saccharolyticus извършва на тъмно, при което се отделят само 4H2 (33%) от една молекула глюкоза. Останалата енергия се отделя под формата на оцетна киселина (CH3COOH).
Пълно разграждане на глюкозата до H2: C6H12O6 + 6H2O → 12H2 + 6CO2 (5)
Ферментация на тъмно: C6H12O6 + 2H2O → 4H2 + 2CO2 + 2CH3COOH (6)
За освобождаването на останалата част H2 в оцетната киселина е необходима енергия. Обаче метанът (CH4), от който чрез паров реформинг може да бъде получен H2 (уравнения 1 и 2), може да се добие от оцетна киселина. За щастие съществуват три перспективни начина това да се направи (фиг. 2).
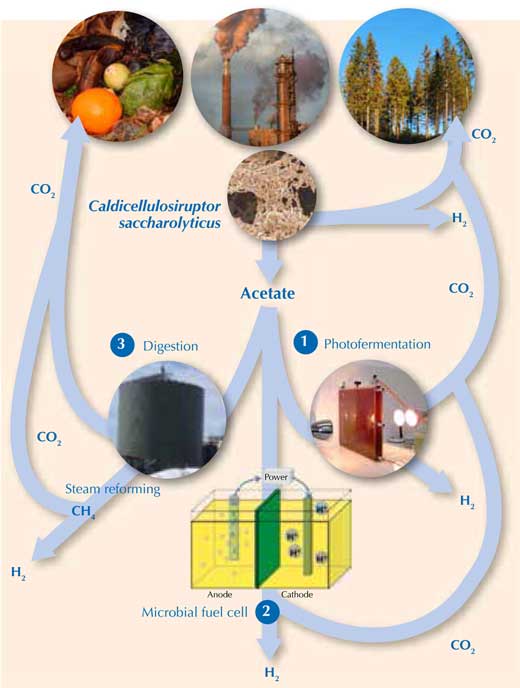
С любезното съдействие на Holger / pixelio.de (отпадъци), Michael Cavén (хартиена фабрика), Keith Bryant (trees), Marcel Verhaart (C. saccharolyticus), Jakub Gebicki (фотобиореактор), Gokce Avcioglu, METU Лаборатория за изследване на биоводород, Турция (реактор за анаеробно преработване) и Karin Willquist (микробиална горивна клетка)
- Използване не слънчевата светлина за преобразуване на оцетната киселина до H2 от фотоферментираща бактерия (уравнение 7)w3. Както и при производството на H2 от синьо-зелени водорасли обаче, този процес е бавен и скъп за да бъде използван за търговски цели в близкото бъдеще (Hallenbeck & Ghosh, 2009).
2CH3COOH + 4H2O → 8H2 + 4CO2 (7)
- Използване на електричество за възбуждане на превръщането на оцетната киселина до H2 в микробактериална горивна клетка в присъствието на няколко бактериални вида (уравнение 7)w4. Това представлява една елегантна концепция, но приложението й е ограничено от ниските нива на производство (Hallenbeck & Gush, 2009). (За да разберете как да направите своя микробиална горивна клетка, вижте Madden, 2010.)
- Използване на метанови продуценти (Archaea), които да преработят оцетната киселина до метан (уравнение 8). Комбинацията от ферментация на тъмно (уравнение 6) и производството на метан е известна като хитанов процес (hydrogen + methane, т.е. водород и метан) и с него може да бъде преработен приблизително 90% от началния субстрат до H2 и метан.
CH3COOH → CH4 + CO2 (8)
При паров реформинг на метана се освобождава H2.

задвижвано от водородна
горивна клетка
С любезното съдействие на
Bull-Doser; източник:
Wikimedia Commons
Перспектива на хитановия процес: ако четири човека в едно домакинство изяждат по 10 kg картофи на месец, отпадъците им могат да покрият 0,5% от месечния им разход на енергия (3500 kWh), при условие че произведеният H2 се използва директно (за да се избегнат загуби на енергия) и че домът им е снабден с отоплителна и енергийна горивна клеткаw5. Разбира се от отпадъците е възможно да се генерира повече водород – 0,5% е количеството само от картофите.
Горният случай е само груб пример за потенциала на хитановия процес при следните допускания а) 30% загуба на енергия при производствота на H2 и CH4 (хитан) и б) допълнителни 30% при послеващия паров реформинг на CH4 до H2. Паровият реформинг (б) се използва за производството на водород от природен газ и е усъвършенствана техника, използвана в индустрията. Производството на хитан (а) обаче все още не е ефективно, въпреки продължаващите изследвания за повишаване на ефективността му до 70% (както в примера) и по този начин производството на биоводород е конкурентно на паровия реформинг на изкопаеми горива с цел производство на водород.
Въпреки прогреса, постигнат напоследъкw6 (виж карето), все още е твърде рано да се предскаже кога устойчивото производство на H2 ще започне да играе съществена роля при добива на енергия. Но както казва поетът Марк Станд „Бъдещето винаги започва сега.”
Изследвания на съхранението и производството на водород

Безопасното и ефикасно съхранение на водород е едно от основните технологични предизвикателства пред използването на водорода като енергоносител. Институтът Лауе-Ланжевен (ILL)w7 предлага челен опит в изследването на водородната икономика, използвайки неутронна дифракция за контрол на хидрогеназните и дехидрогеназните реакции при материалите с потенциал за съхранение на водорода. За да научите повече, посетете сайта на ILLw7.
Мощните рентгенови лъчи на Европейския център за синхротронна радиация (ESRF)w8 се използват за да се изследват механизмите, чрез които водородът се произвежда чрез ензимите, наречени хидрогенази. Повечето от тях са активни при анаеробни условия и на практика се инхибират в присъствието на кислород. Активните в аеробна среда хидрогенази представляват особен интерес при технологии като ензимните горивни клетки и производството на водород на светло. Немски екип учени наскоро е описал кристалната структура на един от тях (Fritsch et al., 2011) – навярно това е стъпка в посока водородна икономика?
И ILL, и ESRF са членове на EIROforumw9, издателят на Science in School.
References
- Fritsch J et al. (2011) The crystal structure of an oxygen-tolerant hydrogenase uncovers a novel iron-sulphur centre. Nature 479: 249–252. doi: 10.1038/nature10505
-
Свалете си безплатно статията от тук, или се абонирайте за Nature още днес: www.nature.com/subscribe
-
- Hallenbeck P, Ghosh D (2009) Advances in fermentative biohydrogen production: the way forward? Trends in Biotechnology 27: 287–297. doi: 10.1016/j.tibtech.2009.02.004
- Madden D (2010) The microbial fuel cell: electricity from yeast. Science in School 14: 32-35. www.scienceinschool.org/2010/issue14/fuelcell
- Rifkin J (2002) The Hydrogen Economy: the Creation of the Worldwide Energy Web and the Redistribution of Power on Earth. New York, NY, USA: JP Tarker. ISBN: 1585421936
- Schlapbach L, Züttel A (2001) Hydrogen-storage materials for mobile applications. Nature 414(6861): 353–358. doi: 10.1038/35104634
-
Свалете си безплатно статията от тук, или се абонирайте за Nature още днес: www.nature.com/subscribe
-
- Willquist K, Zeidan A, van Niel E (2010) Physiological characteristics of the extreme thermophile Caldicellulosiruptor saccharolyticus: an efficient hydrogen cell factory Microbial Cell Factories 9: 89. doi: 10.1186/1475-2859-9-89
- Microbial Cell Factories е списание с отворен достъп и статията може да бъде свободно прегледана.
Web References
- w1 – За да научите повече за споразумението за въвеждане на водорода на Международната енергийна агенция, посетете: http://ieahia.org
- w2 – За да научите повече за перспективите, които водородът предлага, разгледайте анализа на Joseph Romm’s на сайта на Environmentalists for Nuclear Energy (www.ecolo.org; секция ‘документи’) или директно на: http://tinyurl.com/77dhx8x
-
Анализът на Joan Ogden Hydrogen as an Energy Carrier: Outlook for 2010, 2030 and 2050 може да бъде намерен на сайта на Калифорнийския университет: http://escholarship.org/uc/item/9563t9tc
-
- w3 – Видео за това как от картофена биомаса се получава водород като се използва слънчевата светлина: www.biohydrogen.nl/hyvolution
- w4 – За да разберете повече за микробните горивни клетки, посетете: www.microbialfuelcell.org
- w5 – За да разберете повече за отоплителните и енергийните горивни клетки, посетете: www.fchea.org/index.php?id=57
- w6 – За да прочетете за скорошния напредък в биоводородната горивна станция в Тайван, разгледайте сайта Focus Taiwan (http://focustaiwan.tw) или директно на http://tinyurl.com/7jao2tp
- w7 – ILL е международен изследователски център, водещ в областта на неутронната наука и технологии, който се намира в Гренобъл, Франция. Повече информация: www.ill.eu
-
За повече информация относно изследванията на ILL в икономиката на водорода, посетете сайта на ILL или използвайте директната връзка: http://tinyurl.com/illhydrogen
-
- w8 – Разположен в същия район, в който се намира ILL, в Гренобъл, Франция, в ESRF работи най-мощния източник на синхротронно излъчване в Европа. За да научите повече, посетете: www.esrf.eu
-
За повече информация относно изследванията на ESRF относно съхранението на водорода, посетете сайта на ESRF или използвайте директната връзка: http://tinyurl.com/87bnj4c
-
- w9 – За да разберете повече за EIROforum, посетете: www.eiroforum.org
Review
След публикуването на книгата на Jeremy Rifkin за водородната икономика (2002), тази тема често се споменава в медиите като реално възможна в близко бъдеще. Друг въпрос, касаещ водорода е предполагаемата му роля като чист източник на енергия. В настоящата статия Карин Уилквист прави цялостен преглед на темите, засягащи производството на водород и настоящите изследвания, включително и собствената си работа, в посока устойчив вариант за постигане на целта.
При ясния подход на автора, статията е особено подходяща за учители и ученици в горните гимназиални курсове (на възраст 14-19 години), желаещи да задълбочат познанията си в тази сложна тема. Освен това и учители, и студенти могат да се възползват от изброените източници.
Статията може да се използва в уроци по биохимия (дишане, ферментация, фотосинтеза), физика (горивни клетки, термодинамика: енергия и ефикасност), природни науки (енергийни източници, изкопаеми горива и възобновяеми източници), биология (синьо-зелени водорасли, бактерии, цианобактерии и Archaea) и органична химия (въглеводороди и паров реформинг). Освен това може да осигури добра основа ако се прочете преди посещение в електроцентрала или изследователска лаборатория, занимаваща се с горивни клетки или производство, използване и съхранение на водород.
Статията може да бъде използвана и за иницииране на дискусия относно разликите между източниците на енергия и енергоносителите; проблемите на използването и съхранението на водород; както и възможните сценарии при преминаване от настоящата икономика на въглеводородите към водородна икономика.
Подходящи въпроси биха били:
- Кое от по-долу изброените се отнася за дишането, за ферментацията на тъмно, или за и двете?
- Наличието на глюкоза
- Присъствие на кислород
- Отсъствие на кислород
- Кое от следните не е процес, протичащ при преобразуването на оцетна киселина във водород?
- Ферментация на тъмно
- Използване на електричество в микробиални горивни клетки
- Хитановият процед
Giulia Realdon, Италия





