Supporting materials
Hoja de trabajo para la Actividad 1 (Word)
Hoja de trabajo para la Actividad 1 (Pdf)
Hoja de trabajo para la Actividad 2 (Word)
Hoja de trabajo para la Actividad 2 (Pdf)
Download
Download this article as a PDF

Traducido por Aníbal Pacheco. Caliente, luminoso y destructivo: el fuego, una fuerza de la naturaleza. Aquí veremos como utilizarlo y controlarlo de forma segura con agua y dióxido de carbon.

El fuego tiene un lugar en la prehistoria, cultura y tecnología. Los primeros seres humanos habrían encontrado fuegos de origen natural – desde fuegos forestales y relámpagos, hasta quizás, erupciones volcánicas. Después, el ser humano aprendió como generar y mantener el fuego a su antojo y utilizarlo para iluminación y como fuente de calor. Más tarde, entendimos su química y como adaptarlo para su uso en formas delicadamente controladas – como por ejemplo en el motor de combustión interna.
Hoy en día, además de ser una parte primordial de la tecnología, el fuego es un peligro: en Europa, miles de personas pierden la vida debido al fuego, con pérdidas económicas estimadas del uno por ciento del PIB w1. El fuego es por lo tanto un asunto importante debido a su potencial y a sus riesgos.
Inspirados por esta idea, hemos desarrollado una serie de actividades para estudiantes de 11 a 14 años de edad, para explorar de forma segura la naturaleza del fuego. En la primera actividad, mostramos como ‘quemar dinero’, mientras que en la segunda, demostramos las propiedades extintoras del dióxido de carbono. Finalmente, damos a los estudiantes la oportunidad de discutir cómo mantenerse a salvo del fuego. Las actividades requieren un total de 35 minutos aproximadamente (15 minutos para la primera actividad y 10 minutos para la segunda y tercera actividad).
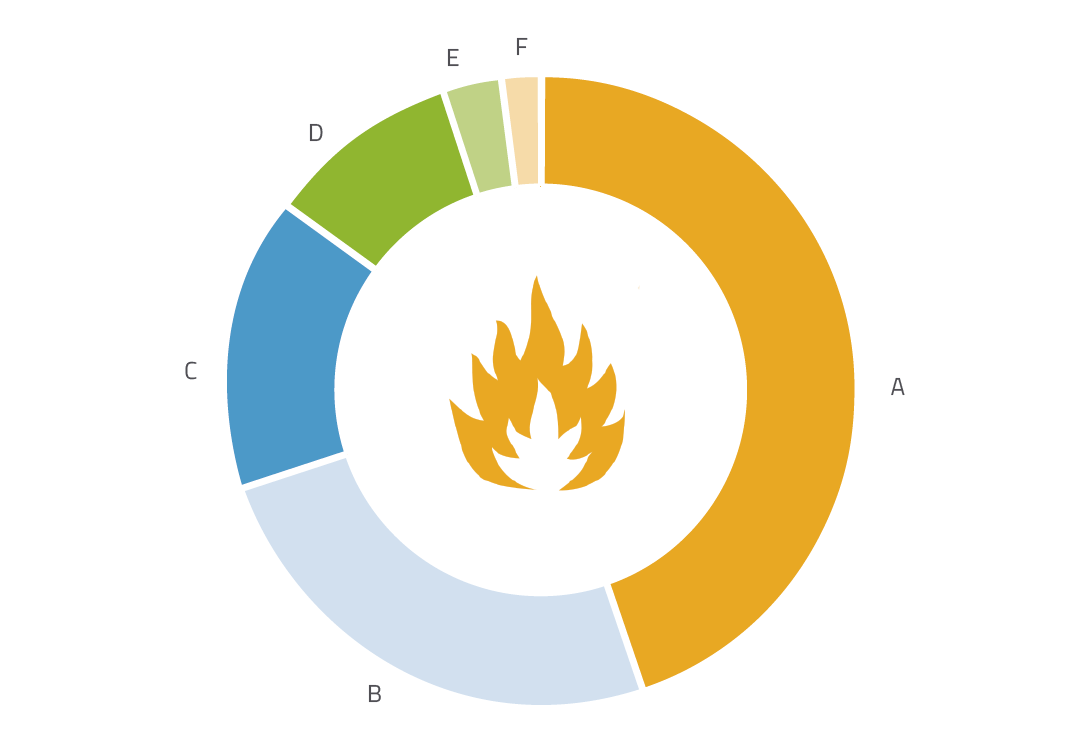
Como preludio a las actividades prácticas, se pide a los estudiantes que nombren cinco ideas que asocien con la palabra ‘fuego’. Las asociaciones más frecuentes se presentan en la figura 1.
Esta actividad es parecida a un truco de magia – ¡una demostración de cómo quemar tu dinero y aún así conservarlo!
Esa actividad debe realizarse solo por el maestro como una demostración.
Llevar gafas de seguridad, bata de laboratorio y guantes. Debe tenerse especial cuidado con las flamas y con el manejo del alcohol para evitar un incendio.




Después del experimento, pide a los estudiantes que discutan en grupos lo que ha sucedido. Motívalos a desarrollar sus propias ideas, utilizando una hoja de trabajow2 o con las siguientes preguntas:
Después, discutan las ideas de los estudiantes con toda la clase, guiándoles a las correctas explicaciones de ser necesario.
Esta actividad es desarrollada por los estudiantes bajo la supervisión del maestro. Existen dos variantes: en la versión más simple (versión 1), se produce dióxido de carbono en un vaso de precipitado y después se muestra como se apaga una cerilla o vela encendida que es colocada dentro del vaso. En la versión 2, se vierte el dióxido de carbono sobre la flama – una acción similar a cuando se utiliza un extintor para apagar un fuego.
Llevar gafas de seguridad, bata de laboratorio y guantes, y la actividad debe desarrollarse en un área bien ventilada. Debe tenerse especial cuidado con las flamas y con el manejo del alcohol metílico para evitar un incendio. Debe recordarse a los estudiantes como trabajar de forma segura con flamas, y que hacer con los remanentes calientes después del experimento.
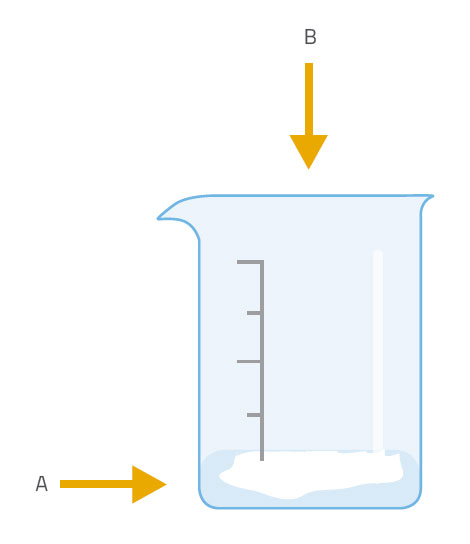
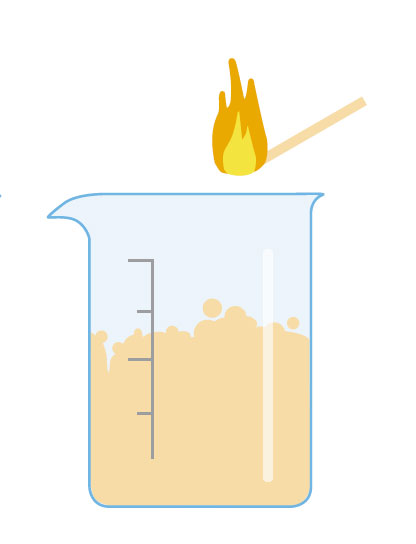
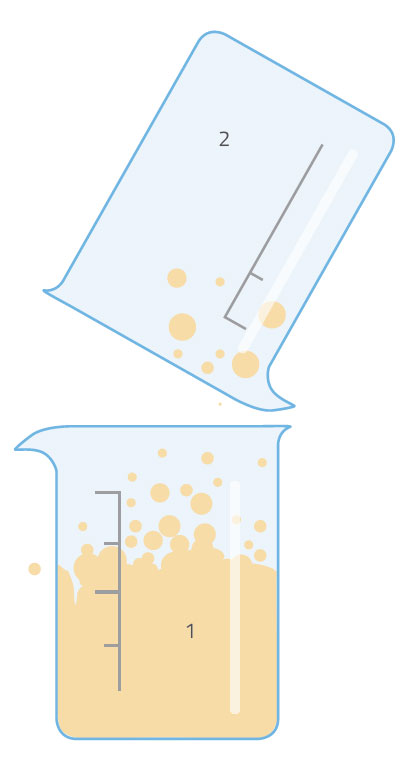

Pide a los estudiantes que discutan en grupos lo que ha sucedido (en cualquiera de las versiones del experimento). Estimúlalos con preguntas como:
Utiliza una hoja de trabajow2 para proveer un enfoque estructurado a estas preguntas, guiando a los estudiantes a la explicación correcta.
El gas producido en la reacción del bicarbonato con el vinagre es dióxido de carbono (CO2):
NaHCO3 + CH3COOH → CH3COONa + H2O + CO2
El dióxido de carbono es más pesado que el aire, por lo que se queda en el vaso. Además, no permite la combustión – de hecho, evita que el oxígeno llegue a la flama, lo cual es necesario para mantener una combustión, por lo que la flama se apaga. El hecho de que el dióxido de carbono sea más pesado que el aire también implica que pueda ser ‘vertido’ de un vaso a otro.
El dióxido de carbono también puede ser peligroso para humanos y otros animales, cuando se encuentra en grandes concentraciones o en un espacio cerrado (por ellos es necesario realizar este experimento en un área bien ventilada). Esto no es solo porque necesitamos de oxígeno para respirar, sino también debido a que nuestros cuerpos sienten los niveles de dióxido de carbono y utiliza esto para regular la respiración – entonces una atmósfera que contenga solo uno por ciento de dióxido de carbono puede interferir con este mecanismo. Pero el dióxido de carbono también es útil: las plantas utilizan dióxido de carbono, agua y luz para la fotosíntesis, con lo que se produce el oxígeno y permite el crecimiento de las plantas.
El objetivo de esta actividad es para aumentar la concientización de los estudiantes sobre los riesgos asociados con el fuego. Los tópicos a cubrir son:
Sugerimos iniciar con una discusión liderada por el(la) maestro(a), seguido de búsquedas en internet realizadas por los estudiantes en grupo. Cada grupo puede abordar una de las cuestiones planteadas arriba (o cuestiones similares), creando un poster o una presentación para mostrarla al resto de la clase.
También vale la pena invitar a un(a) orador(a) invitado(a) – idealmente un(a) bombero(a) o un(a) proveedor(a) de primeros auxilios entrenado en lidiar con quemaduras. Además de proveer información, esto subrayara el hecho de que los incendios ocurren de verdad – y mientras que confiamos en expertos entrenados cuando las cosas van mal, depende de nosotros en primer lugar el ayudar en la prevención de incendios.
Este artículo es una gran oportunidad para que los maestros conecten las clases con las experiencias diarias de los niños. Combina actividades interesantes con una discusión final sobre seguridad; me agrada el hecho de que el artículo este basado en el aprendizaje del seguro manejo de fuego. Además, la actividad final hace que el artículo sea adecuado para discusiones relacionadas con los límites y peligros de la química y la ciencia, así como su aplicación en la vida diaria.
Christiana Nicolaou, Escuela Elemental Archangelos, Nicosia, Chipre