La ciencia del sobreenfriamiento Understand article
Traducido por Elisa Inés López Schiaffino. Cuando algo se enfría hasta alcanzar temperaturas inferiores a su punto de congelación, se solidifica; o al menos eso es lo que se espera. Tobias Schülli investiga por qué no siempre es así.

iStockphoto
¿Cómo puede ser que las nubes a gran altura, a una temperatura inferior a 0°C, estén compuestas de pequeñas gotitas de agua en vez de hielo? En realidad, bajo determinadas condiciones, los líquidos pueden permanecer en estado líquido por debajo de su punto de fusión. Aunque este fenómeno, llamado sobreenfriamiento, fue descubierto en 1724 por Daniel Gabriel Fahrenheit (Fahrenheit, 1724), todavía hoy es objeto de estudio.
Los diferentes estados de la materia
Para los científicos, la fase líquida es un estado de la materia extraño entre el orden y el desorden. El gas perfecto es un buen ejemplo del estado de la materia en desorden: el movimiento térmico de los átomos individuales (o moléculas) es tan importante que las fuerzas de atracción entre ellos no tienen relevancia y por lo tanto los átomos se mueven libremente a través del espacio. En el extremo opuesto, en el estado sólido, cada átomo permanece en un lugar fijo, vinculado estrechamente a su vecino. Esto, debido a la optimización de las uniones químicas y las energías de enlace, generalmente produce un empaquetamiento más denso de los átomos en una distribución tridimensional regular, que se llama cristal. Por lo tanto, la mayoría de las veces, lo que llamamos sólido es en realidad un sólido cristalino.
En el estado líquido (intermedio), los átomos vecinos están en contacto al igual que en el estado sólido (por eso ambos estados son conocidos como la materia condensada), pero los átomos individuales pueden moverse, lo que impide la formación del patrón regular perfecto del cristal. Por lo tanto, la densidad de un líquido (comparada con la de un gas) difiere muy poco de la del estado sólido (véase la Figura 1).

Los estados de la materia:
a) En el estado sólido o cristalino de la materia, cada átomo permanece en un lugar fijo. Se puede decir que está vinculado estrechamente a sus vecinos. Si calentamos un cristal, los átomos comienzan a moverse (vibración térmica).
b) En el estado líquido (a temperaturas superiores al punto de fusión), el movimiento térmico permite que los átomos individuales se muevan libremente, aunque las fuerzas de atracción entre los átomos hacen que estén casi tan cerca como en el estado sólido. Por eso, un líquido tiene casi la misma densidad que un sólido y resiste la compresión, al igual que un sólido.
c) A temperaturas elevadas, el movimiento térmico de los átomos individuales en un gas se vuelve tan significativo que las fuerzas de atracción entre los átomos no juegan ya ningún papel, y los átomos pueden moverse libremente en el espacio. La densidad de un gas depende de la presión y la temperatura circundante. En condiciones de alta presión o baja temperatura, los átomos pueden juntarse nuevamente y condensarse en formaciones más densas, originando un líquido o un sólido. Por esto, a estos dos estados también se los llama materia condensada
Imágenes cortesía de Tobias Schülli
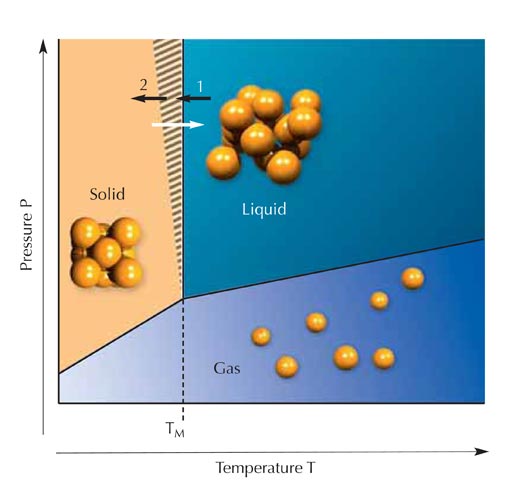
Imagen cortesía de Tobias Schülli

en un estado metaestable:
permanece en este estado
solamente si las condiciones
permanecen sin cambios. El
círculo azul está en un
estado de transición (o
inestable), desplazándose
hacia el estado estable
representado por el círculo
negro. Cualquier estado
inestable se desplaza hacia el
estado estable, mientras que
el estado metaestable
requiere de condiciones
específicas para hacer lo
mismo
Imagen cortesía de Tobias
Schülli
Aunque se considera que un líquido está mayormente en desorden, los átomos se pueden disponer localmente en pequeños grupos, lo que da origen al concepto de orden local. Es difícil observar experimentalmente la naturaleza exacta de estos estados de orden local, pero se cree que desempeñan una función crucial en la transición de una sustancia de una fase desordenada a una ordenada.
El hecho de que una sustancia particular esté en la fase gaseosa, sólida o líquida depende de la temperatura y la presión. A temperatura atmosférica, el hielo se funde a 0 °C, el mercurio a -39 °C y el oro a 1064 °C. Al calentarse, los sólidos (los cristales) se funden precisamente a estas temperaturas. Sin embargo, no pasa lo opuesto: cuando se enfría un líquido a su punto de fusión, es posible que se forme un cristal pero no necesariamente pasa a su punto de fusión (Figura 2). En la zona a rayas de la figura, un líquido puro (sin impurezas cristalinas) permanece en estado líquido; se lo llama líquido sobreenfriado. Este estado de la materia es llamado metaestable (Figura 3).
¿Cómo se explica el sobreenfriamiento?
La primera explicación del sobreenfriamiento se encuentra en la física de la cristalización. La formación de un cristal requiere de un núcleo de átomos distribuidos regularmente, alrededor de los que se pueda formar un cristal. La cristalización ocurre en mayor medida cuando un líquido está en contacto con una superficie sólida o cuando un líquido contiene impurezas cristalinas; es como si el líquido imitara la estructura ordenada de la superficie vecina. Eso se llama nucleación heterogénea, y comienza a partir de una semilla.
Si no hay un sólido cristalino, no es probable que ocurra la formación de una estructura grande y regular espontáneamente a partir de un líquido en desorden. Aunque un pequeño número de átomos puede formar espontáneamente una disposición regular, estos grupos son generalmente demasiado pequeños para que sirvan de núcleos de cristalización, y se vuelven a disolver rápidamente en el líquido. Por ello, un líquido puro necesita ser sobreenfriado para que ocurra la nucleación homogénea: algunos átomos en el líquido se ordenan espontáneamente de la manera correcta para formar un cristal que sea lo suficientemente grande y estable como para servir de núcleo para un mayor crecimiento del cristal (Figura 4).

a) La formación de cristales generalmente comienza alrededor de un sólido cristalino en contacto con el líquido (nucleación heterogénea).
b) Como consecuencia, el líquido necesita ser sobreenfriado para que ocurra la nucleación homogénea: algunos átomos en el líquido se ordenan espontáneamente de la manera correcta para formar un cristal, que luego sirve de núcleo para un mayor crecimiento del cristal. Imagen cortesía de Tobias Schülli
Imagen cortesía de Tobias Schülli
La mayoría de las pequeñas gotitas de agua que forman las nubes estratiformes y cumuliformes no contienen semillas de cristales; esas gotas pueden permanecer líquidas a temperaturas inferiores a 0 °C.
El sobreenfriamiento profundo en los metales
Aún más espectacular que el agua (que puede ser sobreenfriada sólo aproximadamente a 40 grados por debajo de su punto de fusión de 0 °C) son los metales, que pueden existir en forma líquida a varios cientos de grados por debajo de su punto de fusión. Esto se llama sobreenfriamiento profundo, y ha desafiado a los científicos a ir más allá de la teoría de la nucleación de los cristales para explicar la metaestabilidad de los líquidos (Turnbull, 1952).
Los científicos piensan que la estructura interna de algunos líquidos podría ser incompatible con la cristalización. En los años cincuenta, Frederick Charles Frank propuso que la disposición más densa de un pequeño número de átomos puede ser distinta de la disposición local de átomos en un cristal, y que, debido a eso, en un líquido estos grupos no están ordenados de la manera indicada para servir como núcleo de cristalización (Frank, 1952).

Imagen cortesía de Nicola Graf
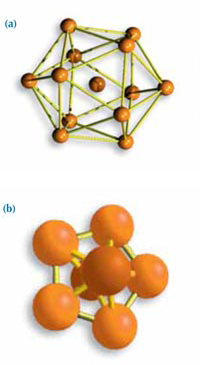
estructuras que no son
compatibles con la formación
de un cristal:
(a) Un icosaedro, la
disposición más densa
posible de 13 átomos.
(b) Un grupo de 7 átomos con
simetría pentagonal.
Imágenes cortesía de Tobias
Schülli
Como modelo, Frank utilizó un icosaedro: un átomo central con doce átomos circundantes. Tal estructura, que tiene una simetría pentagonal, no puede constituir la base de un cristal. En general, una estructura cristalina debe repetirse en tres dimensiones, como los ladrillos de una pared. Una disposición cúbica, por ejemplo, es una estructura excelente para un cristal, ya que es densa y completamente regular.
En un plano bidimensional, los triángulos, rectángulos y hexágonos pueden cubrir una superficie en su totalidad, mientras que los pentágonos no (Figura 5). En el plano tridimensional, las estructuras pentagonales son incompatibles con la formación de un cristal (Figura 6).
Las simulaciones y los modelos teóricos recientes respaldan la conjetura de Frank, lo que sugiere que una fracción importante de los átomos de los líquidos se agrupan en formaciones con cinco ejes de simetría, representando por ello un obstáculo a la cristalización. Sin embargo, hasta ahora muy pocos experimentos han permitido la visualización de la simetría pentagonal en líquidos (Reichert et al., 2000).
El sobreenfriamiento en nanoestructuras semiconductoras
Mi encuentro con el fenómeno del sobreenfriamiento no fue intencional. En realidad, el objetivo de mi investigación, realizada dentro de un grupo en la CEAw1 en Grenoble, Francia, era comprender y mejorar nuevos métodos de crecimiento de nanoestructuras semiconductoras. En estos métodos, los procesos de solidificación y nucleación son cruciales. A nuestro grupo le llamó la atención un informe sobre el sobreenfriamiento en gotitas de aleaciones de metales semiconductores: estas gotitas nos servían para estudiar la influencia de la semilla cristalina (una superficie de silicio) en la solidificación de la aleación.
Depositamos pequeñas gotitas (0,1 – 0,2 µm) de una aleación líquida de oro y silicio sobre una superficie de silicio, preparada bajo condiciones de ultra alto vacío, una técnica comúnmente usada en los procesos semiconductores. Observamos que, mientras estuvieron en contacto con esta superficie cristalina, las gotitas permanecieron líquidas a 240 °C, bien por debajo de su punto de fusión (que es 363 °C). Para poder comprender este extraordinario fenómeno de sobreenfriamiento (generalmente sólo observado en ausencia de semillas cristalinas), llevamos a cabo un experimento en el European Synchroton Radiation Facility (ESRF)w2, también en Grenoble. Una buena manera de obtener información sobre la disposición de átomos en superficies líquidas y sólidas es a través de la dispersión de intensos rayos X que se producen en un sincrotón.
Disparamos rayos X en forma casi paralela a la superficie del cristal de silicio sobre el que habíamos depositado las gotitas de aleación de oro y silicio. A un ángulo de sólo 0,1° (una técnica llamada incidencia rasante), los rayos X son reflejados por la superficie de silicio plana y penetran las gotitas. Los rayos X dispersos llevan información sobre la disposición atómica de la última capa atómica de la superficie de silicio, y también sobre la estructura de las gotitas.
Estos experimentos nos permitieron determinar el estado (líquido o cristalino) de las gotitas a medida que se enfriaban, y determinar la disposición atómica exacta de la capa atómica superior de la superficie de silicio. Los resultados de los rayos X mostraron que en la capa atómica superior de la superficie de silicio, los átomos presentan formaciones con cinco ejes de simetría. Sobre estas superficies, incluso cuando se las enfrió a más de 100 grados por debajo de su punto de fusión, las gotitas permanecieron líquidas.
Un análisis más detallado de la interfaz sólida / líquida reveló que estas estructuras pentagonales de la superficie estaban formadas por una sola capa de átomos de oro estrechamente vinculados al cristal de silicio. Como explicamos anteriormente, generalmente se espera que los líquidos imiten la estructura sólida con la que están en contacto, provocando la nucleación heterogénea. Nuestras mediciones mostraron que dicha imitación de la estructura de la superficie ocurre, pero puede tener el efecto opuesto: una estructura que es incompatible con la formación de un cristal en 3D puede hacer que el líquido adopte localmente un tipo de orden ‘equivocado’. En lugar de causar la nucleación heterogénea, esto aumenta la estabilidad de la fase de sobreenfriamiento del líquido (véase la Figura 7).
Luego de 60 años de investigación sobre el sobreenfriamiento de los metales, con esto se demuestra experimentalmente que los cinco ejes de simetría afectan la metaestabilidad de un líquido (Schülli et al., 2010; Greer, 2010).
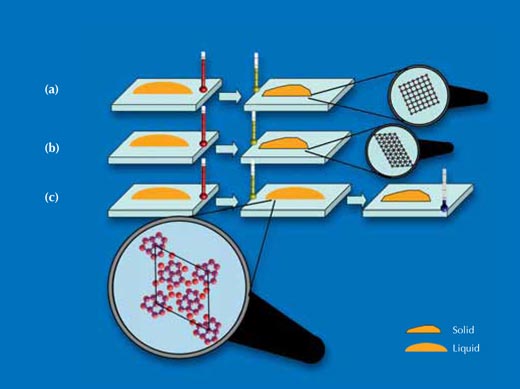
(a) Cuando se cortó el cristal de silicio a lo largo de las facetas cúbicas, los átomos de silicio sobre la superficie que estaba en contacto con la gotita se dispusieron en forma de red cuadrada. Sobre esta superficie, las gotitas se cristalizaron aproximadamente a 60 K por debajo de su punto de fusión. Los resultados de los rayos X mostraron que la gotita se había cristalizado con una estructura y orientación similar a la del cristal de silicio sobre el que se había depositado.
(b) Cuando se cortó el cristal de silicio por la diagonal del cubo, los átomos de silicio sobre la superficie que estaba en contacto con la gotita se dispusieron en forma de red triangular. Sobre esta superficie, la gotita se cristalizó aproximadamente a 70 K por debajo de su punto de fusión. Los resultados de los rayos X mostraron que la gotita también se había cristalizado con una estructura y orientación similar a la del cristal de silicio sobre el que se había depositado.
(c) El cristal de silicio fue cortado de la misma manera que en b), pero se le realizó un tratamiento especial a alta temperatura que causó la formación de una disposición atómica pentagonal de los átomos de oro vinculados a la superficie de silicio. Sobre esta superficie, las gotitas permanecieron en su fase líquida metaestable hasta 120 K por debajo de su punto de fusión – sobreenfriamiento profundo.
Imagen cortesía de Tobias Schülli
Experimente con el sobreenfriamiento
Coloque una botella de agua mineral sin gas que no haya sido abierta en el congelador durante 1 – 2 horas. Pasado este tiempo, el agua debería estar entre -10 y -5 °C. Como el agua no debería contener impurezas sólidas, todavía estará líquida incluso a esta temperatura; el agua se ha sobreenfriado.
Con cuidado, retire la botella del congelador y luego golpéela sobre la mesa o con su mano. Debería poder ver que el agua se cristaliza (se congela), y la formación de hielo avanza rápidamente por toda la botella. La cristalización es desencadenada por el desplazamiento de la onda expansiva a través del líquido. (La onda expansiva es una explicación posible de por qué los aviones van dejando una estela visible de cristales de agua.)
Esto solamente puede ser logrado en líquidos que no contengan semillas que puedan dar lugar a la cristalización. Es poco probable que esto funcione con agua corriente, ya que puede contener impurezas cristalinas que originen la cristalización llegando al punto de fusión (congelación) del agua.
No deje la botella en el congelador por demasiado tiempo, porque cuando el agua llega por debajo de entre -10 a -5 °C, se congela, incluso aunque no haya impurezas cristalinas.

References
- Fahrenheit DG (1724) Experimenta & observationes de congelatione aquæ in vacuo factæ. Philosophical Transactions 33: 78-84. doi: 10.1098/rstl.1724.0016
- Frank FC (1952) Supercooling of liquids. Proceedings of the Royal Society 215: 43-46. doi: 10.1098/rspa.1952.0194
- Greer AL (2010) Materials science: a cloak of liquidity. Nature 464: 1137-1138. doi: 10.1038/4641137a
- Descargue el artículo gratuitamente aquí, o suscríbase a Nature hoy: www.nature.com/subscribe.
- Reichert H et al. (2000) Observation of five-fold local symmetry in liquid lead. Nature 408: 839-841. doi: 10.1038/35048537
- Descargue el artículo gratuitamente aquí, o suscríbase a Nature hoy: www.nature.com/subscribe.
- Schülli TU et al. (2010) Substrate enhanced supercooling in AuSi eutectic droplets. Nature 464: 1174-1177. doi: 10.1038/nature08986
- Descargue el artículo gratuitamente aquí, o suscríbase a Nature hoy: www.nature.com/subscribe.
- Turnbull D (1952) Kinetics of solidification of supercooled liquid mercury droplets. Journal of Chemical Physics 20: 411-424. doi: 10.1063/1.1700435
Web References
- w1 –La CEA es la Comisión de energía atómica y energías alternativas de Francia (Commissariat à l’énergie atomique et aux énergies alternatives). Si desea más información, visite: www.cea.fr
- w2 – El European Synchroton Radiation Facility (ESRF) es un instituto internacional de investigación de vanguardia en el estudio de la ciencia con fotones. El ESRF es un miembro de EIROforum, la asociación que publica Science in School. Para obtener más información, visite : www.esrf.eu
Resources
- Para mayor información sobre las nubes, consulte:
-
Ranero Celius K (2010) Clouds: puzzling pieces of climate. Science in School 17: 54-59. www.scienceinschool.org/2010/issue17/clouds
-
Institutions
Review
Uno de los fenómenos extraños de la naturaleza es que, para algunas sustancias, el punto de fusión no siempre es el mismo que el punto de congelamiento. En este artículo, Tobias Schülli nos lleva al mundo de la materia condensada, nos explica la diferencia entre los distintos estados de la materia, y proporciona una explicación de una anomalía aparente: el sobreenfriamiento.
Se puede utilizar este artículo en el aula de varias maneras. Los docentes pueden dar a leer el artículo a los alumnos para luego comenzar una discusión sobre los cambios de estado de la materia y también sobre métodos de investigación modernos en el campo de la física de la materia condensada. Para asegurarse de que los alumnos hayan comprendido el texto, el docente puede hacer preguntas, por ejemplo acerca de las condiciones para el crecimiento de los cristales.
Además, este artículo podría inspirar a algunos lectores a desarrollar su propio material educativo sobre el sobreenfriamiento.
La sencilla actividad para el aula que contiene el artículo también puede mostrarles a los alumnos que no es sólo la temperatura lo que determina el estado de la materia.
Vangelis Koltsakis, Grecia
