Almidón: un misterio estructural Understand article
Traducido por Liliana Olazar. Una cadena de moléculas de glucosa: almidón. Suena simple, pero no lo es. Dominique Cornuéjols y Serge Pérez exploran las complejidades de su estructura - y demuestran que el misterio no está resuelto.

Klement / iStockphoto
Tome un puñado de espaguetis y échelo en el agua hirviendo. Las varillas rígidas se convertirán rápidamente en curvas suaves y delicadas, mientras se hinchan. Nosotros aprovechamos este comportamiento de los fideos en agua caliente por supuesto, pero ¿qué está pasando con la estructura íntima de los espagueti para dar lugar a una metamorfosis espectacular?
El comienzo de la respuesta es que la pasta – como el arroz, las papas o el pan – contiene una gran cantidad de almidón. Pero, ¿qué es el almidón? Los gránulos de almidón, que se producen en las plantas a partir de la fotosíntesis de dióxido de carbono, están formados por polímeros de glucosa y sirven como reservas de energía. Hacia el final de la temporada de cultivo, el almidón se acumula en las ramas de los árboles, cerca de las yemas. También se encuentra en frutas, semillas, rizomas y tubérculos. Los gránulos de almidón son muy adecuados para el almacenamiento a largo plazo, debido a que es un material compacto, la sequedad relativa y alta estabilidad.
Sin embargo, esta fuente esencial de energía solamente llega a ser accesible a los humanos una vez que se conoció y dominó el fuego, dado que los gránulos de almidón crudo son demasiado compactos para ser difícilmente digeribles. Para aumentar su digestibilidad, el almidón necesita ser cocinado: sólo cuando ha sido calentado se vuelve soluble y comestible.
La transformación del almidón crudo en agua caliente se llama gelatinización: los gránulos se hinchan y estallan, formando una pasta. Durante el almacenamiento prolongado o refrigeración, la pasta de almidón a menudo se espesa debido a un fenómeno llamado retrogradación. Gelatinización y retrogradación, que corresponden a modificaciones estructurales en los gránulos, afectan el comportamiento del almidón que contienen los sistemas.
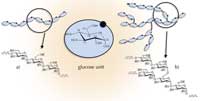
estructurales básicas de
amilosa (a) y amilopectina
(b). Haga clic sobre la imagen
para ampliarla
Imagen cortesía de Serge
Pérez, ESRF
En consecuencia, el almidón es excelente para modificar la textura de muchos procesados y los alimentos cocinados en casa (por ejemplo, como harina de maíz o harina para espesar las salsas) y también ha sido utilizado durante siglos para otros fines, incluida la fabricación de papel, colas o refuerzos de la tela. Hoy en día, las nuevas aplicaciones del almidón son emergentes, incluyendo las fibras de las dietas bajas en calorías, los materiales biodegradables, envases, películas delgadas y materiales termoplásticos.
However, this essential source of energy only became accessible to humans once they had tamed fire, because raw starch granules are so compact that they are hardly digestible. In order to increase its digestibility, starch needs to be cooked: it is only once it has been heated that it becomes water-soluble and edible.
The transformation of raw starch in hot water is called gelatinisation: the granules swell and burst, forming a paste. During cooling or prolonged storage, the starch paste often thickens due to a phenomenon called retrogradation. Gelatinisation and retrogradation, which correspond to structural modifications in the granules, affect the behaviour of starch-containing systems.
Consequently, starch is excellent for modifying the texture of many processed and home-cooked foods (for example, as flour or corn flour to thicken sauces), and has also been used for centuries for other purposes, including the manufacture of paper (sizing), glues or fabric stiffener. Today, new applications of starch are emerging, including low-calorie dietary fibres, biodegradable packaging materials, thin films and thermoplastic materials.
Ciencia: un pequeño paso por vez
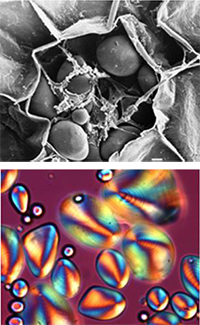
natural de almidón
observado por microscopía
de barrido electrónico b) El
gránulo correspondiente bajo
luz polarizada
Imagen cortesía de Serge
Pérez, ESRF
El almidón, por lo tanto, es ampliamente utilizado en la industria – y lo ha sido durante miles de años. El estudio científico de almidón se inició en 1833 cuando el químico francés Anselme Payen identificó que el almidón está formado por unidades de glucosa. Sin embargo, aún hoy, su bioquímica y la estructura detallada aún no están bien comprendidos. A nivel molecular, sabemos que el almidón nativo (como ocurre de forma natural) está formado por dos componentes distintos, amilosa y amilopectina, que se pueden aislar por fraccionamiento y ser estudiados de forma independiente.
Ambos componentes contienen cadenas de polímeros formados por unidades de glucosa, pero estas cadenas están vinculados de manera diferente. La amilosa es principalmente lineal (con unidades de glucosa unidas por (1-4) (Figura 1a), mientras que la amilopectina tiene muchas ramas, la estructura es muy densa, debido a (1-6) unión (Figura 1b). Amilopectina puede contener hasta cientos de miles de residuos de glucosa y es la mayor biomacromolécula conocida.
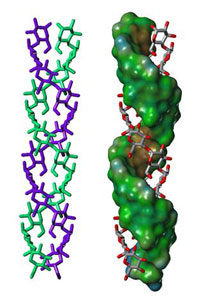
hélice de amilopectina
Imagen cortesía de Serge
Pérez, ESRF
Los gránulos de almidón nativos varían enormemente de forma y de tamaño (desde 0,1 a 200 :m), pero todos tienen una característica común: bajo el microscopio e iluminados con luz polarizada, granos de almidón teñidos con yodo presentan una «cruz de Malta» distintiva lo que indica la existencia de algún orden interno común. Cuando los gránulos se calientan en exceso de agua (como cuando se cocina espaguetis), la “cruz” comienza a desaparecer, lo que demuestra que este orden molecular se está interrumpido.
Las propiedades físicas del almidón – su estabilidad y las transformaciones de fase, por ejemplo, de gránulos de almidón a los geles, o de pasta cruda, quebradiza a la pasta suave, cocinada – están directamente vinculados a este orden molecular. Sin embargo, la comprensión de la estructura detallada del almidón requiere de herramientas de investigación muy avanzadas y técnicas, tales como la cristalografía de rayos X, microscopía electrónica, resonancia magnética nuclear y modelos informáticos.
Con la ayuda de estas herramientas, los científicos están empezando a construir una imagen de cómo almidón – algo que estamos tan familiarizados con – está construido.
Comenzando desde la nanoescala: doble hélices, laminillas y superhélices
Las investigaciones de difracción de rayos X a nivel nanoscópico indican que:
- El almidón está compuesto de finas laminillas (de aproximadamente 4,5 nm de espesor);
- Cada lámina está compuesta por cerca de 100 hélices de doble cadena (o doble hebra) , cada uno con alrededor de 20 unidades de glucosa (Figura 3);
- Las doble hélices son muy densas, con un alto grado de regularidad, como en un cristal (ver glosario de términos en cursiva).
(Para una explicación acerca de cómo se utiliza la difracción de rayos X para analizar estructuras cristalinas, vea Cornuéjols, 2009.)
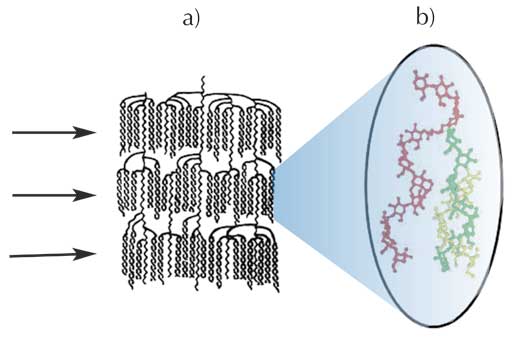
clúster de amilopectina que
muestra tres láminas
(marcados con flechas)
b) el posible enredo entre
una cadena de amilosa (rojo)
y amilopectina hélices dobles
(verde y amarillo)
Imagen cortesía de Serge
Pérez, ESRF

una estructura de superhélice
Imagen cortesía de Serge
Pérez, ESRF
Estos resultados de rayos X corroboran los estudios bioquímicos de la molécula de amilopectina que muestran que esta enorme molécula se organiza en grupos cristalinos de doble hélice (Figura 4a): las láminas reveladas en la investigación de difracción de rayos X consisten en los grupos de dobles hélices demostrados en los estudios bioquímicos. En este modelo, los puntos de ramificación (en los enlaces (1-6)) en las moléculas de amilopectina se encuentran en regiones menos organizadas (o más amorfa) entre los grupos. La amilosa se enreda con la amilopectina (Figura 4b), pero hasta ahora nadie sabe exactamente cómo.
Estudios adicionales de rayos X, utilizando las técnicas de ángulo pequeño y la dispersión de gran angular (SAXS y WAXS) para analizar el almidón hidratado, muestran que las laminillas de dobles hélices son probablemente organizados en una superestructura helicoidal, o superhélice (Figura 5). (Para una explicación de SAXS, ver Stanley, 2009.)
Abajo, desde la microescala: el crecimiento de anillos y “ladrillos” (blocklets)

los anillos que consiste en
capas alternas de regiones
amorfas y semi-cristalina.
Haga clic sobre la imagen
para ampliarla
Imagen cortesía de Serge
Pérez, ESRF
Las estructuras laminares y superhélice de amilopectina son, sin embargo, sólo una pequeña parte de todo el cuadro. En una escala más grande (microscópica), se sabe que los gránulos de almidón están formados por la alternancia de depósitos amorfos y semicristalinos, entre 100 y 800 nm de espesor. Estas estructuras se denominan anillos de crecimiento (Figura 6).
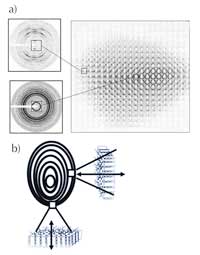
imágenes de difracción
tomadas en diferentes
lugares en el gránulo
(‘mapeo’ del gránulo)
b) La orientación de las
láminas vis-à-vis en la
superficie del gránulo. Haga
clic sobre la imagen para
ampliarla
Imagen cortesía de Serge
Pérez, ESRF
No sabemos casi nada acerca de las partes amorfas de los anillos de crecimiento. Las regiones más cristalinas, sin embargo, pueden ser estudiadas por difracción de rayos-X. Experimentos recientes usando un haz de rayos X muy centrado en un sincrotrón (véase el recuadro) han demostrado que en las regiones semi-cristalinas, las laminillas nanoscópicas son paralelas a la superficie del gránulo de almidón (Figura 7). Esto ha permitido a los científicos establecer el vínculo entre las pequeñas (microescala, por ejemplo, los gránulos de almidón) y la muy, muy pequeño (escala nanométrica, por ejemplo, láminas) – un vínculo que es difícil de obtener en tales investigaciones estructurales.
Otro estudio reciente, utilizando microscopía de fuerza atómica para estudiar la superficie del gránulo de almidón, mostró la presencia de “blocklets” dentro de los anillos de crecimiento. Estos blocklets son más o menos esféricos y tiene un tamaño de 20-100 nm. Hasta ahora, sin embargo, nada más se sabe sobre estos “blocklets”.
Tomando todos los estudios juntos, podemos estar bastante seguros acerca de la estructura a nanoescala (dobles hélices formando láminas) y los anillos de crecimiento (alternando los depósitos amorfos y semicristalinos). Sin embargo, la evidencia de las estructuras intermedias (las superhelices y los “blocklets” (o “ladrillos” ) es menos sólido. Por otra parte, todavía no está claro cómo las superhelices, los blocklets y los anillos de crecimiento se relacionan entre sí. Figura 8 resume los diferentes niveles estructurales (unidades de glucosa, hélices, láminas, superhelices, blocklets y los anillos de crecimiento), desde el molecular (10-9 m) a la microscópica (10-5 m) de nivel.

a) Unidad de glucosa
b) Doble hélice
Comienzo de la página: patrón de difracción de rayos X de la fibra que demuestran una estructura de doble hélice (cortesía de Imberty et al., 1988)
Bottom: model of the double-helix structureAbajo: modelo de la estructura de doble hélice
c) De laminilla
Arriba: Imagen de microscopía electrónica de transmisión de almidón hidrolizado, mostrando la forma de las laminillas cristalinas (cortesía de Angellier-Coussy et al., 2009)
Abajo: modelo de una lámina cristalina formada por unos 100 dobles hélices
d) Superhélice
Comienzo de la página: dispersión de rayos X de pequeño ángulo (SAXS) y dispersión de gran angular de rayos X (WAXS) imágenes de difracción que indica la presencia de una estructura superhélice (cortesía de Waigh et al., 2000)
Abajo: el modelo superhélice, con un campo de 9 nm y un diámetro de 18 nm
e) Blocklets
Arriba: Imagen de microscopía de fuerza atómica de la superficie típica de un gránulo de almidón (cortesía de Gallant et al., 1997). Las protuberancias que se ven en la superficie indican la presencia de blocklets
Abajo: modelo blocklet. Se cree que los blocklets que son más pequeñas en las regiones amorfas (región central) que en las regiones semi-cristalinos (arriba y abajo)
f) Los anillos de crecimiento
Imagen de microscopía electrónica de una sección ultrafina del gránulo de almidón hidrolizado, que muestra los anillos de crecimiento de capas alternas de regiones amorfas y semi-cristalinos (cortesía de I. Paintrand, CERMAV, Grenoble, Francia)
g) Gránulo
Comienzo de la página: gránulo de almidón observados por microscopía de barrido electrónico (imagen grande) y el gránulo correspondiente bajo la luz polarizada (recuadro)
Medio: conjunto de patrones de difracción de rayos X (microfocus)sobre un gránulo de almidón que muestra la distribución y orientación de los campos cristalinos en un gránulo de almidón. Cada patrón de difracción corresponde a un área de aproximadamente de 3 μm2 de la especie y escalones de 7mm que separan los dos patrones (cortesía de Buleon et al., 2009)
Abajo: sección del gránulo de almidón que muestra la orientación radial de los dominios cristalinos (laminillas) en un gránulo de almidón
Haga clic sobre la imagen para ampliarla
Imagen cortesía de Serge Pérez, ESRF
Ya en 1858, el botánico Carl von Nägeli tenía una intuición genial, afirmando que «El grano de almidón… abre la puerta a la creación de una nueva disciplina … los mecanismos moleculares de los cuerpos organizados. «Él, sin duda, no se habría asombrado de que, más de 150 años después, todavía estamos tratando de entender la compleja arquitectura de los gránulos de almidón.
Glosario
Amorfo: Describe un material (o parte del material) que no tiene organización y el orden no.
Cristal: Un cristal perfecto es un material sólido, cuyo constituyentes sean átomos, moléculas o iones se disponen en un patrón ordenado repetir extiende en las tres dimensiones espaciales.
Cristalino: Tiene las propiedades de un cristal, por extensión, caracteriza a las piezas de un material que se piden (por ejemplo, un grupo de hélices dobles, todas incluidas con la misma orientación del eje de la hélice).
Semi-cristalino: Describe un material (normalmente un biopolímero) con ambas partes amorfas y cristalinas.
ESRF
El European Synchrotron de Radiation Facility (ESRF) en Grenoblew1, Francia, es un buen ejemplo de una gran instalación de que opera día y noche en beneficio de miles de usuarios de todo el mundo. Un “usuario” es un científico, por lo general parte de un equipo más grande, que a veces necesita una poderosa herramienta para obtener información sobre una muestra de interés (un polímero, un cristal de proteína, fósiles o una reacción catalítica, por ejemplo).
El ESRF produce rayos X muy intensos, la llamada radiación sincrotrón. Estos haces de rayos X son emitidos por electrones de alta energía, que circulan en un anillo de almacenamiento grandes, 844 metros de circunferencia. El haz de rayos X se dirigen a las líneas de luz que rodean el anillo de almacenamiento en la sala de experimentación. Cada una de las 42 líneas de luz en el ESRF se ha especializado en una técnica específica o tipo de investigación. Para alrededor de media docena de ellos, la especialidad son los polímeros.
En el futuro, la investigación de polímeros se beneficiará de la recién creada Asociación para la Suave Materia Condensada (que incluye polímeros). La introducción de nanorayos (aun más centrados, haz de rayos X nanométricos) pronto permitirá el análisis estructural más fino y el progreso aún mayor en el estudio de los polímeros, incluyendo el almidón.
References
- Angellier-CouReferenciasssy H, et al. (2009) The molecular structure of waxy maize starch nanocrystals. Carbohydrate Research 344: 1558-1566.
 doi: 10.1016/j.carres.2009.04.002
doi: 10.1016/j.carres.2009.04.002 - Buléon A, Véronèse G, Putaux JL (2007) Self-association and crystallization of amylose. Australian Journal of Chemistry 60: 706-718. doi: 10.1071/CH07168
- Cornuéjols D (2009). Biological crystals: at the interface between physics, chemistry and biology. Science in School 11: 70-76. www.scienceinschool.org/2009/issue11/crystallography
- Gallant DJ, Bouchet B, Baldwin PM (1997) Microscopy of starch: evidence of a new level of granule organization. Carbohydrate Polymers 32: 177-191. doi: 10.1016/S0144-8617(97)00008-8
- Imberty A et al. (1988) The double-helical nature of the crystalline part of A-starch. Journal of Molecular Biology 201: 365-378.
 doi: 10.1016/0022-2836(88)90144-1
doi: 10.1016/0022-2836(88)90144-1 - Stanley H (2009) Plasma balls: creating the 4th state of matter with microwaves. Science in School 12: 24-29. www.scienceinschool.org/2009/issue12/fireballs
- Waigh TA et al. (2000) Side-chain liquid-crystalline model for starch. Starch 53: 450-460. doi: 10.1002/1521-379X(200012)52:12<450::AID-STAR450>3.0.CO;2-5
Web References
- w1 – Para aprender más sobre ESRF, ver: www.esrf.eu
Resources
- Para una revisión extensiva del almidón vea científicos de ESRF Serge Pérez y Anne Imberty’s ‘Starch: structure and morphology’ website: www.cermav.cnrs.fr/glyco3d/lessons/starch
- Imberty A, Pérez S (1988) A revisit to the three-dimensional structure of B-type starch. Biopolymers 27: 1205-1221. doi: 10.1002/bip.360270803
- Pérez S, Baldwin P, Gallant DJ (2009) Structural features of starch. In: Starch-Chemistry and Technology, 3rd edition. BeMiller J, Whistler R (eds.). pp149-192. New York, NY, USA: Academic Press. ISBN: 978-0127462752
- Chanzy H, et al. (2006) Morphological and structural aspects of the giant starch granules from Phajus grandifolius. Journal of Structural Biology 154(1): 100-120. doi: 10.1016./j.jsb.2005.11.007
Institutions
Review
La ultra estructura de almidón no se considera a menudo, pero este artículo se describe cómo los componentes del almidón – amilosa y amilopectina – forma los complicados niveles de la estructura dentro del polímero. El artículo puede ser utilizado como trabajo de extensión en una lección sobre la digestión de almidón o de medición. También podría ser utilizado como un ejemplo de la utilización de la técnica de difracción de rayos X o la microscopía de luz polarizada. Se podrían hacer carteles (o tareas foro) sobre los usos del almidón en la industria, cada grupo podría tener un uso diferente. Se podrían investigar los métodos para producir y / o ensayar almidón en la industria. Se podría establecer las preguntas de comprensión, por ejemplo:
- El almidón está formado por dos componentes que son:
- Amilasa y amilopectina
- Amilosa y amilopectina
- Glucosa y amilasa
- Glucosa y amilosa
- Describa que es la gelatinización.
- ¿qué son los anillos de crecimiento en el almidón?
- ¿Cuál es la diferencia entre la amilosa y la amilasa?
- Convierta los tamaños de los diferentes niveles estructurales de 10-9m a unidades más pequeñas por ejemplo micrometros o nanometros.
- La difracción con rayos X fue usada en la década del 50 para determinar la estructura de una molécula bien conocida. ¿qué molécula?
Shelley Goodman, Reino Unido





