Anil: recriando o corante do Faraó Teach article
Traduzido por António Daniel Barbosa. Qual a ligação entre as calças de ganga, caracóis marinhos, a planta pastel-dos-tintureiros e a família real Egípcia? A resposta é o corante anil. Aprenda sobre esta história fascinante e como extrai-lo na sala de aula.

folhas de plantas
Imagem cortesia de: gitane;
fonte da imagem: Wikimedia
Commons
No Egito antigo apenas um barco tinha velas tingidas de púrpura. Pertencia ao Faraó e era um sinal vibrante e poderoso para os restantes utilizadores do Nilo de que deveriam afastar-se para deixar passar o barco real.
Mesmo nos dias de hoje, azul-escuro, púrpura e carmesim são tradicionalmente associados à realeza, magnificência e riqueza. Isto deve-se ao facto de serem cores difíceis e dispendiosas de obter usando corantes naturais. Até ao aparecimento dos corantes sintéticos há 100 anos, os corantes naturais (de fontes animal, vegetal ou mineral) eram a única forma de tingir os tecidos.

real Egípcio com uma vela
imperial púrpura enrolada.
Note que “púrpura” nem
sempre é o que esperamos
nos dias de hoje. Clique na
imagem para aumentar
Imagem cortesia de: dudchik
/ iStockphoto
O púrpura intenso da vela do barco do Faraó era obtido usando anil – um corante natural que pode ser extraído de algumas plantas e animais. Graças ao naturalista Romano Plínio, o Velho (ver caixa sobre Plínio, o Velho), conhecemos ainda os métodos de coloração usados por civilizações antigas. Esta atividade permite aos seus alunos seguir as pegadas destes antigos químicos, extraindo o anil a partir das folhas da planta pastel-dos-tintureiros.
Usando equipamento básico de laboratório, os alunos do secundário de todas as idades podem realizar esta extração em uma ou duas atividades práticas.
Alunos mais novos (idades entre os 11 e 15 anos) podem realizar a extração sem entrar em grande detalhe sobre a reação química [note que o revisor sugeriu que a atividade é apropriada para alunos com mais de 14 anos]. Alunos com mais conhecimentos em química orgânica (idades superiores a 16 anos) poderão investigar os compostos e as reações mais aprofundadamente. A experiência também é relevante em relação ao uso da ciência na indústria e pode ser usada como parte de um projeto sobre este tópico.
Tudo sobre o anil
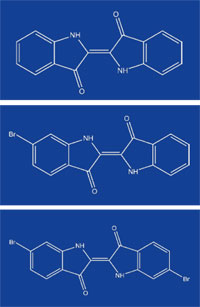
(topo), mono-bromoindigo
(meio) e di-bromoindigo
(fundo). Clique na imagem
para aumentar
Imagem cortesia de: Gianluca
Farusi
Anil é um composto orgânico encontrado em três formas com cores diferentes – o anil em si mesmo, que é azul; o mono-bromoindigo púrpura; e o di-bromoindigo vermelho-púrpura (figura 1). Os corantes derivados de fontes naturais podem conter apenas um destes pigmentos ou uma mistura de dois ou três em proporções variáveis, conduzindo a uma gama de cores desde o vermelho ao azul (Cooksey, 2001). A intensidade da cor é também influenciada pela forma como é processado, bem como se o tecido corado é seco à luz ou à sombra.
Nos tempos do Egito antigo, o anil de melhor qualidade era extraído de caracóis marinhos Murex, que eram comuns nas águas costeiras do Mediterrâneo oriental. Evidências arqueológicas obtidas em Creta sugerem que a extração do anil de caracóis Murex iniciou-se por volta de 2000 a.C. Cerca de 1000 a.C. os Fenícios, uma civilização situada no atual Líbano, exploravam este corante valioso.

brandaris, dos quais as
secreções foram inicialmente
usadas para produzir anil em
2000 a.C.
Imagem cortesia de: H Zell;
fonte da imagem: Wikimedia
Commons
Toda a sua economia era baseada no comércio de púrpura-de-Tiro, um corante violeta-púrpura de anil derivado do caracol Murex brandaris (atualmente conhecido por Bolinus brandaris). Eram tão famosos por isso que o nome Fenício é derivado da palavra grega “phoinísso”, que significa “fazer vermelho”.
O anil derivado de Murex era muito dispendioso porque 12 000 caracóis originam apenas 1,4 g de púrpura-de-Tiro – o suficiente para tingir um lenço de mão. Os compostos usados no fabrico do corante são secretados pela glândula hipobranquial do caracol, encontrada entre as vísceras e o órgão branquial. Os caracóis parecem produzir estes precursores de anil como uma resposta de defesa e pelas suas propriedades antimicrobianas. As secreções frescas são incolores mas escurecem quando expostas ao ar. De acordo com Plínio, o Velho, o corante era extraído esmagando os caracóis, deixando-os putrefazer durante três dias em água salgada alcalina e depois fervendo-os por um período até dez dias – imaginem o cheiro!
Os Fenícios aperfeiçoaram este processo durante centenas de anos e descobriram que variando as espécies de caracóis, métodos de extração e processamento, podiam produzir uma gama de cores desde o vermelho, ao púrpura até ao azul (tabela 1).
| Espécies | Aparência |
Precursores do corante encontrados no organismo |
Nome do corante |
Cor |
Composição química do corante |
|---|---|---|---|---|---|
|
Bolinus brandaris (anteriormente Murex brandaris) |
|
6-bromoindoxil |
Púrpura-de-Tiro / púrpura imperial / argaman |
Vermelho-púrpura |
Principalmente di-bromoindigo |
| Hexaplex trunculus (anteriomente Murex trunculus) |
|
Indoxil e 6-bromoindoxil |
Azul real / tekhelet |
Azul-púrpura |
Mistura de anil, mono- e di-bromoindigo |
|
Indigofera tinctoria ((“anil verdadeiro”) |
|
Indicano | Azul | Blue | Anil |
|
Isatis tinctoria (pastel-dos-tintureiros) |
|
Isatano B |
Azul | Blue | Anil |
Anil de qualidade inferior pode também ser extraído de algumas plantas, sendo que esta técnica precedeu o corante produzido pelos Fenícios a partir de caracóis. Na Índia, métodos para extrair anil do arbusto “anil verdadeiro” Indigofera tinctoria eram conhecidos antes de 2000 a.C.. Na Europa, o corante foi extraído a partir do pastel-dos-tintureiros (Isatis tinctoria). Apesar de estas duas plantas conterem percursores diferentes, indicano no “anil verdadeiro” e isatano B no pastel-dos-titureiros (tabela 1 e figura 2), ambos originavam o mesmo corante – anil.
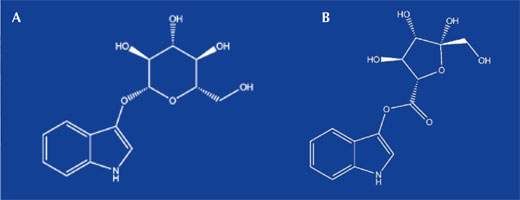
Imagem cortesia de: Gianluca Farusi
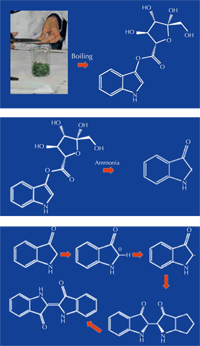
do isatano B a anil. Clique
nas imagens para aumentar
Imagens cortesia de: Gianluca
Farusi
A produção do anil a partir do pastel-dos-tintureiros ocorre em três etapas principais:
- Ferver as folhas para extrair o isatano B solúvel em água (figura 3A; passos 1 a 6 na atividade abaixo).
- Adição de uma base (amoníaco) para hidrolisar a molécula, removendo o grupo carboidrato para originar indolin-3-ona ou o seu tautómero, indoxil (figura 3B; passo 7 na atividade abaixo).
- Exposição do extrato ao ar, conduzindo à sua oxidação e acoplamento de duas moléculas de indolin-3-ona para formar o anil de cor azul (figura 3C; tingindo a lã e obtendo o pó de anil na atividade abaixo).
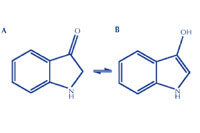
Clique na imagem para aumentar
Imagem cortesia de: Gianluca Farusi
Atividade para os alunos: extraindo anil de folhas de pastel-dos-tintureiros
Materiais
fonte da imagem: Wikimedia
Commons
Para cada grupo de alunos:
- Folhas de pastel-dos-tintureiros (Isatis tinctoria) frescas (suficientes para encher um gobelé de 1 l)
- Sementes de pastel-dos-tintureiros podem ser obtidas facilmente em centros de jardinagem e em alguns países é uma planta comum.
- Solução de amoníaco 20%
- Três gobelés de 1 l
- Água destilada
- Ácido octanóico (opcional)
- Bico de Bunsen e tripé
- Vareta de agitação
- Crivo ou coador
- Provetas e/ou pipetas de 10 ml
- Luvas térmicas
- Funil e filtros de papel
- Faca para cortas as folhas (opcional)
- Lã para corar (opcional)
Eu usei um novelo de lã de tricô e lã áspera acinzentada de ovelha.
Procedimento
- Encher um gobelé com folhas de pastel-dos-tintureiros. Remover as folhas e corta-las em pedaços pequenos.
- Encher dois terços do gobelé com água destilada e levar à ebulição num bico de Bunsen.
-

Anil tingide linho a partir de
1873
Imagem cortesia de: PKM; fonte
da imagem: Wikimedia
CommonsAdicionar alguns pedaços de folhas à água em ebulição, mexer e continuar a aquecer. Quando a água voltar a ferver, adicionar mais algumas folhas. Continue a adicionar folhas e aquecer até que todas tiverem sido adicionadas.
- Quando todas as folhas tiverem sido adicionadas, deixar ferver durante 1 minuto.
- Coar todo o líquido das folhas fervidas para um gobelé limpo.
- Arrefecer o extrato até a temperatura ambiente flutuando o gobelé num tabuleiro raso cheio de água fria, mexendo o extrato e a água do tabuleiro. Agora tem uma solução contendo, entre muitas outras coisas, isatano B, um glicosídeo instável do indoxil.
- Quando tiver arrefecido, meça o volume do seu extrato e adicione amoníaco equivalente a 1% do volume, por exemplo a 1 l de extrato juntar 10 ml de amoníaco; para 100 ml de extrato adicionar 1 ml de amoníaco. A solução deve mudar imediatamente de castanho a amarelo-acastanhado e depois a verde. Agora tem uma solução contendo, entre outras coisas, indoxil.
Para corar lã
Humedeça a lã e coloque-a no extrato durante 10 minutos. Remova e deixe secar ao ar.

pastel-dos-tintureiros a
partir do qual foi extraído
Imagem cortesia de:
naturaldyer; fonte da imagem:
Flickr
Para obter pó de anil
- Areje o extrato vertendo a solução de um gobelé para outro durante 10 minutos.
- Opcional: se se formar demasiada espuma durante o processo de arejamento, adicionar um pouco de ácido octanóico, gota a gota. Este composto atua como surfactante.
- Filtre o extrato através de um filtro de papel para obter o pó de anil.
Para usar o pó de anil como corante, é necessário dissolve-lo em água e misturá-lo com um agente redutor, como o hudrossulfito de sódio (Na2S2O4). Quando o material corado (por exemplo lã) for exposto ao ar, tornar-se-á azul.
Nota de segurança
Lembre-se que o anil e muitos dos seus precursores são corantes, por isso tome cuidado para não os derramar nas roupas ou na pele. Quando manusear soluções de amoníaco concentradas, bem como o anil e os seus precursores, use luvas e óculos protetores adequados e uma hotte. Consulte também as regras gerais de segurança da Science in School.
Perguntas para discussão
- Por que se ferve as folhas? O que acontece?
- O que acontece quando se adiciona amoníaco?
- Durante a secagem, por que aparece a cor azul à medida que a lã seca?
- Quando se produz o pó, o que acontece quando a solução é vertida de um gobelé para outro? Porque precipita o anil?
- Consegues descobrir como é produzido o anil atualmente? Quais são as suas principais utilizações?
Atividades extra
Pode também pedir aos seus alunos para investigarem a química do anil e de outros corantes com algumas das atividades seguintes.
Cálculo do rendimento do anil
Pese as folhas antes da extração e o pó de anil seco. Calcule a percentagem de rendimento de anil: (massa de anil / massa das folhas) x 100. Pode comparar o rendimento obtido usando folhas frescas e folhas secas, ou compare com o rendimento obtido utilizando outras fontes de anil como a Indigofera tinctoria.

SixRevisions; fonte da imagem:
Flickr
Uso do anil como corante
A nossa experiência envolve o uso do anil para corar lã. Pode o anil ser usado para corar outros materiais? Pode comparar materiais naturais como o algodão, linho e seda com sintéticos ou misturas sintéticas (por exemplo poliéster, licra).
A eficácia da produção de anil
- O que produz mais anil, folhas antigas e grandes ou pequenas e jovens? Expresse a quantidade de anil obtido pelo peso e por folha (conte as folhas antes da extração). Qual produz mais anil?
- Cresça plantas com e sem adubo contendo azoto. Aponte para 2 a 4 g de azoto por m2 de solo (vai precisar de calcular a quantidade de fertilizante que produz esta quantidade de azoto). Acrescentando fertilizante com azoto aumenta a quantidade de anil produzido?
- Experimente colocar as plantas no escuro durante alguns dias (cubra-as com um plástico preto). Estas condições têm algum efeito na quantidade de anil produzido? O que se pode concluir sobre o metabolismo do isatano B na planta?
- Investigue o efeito de outros tratamentos na planta ou nas folhas cortadas.
- Teste o efeito de variar o método de extração, por exemplo usando diferentes agentes alcalinos.

Imagem cortesia de: Marcel Douwe Dekker; fonte da imagem: Flickr
Investigação de outros corantes
Os meus alunos produziram corantes a partir de cascas de cebola, de garança (Farusi, 2006), e de bagas de murta. Além disso, testaram a durabilidade da cor desses corantes lavando os materiais corados usando diferentes métodos.
Estudando química com Plínio o Velho

da Naturalis Historia. Clique
na imagem para aumentar
Imagem cortesia de: PHGCOM;
fonte da imagem: Wikimedia
Commons
Esta atividade é parte de um projeto interdisciplinar, desenvolvida juntamente com alunos de 14 e 15 anos de idade, para explorar técnicas cientificas antigas. Plínio, o Velho (23-79 d.C.) foi um autor Romano e naturalista. A sua enciclopédia, Naturalis Historia, agrega muito do conhecimento científico do seu tempo. Iniciamos cada tópico pela discussão de uma passagem da Naturalis Historia e posteriormente delineamos como recriar a experiência descrita ou uma similar.
Desta forma, os alunos começam do mesmo estado pré-científico como Plínio e, através de trabalho de laboratório e discussão, adquirem conhecimento científico moderno em cada um dos tópicos. O processo motivou mesmo os alunos com menos entusiasmo.
Outras atividades neste projeto incluem recriar perfumes antigos (Farusi, 2011), preparação de tessela de vidro com ácido bórico, estimulação de luminescência do molúsculo Pholas dactylus, e preparação de tinta biliar de ferro (Farusi, 2007).
Agradecimento
O autor gostaria de agradecer ao Dr David Hill da Universidade de Bristol, Reino Unido, pelos seus conselhos sobre extração de anil a partir de pastel-dos-tintureiros.
References
- Cooksey CJ (2001) Tyrian purple: 6,6’-dibromoindigo and related compounds. Molecules 6: 736-769.
- Farusi G (2006) Teaching science and humanities: an interdisciplinary approach. Science in School 1: 30-33.
- Farusi G (2007) Monastic ink: linking chemistry and history. Science in School 6: 36-40.
- Farusi G (2011) Cheira como Júlio César: recriando antigos perfumes no laboratório. Science in School 21.
Resources
- Seefelder M (1994) Indigo in culture, science and technology. Landsberg, Germany: Ecomed Verlagsgesellschaft. ISBN 978-3609651606
Review
Neste e noutros artigos da Science in School, Gianluca Farusi mistura com sucesso História antiga e química numa mistura incomum – neste caso, uma atividade prática, simples e inovadora para isolar o corante anil a partir de folhas da planta pastel-dos-tintureiros (Isatis tinctoria). Pela minha experiência, atividades práticas envolvendo cores intensas são uma forma efetiva de atrair a atenção dos alunos.
As atividades adicionais e perguntas suplementares sugeridas no artigo devem ajudar os alunos a obter mais competências práticas e também estimular questões intrigantes, bem como oferecer respostas sonantes.
Vladimir Petruševski, Republica da Macedónia









