Combatendo a malaria numa nova frente Inspire article
Traduzido por Artur Manuel Semedo Rodrigues de Melo. Stéphanie Blandin expõe o seu trabalho sobre a malária a Russ Hodge, do European Molecular Biology Laboratory em Heidelberg, Alemanha – e descreve como se tornou uma bióloga molecular.
O mais próximo que muitos de nós alguma vez estaremos da malária, será uma mão cheia de comprimidos receitados antes de uma viagem a um país tropical, ou histórias de expedições antigas dizimadas por febres misteriosas. Mas a doença apenas parece remota vista dos sofás confortáveis do mundo desenvolvido. Para a maior parte do resto do globo, a malária ainda é um enorme problema. Mata milhões de pessoas em cada ano – na sua maioria crianças em África.
A malaria é causada por um parasita unicelular chamado Plasmodium. Os cientistas acreditam que a forma mais perigosa deste organismo existe há cerca de oito milhões de anos – desde que os humanos se separaram evolutivamente dos macacos. A doença tornou-se, provavelmente, um enorme problema quando os humanos iniciaram a desmatação dos campos para a agricultura, deixando charcos de água estagnada que constituem ambientes ideais de reprodução para os mosquitos, que transmitem o parasita aos humanos com as suas picadas.
No nosso organismo, o Plasmodium infecta as células sanguíneas e reproduz-se, rebentando-as. As proteínas superficiais do parasita alteram-se em cada geração, ajudando-o a escapar ao nosso sistema imunitário. Uma infecção origina febre e frequentemente a morte.
Existem duas formas principais de combater a malária: a primeira é através do ataque aos mosquitos – destruindo os locais onde se reproduzem ou matando-os com pesticidas (tal como o abominável, e praticamente banido, DDT). A segunda solução é tratar os doentes infectados com medicamentos, tal como o quinino, mas o Plasmodium desenvolve resistência aos medicamentos. E o aquecimento global pode devolver a malária a regiões do globo mais frias onde foi quase totalmente eliminada.
Por isso, investigadores como Stéphanie Blandin, no European Molecular Biology Laboratory (EMBL) em Heidelberg, Alemanha, têm utilizado novas abordagens científicas para solucionar o problema. Estudos com Plasmodium podem revelar fraquezas no organismo que podem ser atacadas com medicamentos. Uma outra abordagem, em que Stéphanie está particularmente interessada, poderá ser realizar a luta no interior do mosquito. A malária também faz os insectos adoecer e curá-los poderá ser tão eficaz como parar o organismo no interior do corpo humano – talvez mais.
Stéphanie sempre quis ser cientista. O pai é um criador de gado e cultiva cereais na região francesa da Borgonha; os tios produzem vinho; a mãe é enfermeira. “Em casa, havia revistas por todo o lado; recordo-me especialmente de uma revista sobre a investigação do cancro,” diz ela. “Quando era muito pequena, gostava de ver as imagens. Gostava dos frascos, das provetas e do equipamento de laboratório. Gostava das cores azuladas e violetas estranhas – as cores dos géis que usamos nas experiências. Mais tarde quando aprendi a ler, gostava dos nomes estranhos das substâncias referidas nas revistas.
Na escola, Stéphanie gostava de matemática e diz que provavelmente se teria formado em matemática, se não fosse bióloga. Gostava da quinta e do ar livre, colocando a possibilidade de prosseguir os estudos em ciências agrárias. Estudou biologia de plantas e animais na prépa – a escola que alguns alunos franceses frequentam antes da escola secundária, para se prepararem para as grandes écoles onde aprendem ciências e outras áreas.
Finalmente, decidiu concentrar-se na biologia. “Mas primeiro quis ver como era o trabalho de laboratório no mundo real. Também quis aprender melhor inglês.” Stéphanie passou algumas semanas num laboratório no EMBL. Depois, quando surgiu uma oportunidade para frequentar um curso prático no laboratório de Max Cooper, na Universidade do Alabama, atirou-se à possibilidade de ir para os EUA. Cooper estava a trabalhar num problema fascinante: como é que sinais moleculares activam células indiferenciadas para se transformarem em células especializadas do sistema imunitário. Após seis meses no Alabama, ficou ’presa’.
Stéphanie sente-se perfeitamente à vontade em frente a um microscópio, montando uma preparação e ajustando a focagem com uma rotação rápida da mão. Afasta-se um pouco e deixa-me observar. Alguns dias atrás, um rato tinha sido picado por mosquitos Anopheles e estamos a observar amostras do seu sangue. O campo de visão está cheio de glóbulos semelhantes a pérolas – glóbulos vermelhos – e quando Stéphanie me indica o que devo procurar, até eu consigo ver que o rato tem malária. Algumas das células estão misturadas com pontos negros, originados pela utilização de um corante que indica a presença do parasita.

A parte mais difícil do seu trabalho é infectar ‘bonitos ratos brancos’ com malária, diz ela. “Mas é necessário. Quando vemos uma criança a sofrer com esta doença horrível… essa visão nunca mais se esquece. O facto do parasita estar a criar resistência aos medicamentos coloca mais alguns milhões de pessoas em risco e vamos precisar de novos métodos para o combater. Obriga-nos a trabalhar mais e ajuda-nos a tomar algumas destas difíceis decisões.”
Agora que já mostrou que os ratos tinham sido infectados, Stéphanie vai tentar infectar uma nova série de mosquitos. Divide os insectos por três recipientes que ela própria construiu – “casas de mosquitos” – pois existem pequenas diferenças entre os três grupos. Deixa que todos se alimentem dos ratos infectados – que foram temporariamente adormecidos – na esperança de observar diferenças na sua capacidade de transmitir a doença.
“Quando comecei a trabalhar nesta área, não se conhecia quase nada acerca do sistema imunitário dos mosquitos – não se tinha sequer a certeza que tinham sistema imunitário,” afirma Stéphanie. “Havia bons motivos para se pensar que tinham, porque se sabe que vários outros insectos apresentam um sistema imunitário simples, e os mosquitos estão evolutivamente relacionados com eles. Algumas moscas, por exemplo, produzem proteínas que as protegem de algumas bactérias. Elena Levashina, a minha supervisora no laboratório, descobriu dois tipos de moléculas, chamadas tioester proteínas [TEPs], no mosquito. O meu trabalho era encontrar mais, e descobrir se estavam relacionadas com o sistema imunitário do mosquito.”
Alguns mosquitos pareciam ser capazes de combater a malária: investigadores descobriram uma estirpe de Anopheles que era incapaz de transmitir a doença. “Esta estirpe de mosquito invulgar é tão parecida com a normal, transmissora da doença, que pensamos que apenas algumas mutações genéticas – talvez apenas uma – lhe conferem a protecção,” diz Stéphanie. “Uma única proteína deve estar a matar o parasita no interior do corpo do mosquito.”
No espaço de dois anos, Stéphanie e os seus colegas, descobriram cerca de uma dúzia de outras moléculas potencialmente relacionadas com o sistema imunitário. Estudos recentes mostraram que as TEPs ajudam as células do mosquito a matar bactérias – poderão as moléculas ajudar também na luta contra a malária? “Não podemos estudar parasitas e células de mosquito em tubos de ensaio,” refere Stéphanie, “por isso tivemos de realizar os estudos directamente no corpo do mosquito.” A equipa discutiu como iriam realizar as experiências, sabendo que estavam a dirigir-se para a fronteira da tecnologia genética.
“Noutros organismos, existem métodos que permitem desactivar ou activar moléculas,” diz Stéphanie. “Este tipo de engenharia genética é muito útil para a investigação destes problemas – podemos pegar na estirpe imune e desactivar uma das suas proteínas. Se o mosquito passar a conseguir transmitir a malária, o que não conseguia fazer antes da alteração, ficamos a saber que essa molécula específica estava a ajudar a protegê-lo.”
Infelizmente, estes métodos ainda não foram desenvolvidos para terem sucesso nos mosquitos. Um novo método estava a ser usado em vermes e outros organismos para desactivar proteínas específicas; envolvia a injecção dos animais com versões ligeiramente modificadas de uma das suas moléculas. Para produzir proteínas, as células sintetizam moléculas molde chamadas ARN. Os cientistas descobriram que a injecção de células com uma versão modificada da molécula molde para uma proteína específica, bloqueava a produção dessa proteína. Assim, Stéphanie tentou o mesmo método (chamado ARN de interferência, ou ARNi) no mosquito, e descobriu que funcionava bastante bem. Conseguiu injectar mosquitos com ARN modificado, desactivando TEPs específicos, na esperança de eliminar a imunidade dos mosquitos resistentes à malária.
“Fiz exactamente o que vos estou a mostrar agora,” diz ela. Na sua primeira ‘casa de mosquitos’, tem o grupo de controlo – insectos normais com capacidade de transmitir a malária. A segunda e terceira casa têm mosquitos naturalmente resistentes. Mas ela injectou-os com ARN, um a um, ao microscópio, bloqueando proteínas cruciais do sistema imunitário. Cada uma das duas estirpes experimentais foi sujeita à desactivação de um TEP diferente. Espera que pelo menos um dos dois tipos de mosquitos alterados seja agora capaz de transmitir a doença.
Após a alimentação dos mosquitos, colocou os ratos adormecidos nas suas gaiolas e os mosquitos bem alimentados na respectiva prateleira. “Agora o parasita tem que crescer e desenvolver-se no interior do mosquito,” afirma. “Temos que esperar alguns dias. A primeira vez que fizemos isto, eu estava bastante excitada.”
Aquilo que Stéphanie gosta mais na ciência é a liberdade. Podemos estabelecer o nosso próprio ritmo e trabalhar nas horas que preferirmos – normalmente muito. Gosta de chegar à tardinha: horas calmas, quando a maior parte das pessoas já foi para casa – é nesta altura que realiza a maior parte do trabalho. Frequentemente chega ao laboratório ao meio-dia e fica até às duas ou três da manhã. “Torna-se um pouco mais difícil quando o nosso companheiro também é um cientista,” diz Stéphanie; o seu marido também trabalha no EMBL. “É preciso organizar um plano de trabalho comum.”
Alguns dias após a minha primeira visita, ela dirige-se à sala refrigerada anexa ao laboratório de Fotis C. Kafatos, onde tem trabalhado nos últimos anos. Os mosquitos que tinha infectado alguns dias atrás estão no gelo. Abaixo de certa temperatura, os insectos entram num estado de dormência no qual conseguem sobreviver alguns dias. Vai agora dissectá-los e pesquisar vestígios de Plasmodium.
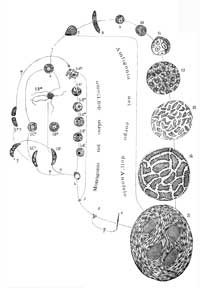
Com alguns movimentos hábeis, ao microscópio, retira o intestino do mosquito, um tecido branco fibroso que se assemelha a uma versão minúscula do nosso intestino. A refeição de sangue passa através do intestino enquanto o mosquito digere o alimento, e é também aqui que o parasita inicia a sua invasão. Os parasitas de Plasmodium, presentes no sangue, passam através das células que revestem o intestino e deslocam-se pelo corpo do mosquito até atingir as glândulas salivares, conseguindo assim infectar um novo animal ou humano, na próxima vez que se alimenta.
O seu teste teve sucesso. Stéphanie encontra vestígios do parasita vivo em estirpes de mosquitos que normalmente conseguem derrotar o Plasmodium. Desactivando um único tipo de TEP, conseguiu transformar Anopheles não infecciosos em transmissores de malária.
Obviamente o que queremos fazer é exactamente o oposto,” diz ela. “Agora que sabemos que esta proteína específica, a TEP1, é vital para matar o parasita, podemos procurar métodos de a introduzir em mosquitos que actualmente transmitem a doença.” Passarão provavelmente muitos anos, diz ela, até que este trabalho tenha como resultado a cura da malária. Talvez na forma de um ‘spray inteligente’ que aumente a resistência do sistema imunitário do mosquito, ou mesmo produzindo mosquitos geneticamente modificados que possam ser depois largados no ambiente. Antes de qualquer destes factos acontecerem, é claro, os cientistas precisam saber muito mais sobre os mosquitos Anopheles, e apenas agirão após cuidadosos estudos e com o consentimento total dos países afectados.
Ninguém sabe de onde virá o próximo grande acontecimento na luta contra a malária. Mas no passado, as batalhas importantes contra a doença têm sido ganhas pelo combate aos mosquitos. Enquanto a doença existir os insectos continuarão a transmitir a malária, tal como sabem fazer. É razão mais do que suficiente, pensam Stéphanie e os colegas, para atacar o problema com todas as ferramentas que os biólogos moleculares têm actualmente à disposição.
Institutions
Review
Este artigo fala de uma cientista que trabalha num laboratório de biologia molecular, tentando encontrar a cura para a doença mortal da malária. O resultado final é uma história que qualquer cientista – ou quem pensa vir a ser cientista – devia ler. É interessante, optimista e envia uma mensagem de esperança para um mundo melhor. Ao mesmo tempo, levanta várias questões importantes.
À medida que a história de desenrola, o leitor fica com uma visão geral da especificidade da doença: o que a provoca, como se propaga, que esforços têm sido feitos para a combater até hoje, e qual a orientação da investigação actual. Apesar de muita desta informação se encontrar em alguns bons livros de biologia escolares, é aqui apresentada de uma forma interessante e de fácil leitura.
Quando lemos acerca da cientista no artigo, ficamos com uma visão positiva do trabalho dos cientistas: eles têm a possibilidade de trabalhar em centros de investigação por todo o mundo, levando a cabo projectos fascinantes; utilizam técnicas científicas modernas; são livres de organizarem o seu horário de trabalho (bastante sobrecarregado); e, o mais importante, a sua contribuição pessoal pode levar a descobertas de importância mundial, que podem salvar a vida de milhões de pessoas, especialmente crianças.
Talvez o que torna este artigo único seja que, de uma forma simples, apresenta alguns assuntos que preocupam não apenas a sociedade científica mas também os governos, organizações e público em geral. Numa breve nota histórica do aparecimento da malária, o autor sugere que talvez tenha sido a actividade humana, há milhares de anos, que permitiu a evolução de uma doença rara para uma doença assassina em larga escala. Actualmente, a actividade humana, que origina o aquecimento global, pode chegar a levar a doença das regiões tropicais distantes para a proximidade do mundo desenvolvido. O assunto da utilização de animais em investigação laboratorial é também brevemente abordado. Além disso é sugerido que as descobertas científicas devem apenas ser postas em prática após cuidadoso exame de todas as suas consequências.
Este artigo poderá ser usado de várias formas como auxiliar educativo. Além de constituir uma óbvia fonte de informação científica para o professor, poderá ser usado como uma ferramenta de ensino alternativa. Por exemplo, o professor poderá fornecê-lo aos alunos e solicitar-lhes que completem uma ficha de trabalho que sintetize informação científica e permita obter uma perspectiva de como os cientistas no seu dia-a-dia planificam a sua pesquisa.
Michalis Hadjimarcou, Cyprus





