Zmierzmy się z chorobami genetycznymi Understand article
Tłumaczenie Dorotę Lisowską. Sabine Hentze i Martina Muckenthaler opowiadają Lucy Patterson o swojej pracy – wykrywaniu chorób genetycznych i doradztwie dla dotkniętych nimi pacjentów.
alex-mit / iStockphoto
W ramach serii wykładów pod nazwą SET-routesw1Insight Lecturesw2dwójka naukowców z Heidelbergu, Niemcy, opowiedziała o swojej pracy i doświadczeniach w dziedzinie chorób genetycznych: Sabine Hentze, lekarz specjalizujący się w genetyce człowieka i związanym z nią doradztwie, profesor w Centrum Pediatrii w szpitalu uniwersyteckim w Heidelbergu, zajmująca się hemochromatozą, dziedziczną chorobą zwaną też przeciążeniem żelazem (patrz ramka).
Choroby genetyczne wywołane są nieprawidłowościami w kodzie DNA danej osoby. Mogą być to proste błędy, takiej jak np. nukleotydowa mutacja w pojedynczym genie lub bardziej skomplikowane nieprawidłowości, takie jak usunięcie i przeniesienie części lub całych chromosomów.

Martina Muckenthaler (po
prawej)
Zdjęcie dzięki uprzejmości
EMBL Photolab
Nasze DNA jest nieustannie atakowane przez wiele przeróżnych czynników, które mogą powodować mutacje, np. promieniowanie występujące w przyrodzie (eksperymenty związane z promieniowaniem, które można przeprowadzić w klasie – zobacz Peralta & Oliveira, 2009). Poza tym kopiowanie całej sekwencji DNA komórki w trakcie każdorazowej mitozy nie stanowi procesu „odpornego na awarie”. W rezultacie, każda komórka w naszym organizmie posiada flotę enzymów naprawczych DNA, które nieustannie łatają uszkodzenia. Jednakże od czasu do czasu mutacjom udaje się uniknąć owego procesu naprawczego i stają się stałą częścią DNA.
Jeżeli takie mutacje wystąpią w obrębie genów o dużym znaczeniu, mogą wywołać poważne choroby. Ze względu na to, iż posiadamy dwa egzemplarze każdego genu (jeden pochodzący od matki a drugi od ojca), mutacje, które uszkadzają tylko jedną kopię genu niekoniecznie muszą wywołać natychmiastowe objawy. Wciąż przecież mamy tę drugą zdrową kopię.Tak naprawdę, może nawet nie jesteśmy świadomi tego, że wszyscy posiadamy od pięciu do dziesięciu takich recesywnie zmutowanych genów. W przypadku gdy jedna kopia genu zostaje uszkodzona, jedynie mutacje dominujące objawią się pod postacią choroby. Jednakże mutacje recesywne mogą okazać się problemem.
Dzieje się tak w przypadku, gdy oboje rodziców są nosicielami tego samego zmienionego genu: istnieje wówczas ryzyko, iż dziecko odziedziczy obie kopie genu. Może to doprowadzić do takich chorób jak zwłóknienie wielotorbielowate czy niedokrwistość sierpowata.
W przypadku gdy zostają utracone lub zamienione całe grupy chromosomów lub gdy chromosomy zostają zduplikowane lub usunięte, aberracje te bardzo często są śmiertelne. W ich rezultacie najczęściej płód obumiera. Często aberracje te prowadzą też do upośledzenia umoślowego i do innych deformacji, tzw. zespołów, np. do zespołu Downa.
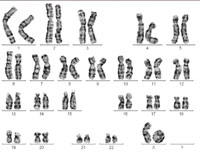
kobiety. Jeden z
chromosomów X tworzy tzw.
chromosom pierścieniowy
powodując zespół Turnera.
Kliknij na obrazek aby
powiększyć
Zdjęcie dzięki uprzejmości
Sabine Hentze
Można również odziedziczyć podwyższoną podatność na te choroby. Pewne mutacje, choć właściwie nie wywołują chorób, radykalnie zwiększają ryzyko zachorowania na poszczególne choroby: na przykład, mutacje dziedziczone w genach BRCA1 i BRCA2 prowadzą do podwyższonego ryzyka wystąpienia raka piersi.
W ramach swej pracy Sabine bada i diagnozuje u swoich pacjentów właśnie takie rodzaje chorób: „Typową sytuację jest, gdy rodzice przychodzą do mnie ze swym dzieckiem mówiąc, że np. ich syn nie rozwija się prawidłowo jak na swój wiek. Syn naszej sąsiadki, który jest w tym samym wieku jest o wiele wyższy i już raczkuje. Nasz jeszcze tego nie potrafi. Sabine dodaje, iż istnieje wiele narzędzi i badań, które pomagają zdiagnozować chorobę: Po pierwsze, w szpitalach takich jak nasz jesteśmy my, lekarze, do nas należy wysłuchanie, zbadanie i ocenienie stanu pacjenta.” Po przeprowadzeniu dokładnego badania klinicznego jak i szczegółowego wywiadu rodzinnego Sabine jest już w stanie odgadnąć, co może być bezpośrednią przyczyną stanu zdrowia u danego pacjenta. Następnym krokiem jest ustalenie, który rodzaj mutacji leży u podstaw choroby.
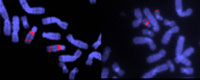
związały się z określonymi
sekwencjami DNA. Zwróć
uwagę na delecję w
chromosomie 22 w próbce po
prawej stronie. Wywołuje to
zespół DiGeorge’a, który
charakteryzuje się aplazją
(niewykształceniem się)
grasicy i gruczołów
przytarczycznych, co
skutkuje zaburzoną
odpornością, niskim
wzrostem i deformacjami
twarzy, serca i dużych naczyń
Zdjęcie dzięki uprzejmości
John Crolla, Wellcome Images
Chromosome analysis was first used by French geneticist and paediatrician Jérôme Lejeune, who in 1959 determined that children suffering from Down syndrome had an extra copy of chromosome 21. Even today, there are many questions that can be more fully answered using this technique than with a genetic test: cells taken from a patient are cultured in the lab, then fixed, prepared and stained so that their chromosomes can be studied under the microscope.
Jednkaże niektóre choroby wywoływane są w skutek zmian w układziechromosomów lub ich wypadnięcia (delecji), które to mutacje są zbyt małe, by mogły zostać dostrzeżone przy pomocy konwencjonalnej analizy chromosomowej. Dlatego też stosuje się metodę zwaną FISH (fluorescent in situ hybridisation – fluorescencyjna hybrydyzacja in situ). Maleńkie, oznakowane barwnikami fluoroscencyjnymi sondy DNA mają albo krzyżować się z, albo dołączyć do określonej sekwencji w obszarze chromosomu, który uważa się za zaatakowany. Następnie lekarze sprawdzają, czy i gdzie połączyły się sondy w próbce chromosomów pacjenta.
Więc kiedy stosuje się badania genetyczne? Sabine mówi, że „wykonuje takie testy, gdy widzi wyraźne przesłanki świadczące o danej chorobie, o której wiedzą, że związana jest z danym genem i możliwą mutacją.
Hemochromatoza, choroba, w której specjalizuje się Martina, jest nie tylko najczęstszą chorobą dziedziczną występujacą na Zachodzie, ale też w 85 – 90% przypadków choroby w Europie Środkowej wywoływana jest przez specyficzną, pojedynczą mutację w genie HFE (zobacz na ramkę poniżej). If patients seem to be suffering from the disease or are concerned that it runs in their family, it is possible to carry out a genetic test to look for HFE mutations. The patient’s DNA is isolated, usually from a blood sample, and the nucleotides of the HFE gene in which the most common point mutations occur are sequenced, and compared with the sequence found in healthy individuals.
Hemochromatoza
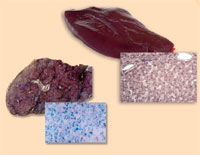
hemochromatoża (po prawej),
w porównaniu ze zdrową
wątrobą (po lewej).Zwróć
uwagę na nadwyżki żelaza
(zabarwione błękitem
pruskim)
Zdjęcie dzięki uprzejmości
Martina Muckenthaler
Hemochromatoza jest najczęstszą chorobą dziedziczną występującą w Europie Zachodniej. Jest to schorzenie powodujące, że organizm pochłania z dostarczanego pokarmu niebezpiecznie wysokie ilości żelaza magazynując je w wątrobie, sercu, trzustce i innych tkankach. Poza brązowych przebarwień na skórze, może doprowadzić do niewydolności wątroby, serca czy cukrzycy, gdyż człowiek, tak jak większość zwierząt, nie potrafi pozbywać się z organizmu nadwyżek żelaza.
Żelazo stanowi istotny składnik hemoglobiny, cząsteczki odpowiedzialnej za transport tlenu w obrębie krwinek czerwonych. Poza tym, jest kofaktorem dla cytochromów, białek bardzo ważnych w produkcji energii w łańcuchu oddechowym każdej z komórek. W przeszłości zauważono, iż wówczas bardzo popularna technika upuszczania krwi przy wykorzystaniu pijawek łagodziła objawy choroby. Prawdą jest, iż technika ta w dzisiejszych czasach pozostaje podstawą w leczeniu hemochromatozy, choć już bez wykorzystania pijawek.
Synteza nowych krwinek czerwonych pomaga w zużytkowaniu nadmiaru żelaza. Początkowo uważano, iż choroba dotyka tylko mężczyzn ujawniając się, gdy osiągali oni wiek średni (40-50 lat). Jednakże obecnie wiemy, że zarówno kobiety mogą zachorować na tę chorobę, z tym, że utrata krwi w trakcie miesiączkowania i ciąży pomaga w sposób naturalny złagodzić symptomy.
Na 85-90 % przypadków w Europie Środkowej, hemochromatoza wywoływana jest przez jedną specyficzną mutację w obrębie genu HFE, zlokalizowanego w chromosomie 6. Uważa się, iż mutacja ta po razp ierwszy wystąpiła u osobnika plemiona celtyckiego zamieszkującego dolinę Dunaju, skąd mutacja rozprzestrzeniła się po całej Europie a następnie wraz z emigrantami do Ameryki i Australii. W Australii wszyscy chorzy wywodzą się od jednego imigranta będącego nosicielem owej mutacji. Jedna osoba na osiem w Europie Zachodniej nosi tę mutację, aczkolwiek ze względu na to, że jest ona recesywna zaledwie jedna osoba na 250 może przejawiać symptomy hemochromatozy.
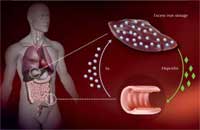
wystarczająco uaktywniana u
ludzi z hemochromatozą, co
prowadzi do nadmiernego
pobierania żelaza w jelitach i
magazynowania zbyt dużych
jego ilości w wątrobie. Kliknij
na obrazek aby powiększyć
Zdjęcie dzięki uprzejmości
Martina Muckenthaler
Badacze, tacy jak Martina Muckenthaler, uważają, iż możliwym jest, że mutacja HFE rozprzestrzeniła się na taką skalę, że nabrała cech selektywnych:” Patrząc wstecz, kobiety rodziły wiele dzieci. Zarówno rozwijające się dziecko jak i sam poród przyczyniające się do utraty pewnej ilości krwi pomagały pozbywać się nadmiaru żelaza. Poza tym, ludzie nie jedli zbyt dużo mięsa, które zawiera najwięcej żelaza w naszej diecie. Zatem niełatwo było uzupełnić zapasy żelaza. Ponadto, w przeszłości ludzie nie żyli tak długo jak w dziesiejszych czasach, więc choroba mogła nawet nie zdążyć się rozwinąć. Oznacza to, że mutacja genu HFE miała swoją dobrą stronę pod względem selekcji naturalnej: ludzie z tą mutacją byli zdolni do udanej reprodukcji w większym stopniu niż ci nieposiadający genu zmutowanego.”
W jaki sposób mutacja ta przyczynia się do podniesienia poziomu żelaza? Organizm wchłania żelazo w jelitach poprzez wyspecjalizowane białko transportowe. Nastepnie żelazo magazynowane jest w komórkach wątroby powiązanych z białkami odpowiedzialnymi za magazynowanie żelaza, tzw. ferrytynami, aż do momentu gdy zajdzie potrzeba uruchomienia zasobów żelaza. Zbyt duża ilość żelaza może doprowadzić do produkcji rodników tlenowych niszczących komórki i powodujących ich obumieranie.
By upewnić się, iż nie występuje nadmiar żelaza, wątroba mierzy jaka ilość żelaza jest dostępna w danej chwili i przekłada tę informację na produkcję hormonu zwanego hepcydyną – im więcej żelaza, tym więcej hepcydyny. W jelitach hepcydyna niszczy białka odpowiadające za transport żelaza, by zapobiec pobieraniu coraz większej ilości żelaza.
Martina utworzyła specjalną mikromacierz składającą się z 500 genów związanych z metabolizmem żelaza i wykorzystującą organizm myszy jako organizm modelowy. Za pomocą tej metody jej zespół porównał genową działalność komórek wątroby u zdrowej myszy z działalnością komórek wątroby u myszy z wszczepioną mutacją HFE powodującą hemochromatozę u ludzi. Odkryli, iż w obecności mutacji HFE hepcydyna nie jest uaktywniania w wystarczającym stopniu, nawet wówczas gdy jest już wystarczająco dużo żelaza w organizmie, co powoduje ciągłe jego pobieranie. W swoich badaniach Martina jak i inni badacze starają się dotrzeć do istoty tego procesu.
W przypadku, gdy dziecko cierpi na niespecyficzne upośledzenie umysłowe lub fizyczne, przyczyną tego mogą być mutacje w wielu genach różnych chromosomów. W tym momencie metody barwienia chromosomów nie wykazują wystarczająco wysokiej rozdzielczości, by zidentyfikować wadliwe geny – jednakże, osobne wysekwencjonowanie wszystkich potencjalnie zaatakowanych genów wymagałoby niewiarygodnie dużego nakładu pracy. W takich przypadkach genetycy tacy jak Sabine wprowadzają nowe technologie: metoda microarray (mikromacierzy) (dokładne wyjaśnienie, czym jest metoda microarray i propozycja zastosowania na lekcji, zobacz Koutsos et al., 2009). Mikromacierze w olbrzymim stopniu przyspiesza proces badań genetycznych; ze względu na to, że setki tysięcy obszarów genomu mogą zostać przebadane w tym samym czasie, możliwe jest jednoczesne przebadanie wielu zaburzeń. Naukowcy mają nadzieję, iż w przyszłości możliwym będzie wykształcenie mikromacierzy, za pomocą której będzie można przebadać wszystkie genetyczne choroby i predyspozycje w trakcie jednego szybkiego i prostego testu.
Zdjęcie dzięki uprzejmości
ktsimage / iStockphoto
Żaden rodzic nie chce, by jego dzieci urodziły się obciążone chorobą genetyczną. Aż do dziś badania prenatalne były jedynie po to, by okreslić, czy dziecko urodzi się z jakimś poważnym zaburzeniem. Jednakże, od nadejścia zapłodnienia metodą in vitro możliwe stało się zbadanie genetycznej budowy embriona jeszcze przed jego zagnieżdżeniem w łonie kobiety. Technika ta zwana jest diagnostyką przedimplantacyjną.
Obecnie mamy wiele badań pozwalających na wykrycie znanych chorób genetycznych. Umożliwiają one rodzicom, którzy są w obszarze ryzyka przekazania choroby genetycznej, na wyselekcjonowanie zdrowego embriona, który zostanie zagnieżdżony w łonie matki. Pod wieloma względami jest to naprawdę świetna nowina, gdyż oznacza, iż rodzice starający się o dziecko nie muszą przechodzić przez proces badania embriona będącego już w macicy (punkcja owodni, która sama w sobie niesie ryzyko dla życia dziecka), oczekiwania na wyniki, podejmowania decyzji, czy usunąć ciążę w przypadku złego wyniku.
Im więcej dowiemy się o genetycznych podstawach różnorodnych chorób i cech i im wyższy poziom będą miały metody badania, tym więcej dowiemy się na podstawie takich badań. Oczywiście żaden rodzin nie chciałby, by jego dziecko cierpiało z powodu jakiejkolwiek poważnej choroby – ale co w przypadku mniej poważnych zaburzeń, takich jak hemochromatoza, wrodzona głuchota czy nawet krótkowzroczność? Kto ma nam powiedzieć, że dziecko dorastające z taką wadą nie przeżyje swojego życia w sposób równie pełny jak zdrowa osoba? W istocie, problem ten dotyka kwestii ustalenia tego, co uznaje się za normalne. W którym miejscu narysujemy linię odgraniczającą akceptowalne schorzenia i cechy genetyczne od tych nieakceptowanych? Co więcej, czy rodzice kiedykolwiek powinni mieć prawo wyboru płci dziecka lub jego wzrostu, poziomu inteligencji czy też bycia atrakcyjnym?
ich genetically determined conditions or traits are acceptable and which are not? Furthermore, should parents ever be allowed to choose if their child is male or female, how tall or attractive or how intelligent they are?

jgroup / iStockphoto
Kolejną kwestią związaną z badaniami genetycznymi jest to, czy naprawdę chcemy wiedzieć co nasze geny jeszcze mają dla nas w zanadrzu. Co byś zrobił dowiadując się, że jesteś w grupie najwyższego ryzyko zachorowania na jakąś poważną chorobę? Mógłbyś starać się dostosować swój tryb życia, by w ten sposób opóźnić jej początek czy zmniejszyć jej objawy. Jednak co byś czuł wiedząc o grożącym ci niebezpieczeństwie? A co gdyby firmy ubezpieczeniowe lub twój przyszły pracodawca mieli pełny dostęp do takiej informacji? Co jeżeli zaistniałoby ryzyko, że możesz przekazać tę chorobę swoim dzieciom? Twój parner chciałby być tego świadomy? Czy mogłoby to wpłynąc na jego uczucia wobec ciebie? Propozycje rozbudzenia dyskusji na te tematy wśród uczniów, zobacz Strieth et al. (2008).
To właśnie w tym momencie praca doradców genetycznych, takich jak Sabine Hentze, nabiera wyjątkowego znaczenia: „Poza moją pracą w laboratorium większość mojego czasu spędzam na udzielaniu porad pacjentom, innymi słowy na komunikacji: co oznacza taki a taki wynik badania? Co oznacza on dla mnie, dla naszego dziecka, dla naszej rodziny, dla naszej przyszłości?”
To właśnie dzięki pracy doradców genetycznych uświadomiliśmy sobie, że najprawdopodobniej jednym z najważniejszych względów, pod kątem którego powinno rozważyć się kwestię badań genetycznych , jest to, że ludzie również mają prawo nie wiedzieć.
References
- Koutsos A, Manaia A, Willingale-Theune J (2009) Fishing for genes: DNA microarrays in the classroom. Science in School 12: 44-49. www.scienceinschool.org/2009/issue12/microarray
- Peralta L, Oliveira C (2009) Radioactivity in the classroom. Science in School 12: 57-61. www.scienceinschool.org/2009/issue12/radioactivity
- Strieth L et al. (2008) Meet the Gene Machine: stimulating bioethical discussions at school. Science in School 9: 34-38. www.scienceinschool.org/2008/issue9/genemachine
Web References
- w1 – By uzyskać więcej informacji na temat organizacji SET-routes, promującej kobiety w różnych dziedzinach nauki, odwiedź www.set-routes.org
- w2 – SET-routes Insight Lectures to seria interaktywnych wykładów naukowych, które można wykorzystać na lekcji. Zaprezentowane przez wyjątkowe kobiety nauki, wykłady te wprowadzają w ekscytujący świat nauki, inżynierię i technologię (SET), dotykając dziedzin nawet tak odległych jak nauka o kosmosie; zmiany klimatyczne, doradztwo genetyczne, hemochromatoza i mikromacierze DNA; malaria, komórki macierzyste i ich odbudowa; aracheologia Wszechświata; i kosmologia. Odwiedź: www.set-routes.org/lectures
Resources
- Gry Democs ułatwiające debatę nad diagnostyką preimplantacyjną i dostępnymi bez ograniczeń badaniami genetycznymi mogą zostać pobrane na tej stronie: www.neweconomics.org/gen/democs.aspx
- Artykuł o Democs w ramach Science in School:
- Smith K (2007) Democs: a conversation card activity for teaching science and citizenship. Science in School 4: 27-19. www.scienceinschool.org/2007/issue4/democs
- The Genes to amerykański portal oferujący krótkie filmy i ćwiczenia na temat chorób dziedzicznych, zobacz: www.genesareus.org
- By uzyskać wstępne informacje na temat najczęstszych chorób genetycznych, odwiedź Genetic Disorders Library (http://learn.genetics.utah.edu/content/disorders/whataregd) zakładka Learn.Genetics (http://learn.genetics.utah.edu), the Genetic Science Learning Center from the University of Utah, USA.
- By dowiedzieć się więcej na temat rodników tlenowych w naszym organizmie i jak je zneutralizować, odwiedź: Farusi G (2009) W poszukiwaniu jedzenia z przeciwutleniaczami. Science in School 13. www.scienceinschool.org/2009/issue13/antioxidants/polish
- Gdy ten artykuł jedynie pobudził twój apetyt, przydać może ci się kolejny na temat najbardziej przełomowych odkryć i opinii o badaniach genetycznych i o genomice na blogu Daniela MacArthura, Genetic Feature: http://scienceblogs.com/geneticfuture
- Jeżeli blog ten okazał się interesujący i pomocny, zapraszamy do przejrzenia artykułów medycznych na Science in School. Odwiedź: www.scienceinschool.org/medicine
Review
Choroby dziedziczne pełnią kluczową rolę w temacie genetyki: temat odnosi się do każdego ucznia i zachęca go do wciągnięcia swej rodziny do 'badania drzewa genealogicznego'. To zapoczątkuje jeszcze więcej dyskusji wśród uczniów, zwłaszcza w przypadku gdy uczniowie ci będą przygotowani do rozmowy o rzadkich chorobach czy aberacjach chromosomowychwystępujących w ich rodzinach. Hemochromatoza to temat, którego nie można omijać, gdyż z medycznego punktu widzenia jest to choroba wyleczalna, pod warunkiem że zostane odpowiednio wcześnie zdiagnozowana. Jest również dobry przykład ewolucyjnego postepu, który może doprowadzić do ślepego zaułku, gdy środowisko ulegnie zmianom. To zapowiedź naprawdę wielu ciekawych dyskusji.
Ponadto artykuł ten opisuje wszystkie główne techniki obecnie stosowane do analizy wad wrodzonych, wraz z przełomową metodą mikromacierzy.
Proponowane tematy dyskusji to: ogólnie etyka w genetyce; zapłodnienie in vitro; genetyka preimplantacyjna; planowanie rodziny w przypadku chorób genetycznych; kwestia, kiedy zaczyna się życie. Wszystkie te tematy powiązane są z zagadnieniami etyki i religii.
Oto kilka propozycji zadań dla uczniów, przy wykorzystaniu powyższego artykułu:
- Wypisz w formie tabelki opisywane techniki i ich poziom wykrywania syndromu czy choroby dziedzicznej.
- Omów cechy każdej z technik w odniesieniu do ich znaczenia dla pacjenta.
- Wypowiedz się na temat 'prawa, by wiedzieć' lub 'nie wiedzieć' i etycznego dylematu, przed którym stają lekarze odkrywając poważne mutacje genetyczne.
- Zilustruj za pomocą schematu sekwencyjnego lub rysunków pobieranie żelaza przez organizm człowieka.
- Narysuj diagram przedstawiający wzorzec dziedziczenia mutacji w genie HFE korzystając z genetyki Mendlowskiej.
Friedlinde Krotscheck, Austria





