Ossidoriduzioni cellulari – la chimica della vita Understand article
Tradotto da Francesca Nuzzo. Imparare come dei biosensori fluorescenti possono monitorare la chimica all’interno di una cellula.
Si tende a pensare che le reazioni di ossidoriduzione (redox) siano solo chimica pura. In una cellula vivente, una riduzione consiste in un guadagno di elettroni mentre un’ossidazione é una perdita di elettroni. Le reazioni redox rivestono ruoli importanti in svariati processi biochimici. Un’alterazione dei processi redox cellulari è alla base di diverse malattie, quindi mantenere un equilibrio in tali reazioni é importante per la nostra salute.
Si considerino le seguenti semi-reazioni:
C ⇌ C4+ +4e–
O2+4e– ⇌ 2O2-
Nella prima, il carbonio é ossidato, nell’altra, l’ossigeno é ridotto. Insieme le due equazioni descrivono una reazione redox che potrebbe apparentemente sembrare solo semplice chimica. Tuttavia, tale reazione avviene nel nostro organismo, di continuo.
Una reazione redox tipica
Nelle ossidoriduzioni, gli elettroni vengono scambiati tra specie chimiche. Ad esempio, nella reazione della termite, a volte usata per saldare i binari, gli elettroni vengono ceduti dall’alluminio metallico al triossido di ferro.
Fe2O3(s) + 2Al(s) → Al2O3(s) + 2Fe(l)
La reazione diventa piú chiara se si rimuovono gli atomi di ossigeno dall’equazione:
2Fe3+ + 2Al → 2Al3+ + 2Fe
Si puó notare che gli atomi di alluminio perdono gli elettroni (ossidandosi), elettroni che vengono poi trasferiti agli ioni di ferro del triossido di ferro, riducendolo. Piú in generale, ogni reazione redox consiste di due porzioni: la reazione di ossidazione (nel nostro caso, la coppia Al/Al3+) e la reazione di riduzione (qui, la coppia Fe3+/Fe).
Ossidoriduzioni biologiche
Metabolismo
La reazione della termite dimostra che le reazioni redox spontanee rilasciano energia, che puó essere utile al corpo. Le due semi-equazioni all’inizio dell’articolo sono effettivamente un modo differente di descrivere il metabolismo cellulare. Quando si mangia, il cibo é scomposto in zuccheri, come il glucosio. All’interno della cellula, questi zuccheri vengono ossidati e gli elettroni trasferiti all’ O2. Un modo alternativo di scrivere l’equazione é:
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l) + energia
In questa equazione, 48 elettroni vengono trasferiti dagli atomi di carbonio dello zucchero agli atomi di ossigeno, rilasciando energia utile per supportare altre reazioni di ossidoriduzione. Garantire un equilibrio di tali reazioni é importante per il normale funzionamento cellulare; se l’equilibrio si sposta verso uno dei due sensi della reazione, ci potrebbero essere delle spiacevoli conseguenze, come una patologia.
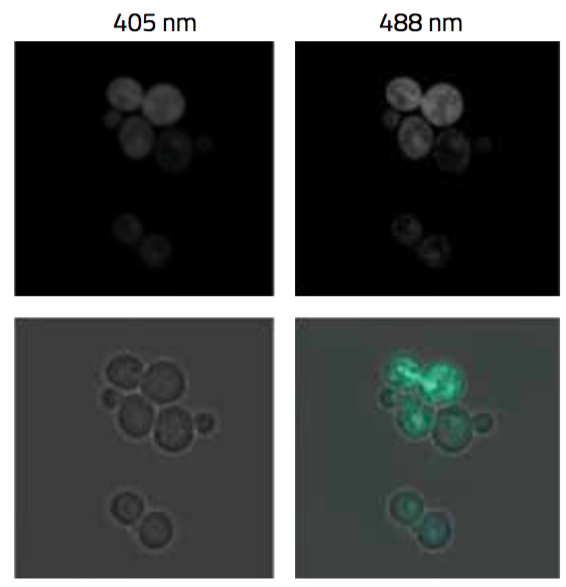
Immagine per gentile concessione di Prince S. Amponsah (DKFZ Heidelberg)
Comunicazioni cellulari
Per lungo tempo, le molecole chimicamente attive, contenenti ossigeno, meglio note come specie reattive dell’ossigeno (ROS), che possono alterare lo stato redox di una cellula, sono state considerate come sottoprodotti indesiderati e dannosi del metabolismo cellulare. Di norma, il citoplasma di una cellula é mantenuto in uno stato ridotto; un cambiamento verso uno stato piú ossidato é alla base di diverse patologie, cancro incluso.w1.
Tuttavia, alcuni ROS ricoprono ruoli positivi come molecole segnale e sono dunque essenziali per la salute dell’organismo. Migliaia di diverse molecole ROS fungono da messaggeri per consentire la comunicazione tra cellule. Ne sono un esempio, il superossido (O2–), il perossido di idrogeno (H2O2) e il monossido di azoto (NO.), la cui produzione é normalmente regolata e che hanno un ruolo in processi, quali cicatrizzazione delle ferite, invecchiamento, infiammazione e morte cellulare programmata (apoptosi).
Ossidoriduzioni e cancro
Nel cancro, le cellule si dividono in maniera incontrollata e le proteine si comportano in modo anomalo, comparendo o scomparendo inspiegabilmente. Le reazioni redox sono coinvolte nello sviluppo del cancro, per esempio danneggiando il nostro DNA, ed é stato anche dimostrato che i ROS possono sia attivare l’espressione di geni le cui proteine promuovono il cancro (oncogeni) o disattivare geni soppressori dei tumori, le cui proteine hanno funzione esattamente opposta. Inoltre, i ROS possono anche ossidare direttamente le proteine, alterandone la loro struttura e quindi funzione. Se queste proteine sono importanti per la divisione o il movimento delle cellule, allora il cancro potrebbe comparire.
Una volta che il tumore si é formato, i meccanismi di ossidoriduzione possono anche essere sfruttati come terapia. Molti farmaci antitumorali colpiscono i tumori intensificando la produzione dei ROS all’interno delle cellule trasformate, uccidendole. Tuttavia, le cellule cancerose di solito aumentano la produzione del loro sistema di difesa antiossidante, controbilanciando cosí l’effetto.
I meccanismi redox possono anche essere responsabili della resistenza alla terapia, quando il trattamento farmacologico disponibile non funziona. Per colpire i tumori efficientemente, questi farmaci usano proteine di trasporto del corpo per raggiungere una specifica localizzazione (ad esempio, laddove si collocano le cellule maligne). Tuttavia, le reazioni di ossidoriduzione potrebbero alterare queste proteine, rendendole non funzionali ed interferendo con la terapia.
Queste sono solo alcune delle ragioni per cui capire le reazioni redox biologiche e come le cellule raggiungono l’equilibrio redox potrebbe aiutare nella lotta contro il cancro.
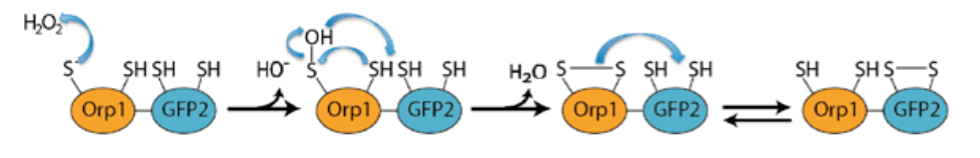
Immagine per gentile concessione di Prince S. Amponsah (DKFZ Heidelberg)
Fare luce sulle reazioni di ossidoriduzioni
Per capire come diversi fattori interagiscono in cellule sane e malate, seguiamo i processi redox nelle cellule usando varianti di una proteina fluorescente di medusa nota come proteina verde fluorescente (GFP). Negli anni ‘60 e ‘70, i ricercatori hanno scoperto la GFP nella medusa Aequorea victoria e l’hanno modificata per produrre diversi colori. Questo lavoro valse un premio Nobel per la Chimicaw2.
Sfruttando la genetica, si può indurre le cellule a produrre biosensori fluorescenti, basati sulla GFP, utili per monitorare lo stato ossidoriduttivo delle cellule. Uno di questi sensori é una variante della GFP detto roGP2, modificabile con diversi segmenti di proteina per raggiungere scopi specifici. Ad esempio, puó esere indirizzato in specifici comparti cellulari (es. citosol o mitocondri) aggiungendo sequenze di trasporto (figura 1). Alternativamente, si può creare un biosensore specializzato per una particolare molecola redox aggiungendo uno specifico segmento di proteina che reagisce con le specie redox.
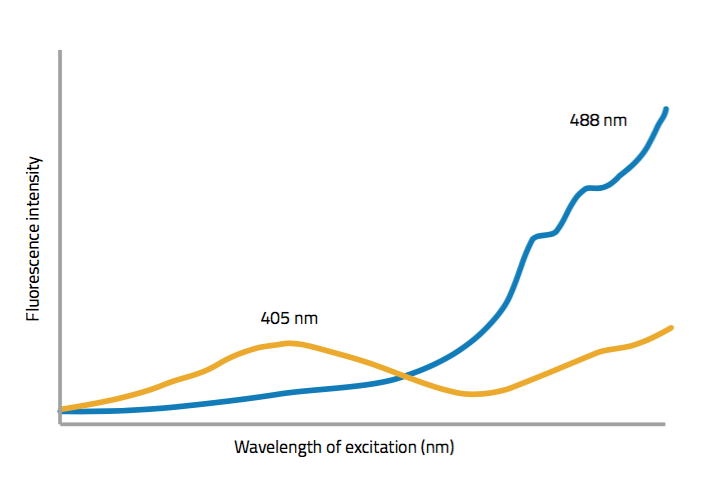
Per misurare i livelli di H2O2 nelle cellule, usiamo il sensore Orp1-roGFP2 (figura 2). Lo zolfo della parte Orp1 del biosensore reagisce con il perossido e la proteina si ossida creando ponti di solfuro che cambiano la forma della proteina e riducono la sua fluorescenza nell’intervallo misurato. (figura 3).
Usando proteine GFP modificate, possiamo osservare in tempo reale dove le specie redox si dirigono nelle cellule e come influenzano o mantengono lo stato redox, sia in individui sani sia in pazienti oncologici. Ciò può aiutare a capire le dinamiche delle nostre cellule quando si é sani o se si sviluppa il cancro. Forse, un giorno, le nostre scoperte potranno suggerire nuovi trattamenti per le malattie.
Web References
- w1 – Il gruppo del professore Tobias Dick presso il Centro Tedesco di Ricerca sul Cancro (DKFZ) studia la regolazione redox in cellule normali e tumorali. Per saperne di più sulla loro ricerca, consultare: www.dkfz.de/en/redoxregulation/index.php
- w2 – Ulteriori informazioni sul Premio Nobel per la Chimica 2008, per la scoperta e lo sviluppo della GFP, sono disponibili sul sito Nobel Prize. Cliccare: http://tinyurl.com/7y8df4s
Resources
- Ulteriori informazioni sulla GFP possono essere trovate qui:
- Furtado S (2009) GFP: la vita dipinta di verde. Science in School 12.
- Per saperne di più sulle reazioni di ossidoriduzione, consultare: http://tinyurl.com/d65vdx6
- Per un attivitá sui geni coinvolti nel cancro, consultare:
- Communication and Public Engagement team (2010) Si può localizzare una mutazione legata al cancro? Science in School 16.
Review
Conoscere le reazioni redox che avvengono nelle cellule viventi é importante per capire molti meccanismi cellulari come invecchiamento, infiammazione, apoptosi e cancro.
Il presente articolo descrive come dei biosensori, la maggior parte dei quali basati sulla GFP, possono essere usati per rilevare il livello delle specie chimiche coinvolte in reazioni redox e capire, dunque, le dinamiche delle nostre cellule.
L’articolo potrebbe essere usato sia per spiegare le tecniche usate in biologia molecolare sia come spunto per discutere sul ruolo degli antiossidanti e della GFP in biologia. Domande sulla compresione dell’articolo includono:
- Nella respirazione cellulare, quali elementi sono ossidati e quali ridotti?
- Dimostrare come 48 elettroni vengono scambiati nella respirazione cellulare.
- Quali sono le specie reattive dell’ossigeno?
- Descrivere i ruoli del superossido, del perossido di idrogeno e del monossido d’azoto nella cellula.
- Descrivere come le specie reattive dell’ossigeno potrebbero essere usate nella terapia per il cancro.
Monica Menesini, Liceo Scientifico A Vallisneri, Italia





