La misura della glicemia: un problema quotidiano dei diabetici Teach article
Tradotto da Monica Mauri. Fred Engelbrecht e Thomas Wendt dell’ExploHeidelberg Teaching Lab descrivono alcuni esperimenti per il dosaggio dello zucchero al fine di far conoscere i problemi che i diabetici affrontano ogni giorno.
Il diabete: una malattia della civiltà moderna
Il monosaccaride glucosio è la più importante fonte di energia negli organismi viventi eucarioti e viene utilizzato dalle cellule nella respirazione aerobica o anaerobica. Esso funge anche da precursore nella produzione delle proteine e nel metabolismo dei lipidi. Quindi, esso è una molecola centrale in alcune vie metaboliche, e la sua concentrazione ematica (glicemia) deve essere rigidamente regolata dall’insulina e dal glucagone.
Il Diabete mellito (o semplicemente diabete) è una sindrome caratterizzata da un alterato metabolismo del glucosio e da eccessivi livelli ematici di zucchero (iperglicemia). Questo è dovuto o a bassi livelli dell’ormone insulina, o ad un’abnorme resistenza all’effetto dell’insulina associata a livelli di secrezione di insulina che sono troppo bassi per poter compensare questa resistenza.
Ci sono due forme principali di diabete: il Tipo 1 ed il Tipo 2. Sebbene abbiano cause diverse, i pazienti di entrambe le forme sono incapaci di produrre, nelle cellule beta del pancreas, quantità di insulina sufficienti ad evitare l’iperglicemia.
Il diabete di Tipo 1 comprende il 10% di tutti i casi di diabete in Europa, ed è caratterizzato dalla perdita di cellule pancreatiche beta, di solito a causa di una distruzione autoimmune. Poiché il Diabete di Tipo 1 spesso affligge pazienti di giovane età, esso viene anche chiamato diabete giovanile. È la forma più grave della malattia, in quanto non esiste una cura. Piuttosto, i pazienti devono adattare il loro stile di vita, per esempio migliorando la loro dieta, facendo esercizio fisico regolare e monitorando i loro livelli di zucchero nel sangue. In aggiunta, per evitare il coma o la morte, sono necessarie iniezioni sottocutanee o continue perfusioni di insulina, mediante una pompa, nel sistema di circolazione sanguigna.
Il diabete di Tipo 2 è dovuto alla resistenza all’insulina o ad una ridotta sensibilità all’insulina nei tessuti bersaglio, combinate con un’insufficiente secrezione di insulina. La diminuita risposta dei tessuti dell’organismo all’insulina quasi certamente coinvolge i recettori dell’insulina nelle membrane cellulari. Questo fa sì che il corpo necessiti di quantitativi di insulina abnormemente elevati per mantenere dei normali livelli ematici di zucchero, ed il diabete si sviluppa quando le cellule beta non possono soddisfare questa richiesta. Il diabete di tipo 2, comunemente noto come diabete dell’età adulta, di solito compare dopo i 30 anni di età. Nella maggior parte dei casi, esso è correlato all’obesità e ad un insufficiente esercizio fisico; adottare uno stile di vita più salutare può migliorare le condizioni o, in alcuni casi, persino portare alla guarigione. Vedere Dugi (2006) per maggiori dettagli sul diabete.
Le persone affette da entrambi i tipi di diabete hanno bisogno di imparare a convivere con i sintomi della malattia. Questi includono frequenti minzioni, aumento della sete e, di conseguenza, un’aumentata assunzione di liquidi. Poiché un gran numero di bambini è affetto da diabete, è essenziale informare gli alunni su questa malattia fin dai primi momenti. I diabetici devono imparare come ridurre al minimo i loro sintomi, o persino a prevenire la malattia adottando una dieta salutare e facendo abbastanza esercizio fisico. I bambini sani dovrebbero comprendere le necessità dei loro amici ammalati.
Noi abbiamo quindi messo insieme alcuni esperimenti che consentano agli studenti di rilevare i carboidrati. Una serie di esperimenti determina se una soluzione contenga o meno amido, proteine, o zuccheri quali glucosio, lattosio o saccarosio. Una volta che gli zuccheri sono stati identificati, ulteriori esperimenti determinano, per mezzo di una reazione enzimatica, quali campioni contengono lattosio o glucosio. Il principio alla base di questi esperimenti è lo stesso dei saggi per la determinazione dei livelli del glucosio nel sangue per la diagnosi del diabete, o per il dosaggio di glucosio e/o lattosio, ad esempio nei succhi di frutta, nel latte e nei latticini. Questi esperimenti, quindi, danno agli studenti un’idea di come i diabetici possano monitorare il loro stato zuccherino.
Esperimento 1: Riconoscimento di zucchero, amido e proteine
Gli studenti ricevono cinque campioni, contrassegnati con le lettere dalla A alla E, contenenti amido, una proteina (sieroalbumina bovina), il monosaccaride glucosio, o i disaccaridi lattosio o saccarosio. Tutte le soluzioni sono alla concentrazione dello 0,1% in acqua. Si potrebbero testare anche campioni di energy-drinks incolori contenenti glucosio (ad esempio Powerade®-Lemon). Usando differenti soluzioni reagenti, gli studenti dovrebbero determinare quali dei cinque campioni contengono zucchero, amido o la proteina.
Per una classe di 30 studenti che lavorino a coppie occorreranno le seguenti soluzioni:
- Una soluzione fresca di reattivo di Fehling, ottenuta mescolando uguali volumi di soluzione di Fehling I di colore blu chiaro (7 g di CuSO4·5H2O sciolti in 100 ml di acqua distillata) e di soluzione di Fehling II incolore (35 g di C4H4KNaO6·4H2O e 10 g di NaOH disciolti in 100 ml di acqua distillata).
- Soluzione di Lugol, ottenuta sciogliendo 1 g di iodio (I2) e 2 g di ioduro di potassio (KI) in 50 ml di acqua distillata.
- Il colorante Coomassie Brilliant Blue per il saggio di Bradford è disponibile in commercio, ad esempio presso la Bioradw1.
a) Riconoscimento di uno zucchero riducente (Reazione di Fehling)
- Pipettare un campione da 1 ml delle soluzioni dalla A alla E in cinque differenti provette, e scaldarne i contenuti a bagnomaria a 60 °C per 2 minuti.
- Aggiungere 16 μl di soluzione di Fehling fresca color blu scuro a ciascuna provetta di reazione e tenere le provette a 60 °C per ulteriori 10 minuti, o fino a quando si osserva una variazione di colore e si forma un precipitato.
Le soluzioni contenenti zuccheri riducenti quali fruttosio, glucosio o lattosio dovrebbero diventare rosse e formare un precipitato rosso (gli ioni rameici disciolti vengono ridotti a ossido rameoso insolubile), mentre non dovrebbe esserci variazione di colore con il saccarosio o l’amido. La soluzione proteica dovrebbe diventare viola pallido.
b) Riconoscimento dell’amido (soluzione di Lugol)
- Pipettare campioni da 500 μl delle soluzioni dalla A alla E in cinque nuove provette distinte.
- Aggiungere 50 μl di soluzione di Lugol a ciascuna provetta e osservare la reazione colorata.
La soluzione di Lugol è un indicatore che serve per identificare l’amido. Il colorante tingerà l’amido non appena esso interagirà con la struttura attorcigliata del polisaccaride, dando luogo ad una colorazione blu intenso. Esso non reagirà con i monosaccaridi (glucosio) o i disaccaridi (lattosio o saccarosio).
c) Riconoscimento della proteina
Il saggio delle proteine è basato sul procedimento legante del colorante di Bradford, che determina il cambiamento di colore del colorante Coomassie Brilliant Blue quando esso si lega alle proteine.
- Pipettare un campione da 20 μl delle soluzioni dalla A alla E in cinque nuove provette, quindi aggiungere 800 μl di acqua deionizzata e 200 μl di colorante Coomassie Brilliant Blue (reagente di Bradford).
- Mescolare i reagenti, lasciare a sé la reazione per 5 minuti, e osservare il cambiamento di colore.
In presenza della proteina, la soluzione diventerà blu (questo può essere rilevato con un fotometro a 595 nm). I campioni che contengono zucchero o amido non cambieranno colore.
Note di sicurezza:
La soluzione per il saggio Biorad per le proteine contiene metanolo ed acido fosforico, e quindi dovrebbe essere usata con cautela.

Immagine gentilmente concessa da Thomas Wendt
| Reazione di Fehling | Reazione di Lugol | Saggio delle proteine | Composto | |
|---|---|---|---|---|
| Soluzione A | Precipitato rosso | Marrone | Marrone | Zucchero riducente |
| Soluzione B | Soluzione blu | Blu scuro | Marrone | Amido |
| Soluzione C | Precipitato rosso | Marrone | Marrone | Zucchero riducente |
| Soluzione D | Soluzione viola | Marrone | Blu | Proteina |
| Soluzione E | Soluzione blu | Marrone | Marrone | Saccarosio |
Risultati e loro interpretazione
La soluzione B dà una reazione positiva con la soluzione di Lugol, rivelando così la presenza di amido. La soluzione D dà risposta positiva al saggio di Bradford, rivelando di essere una soluzione proteica. Le soluzioni A e C danno un precipitato rosso durante la reazione di Fehling, e possono quindi essere identificate come i campioni degli zuccheri riducenti glucosio e lattosio (sebbene non sia possibile in questa fase dire quale sia l’uno e quale l’altro). La restante soluzione, E, non dà reazioni in nessuno dei test, e di conseguenza deve trattarsi della soluzione di saccarosio.
Esperimento 2: Determinazione enzimatica dello zucchero
In questo secondo esperimento, le due soluzioni rimanenti A e C vengono nuovamente analizzate, per vedere quale di loro contenga il lattosio e quale il glucosio. Per questo esperimento utilizziamo un kit reperibile in commercio, EnzyPlus EZS 962+ lactose/D-glucose, che può essere acquistato da BioControlw2. Il procedimento è simile a quello utilizzato abitualmente dai pazienti diabetici per monitorare la loro glicemia. Il protocollo standard per il prodotto è stato modificato e ridotto di scala, in modo che si possa condurre un numero maggiore di esperimenti con i reagenti a disposizione. Un kit fornisce materiali sufficienti per 20 coppie di studenti.
Il principio del test è il seguente (vedere le figure figure sottostanti):
- Il disaccaride lattosio viene idrolizzato dall’enzima β-galattosidasi a D-galattosio e D-glucosio (Stadio 1 sottostante).
- In presenza di ATP, il D-glucosio viene specificatamente fosforilato dall’esochinasi a glucosio-6-fosfato; contemporaneamente, si forma adenosin-5’-difosfato (ADP) (Stadio 2).
- Il glucosio-6-fosfato è ossidato dalla glucosio-6-fosfato deidrogenasi a gluconato-6-fosfato.
- Durante questa reazione, NADP+ viene ridotto a NADPH. La quantità di NADPH formata in questa reazione è in rapporto stechiometrico con la quantità di lattosio, e può essere misurata fotometricamente dall’aumento di assorbanza a 340 nm.
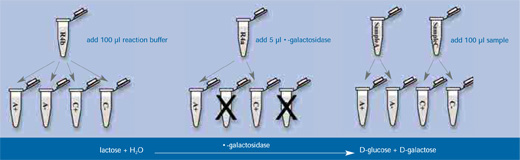
Immagine gentilmente concessa da Thomas Wendt
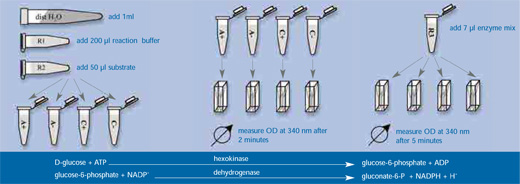
Immagine gentilmente concessa da Thomas Wendt
Per effettuare la reazione:
- Prendere quattro provette da 1,5 ml e contrassegnarle come A+, A-, C+ e C-. Mettere 100 µl di reagente tampone R4b (tampone fosfato a pH 6.6) in ciascuna provetta, e aggiungere 5 µl di soluzione di β-galattosidasi R4a nelle provette A+ e C+ (ma non nelle provette A- o C-).
- Aggiungere 100 µl di soluzione A alle provette A+ e A-, e 100 µl di soluzione C alle provette contrassegnate come C+ e C-.
Nota: nei successivi passaggi di questo esperimento, tutti e quattro i campioni vengono trattati nello stesso modo.
- Lasciare tutti i campioni per 30 minuti a 37 °C a bagnomaria mentre avviene l’idrolisi del lattosio.
- Dopo l’incubazione, aggiungere 1 ml di acqua distillata, 200 µl di tampone reattivo R1 e 50 µl di reagente R2 (contenenti rispettivamente ATP e NADP,) a tutte e quattro le provette e mescolare accuratamente.
- Trasferire 1 ml di ciascuna miscela di reazione in distinte cuvette da fotometro e misurare la densità ottica a 340 nm (OD340) dopo 2 minuti.
- A ciascuna cuvetta, aggiungere 7 µl di miscela enzimatica R3 contenente esochinasi e glucosio-6-fosfato-deidrogenasi, incubare per ulteriori 5 minuti, and misurare nuovamente l’assorbimento a 340 nm.
| Prima misura (OD340) | Seconda misura (OD340) | Risultato | |
|---|---|---|---|
| Campione A+ | 0.09 | 2.43 | Glucose |
| Campione A- | 0.09 | 2.37 | Glucose |
| Campione C+ | 0.10 | 1.43 | Lactose |
| Campione C- | 0.09 | 0.10 | Lactose |
Risultati e loro interpretazione
Tutti e quattro i campioni danno bassi valori di assorbimento alla prima misurazione, evidenziando l’assenza di NADPH. La seconda misurazione (dopo l’aggiunta degli enzimi) dovrebbe permettere la distinzione delle soluzioni A e C. Poiché la soluzione A dà risultati positivi indipendentemente dall’aggiunta o meno della β-galattosidasi, si può concludere che essa contiene glucosio. Al contrario, una variazione dell’assorbimento della soluzione C dovrebbe essere misurato solo in presenza di β-galattosidasi (C+), segno che essa contiene lattosio.
Durante la prova, i partecipanti acquisiscono informazioni di base sul diabete e sui problemi che i diabetici devono affrontare. Per tenere sotto controllo la loro glicemia, i pazienti usano un sistema di misura del glucosio costituito da apposite strisce reattive, che si comporta come una scatola nera, ma è basato sul principio usato nell’esperimento 2. Realizzare questi esperimenti potrebbe accrescere la conoscenza del diabete, o di come si possa sopravvivere alla malattia, o come prevenirla cambiando il proprio stile di vita.
Gli esperimenti qui descritti possono essere realizzati in modo sicuro in un normale laboratorio scolastico, poiché i reagenti impiegati non sono materiali pericolosi ai sensi dei Regolamenti Europei sulle Sostanze Pericolose (EC Regulation 67/548/EEC). Il livello di sodioazide, il conservante presente nei reagenti, è inferiore al più basso livello di tossicità di un preparato, in accordo con la Direttiva 1999/45/EC.
ExploHeidelberg
L’ExploHeidelbergw3 è un centro di apprendimento informale ed interattivo. È costituito da tre diverse sezioni: un’esposizione interattiva, un laboratorio multimediale ed un laboratorio didattico biotecnologico.
Nella mostra interattiva, circa 50 allestimenti sollecitano i visitatori a sperimentare fenomeni acustici, ottici e meccanici. I concetti pedagogici ed il design della mostra interattiva vengono sviluppati in stretta collaborazione con l’Università di scienze dell’educazione di Heidelbergw4. Insegnanti tirocinanti e membri dello staff del dipartimento di fisica vengono coinvolti in qualità di guide della mostra, e nell’ideazione delle esposizioni e nello sviluppo delle attività di laboratorio, nell’addestramento degli insegnanti ed in progetti di ricerca.
Il laboratorio didattico offre agli studenti delle scuole medie e superiori l’opportunità di realizzare, durante corsi pratici giornalieri, esperimenti di biotecnologia che non sono realizzabili in classe.
Un laboratorio multimediale con 12 postazioni, risorse Internet e una video postazione completano il centro studi.
La mostra interattiva ed i laboratori multimediali sono aperti al grande pubblico ogni giorno, e sono pensati per destare l’interesse dei visitatori verso le scienze della vita in generale. Il laboratorio didattico offre agli studenti di scuole e università, agli insegnanti e ai tirocinanti, corsi speciali correlati ai programmi scolastici, che permettono loro di conoscere meglio le moderne tecniche biotecnologiche. I partecipanti possono scegliere, a partire da corsi di un giorno sulla manipolazione del DNA e delle proteine, fino a corsi specialistici di una settimana riguardanti tecniche sofisticate che solitamente vengono insegnate solo a livello universitario.
References
- Dugi K (2006) Diabete mellito. Science in School 1. www.scienceinschool.org/2006/issue1/diabetes/italian
Web References
- w1 – Biorad: www.bio-rad.com
- w2 – BioControl: www.rapidmethods.com
- w3 – ExploHeidelberg: www.explo-heidelberg.de
- w4 – Università di Pedagogia Heidelberg: www.ph-heidelberg.de
Review
In questo articolo, Fred Engelbrecht e Thomas Wendt introducono l’importante tematica del diabete, e propongono due esperimenti volti ad accrescere la conoscenza dei principali componenti degli alimenti e della scienza che sta alla base delle strisce reattive al glucosio usate dai pazienti diabetici.
Lo stile di questo testo, chiaro e appropriato, è più facile nella prima parte (riguardante il diabete); gli esperimenti sono un po’ più impegnativi, e danno ai docenti l’opportunità di usare le diverse sezioni in differenti livelli di scuola secondaria.
L’articolo può essere utilizzato nei programmi di biologia, chimica ed educazione alla salute, con la possibilità di un approccio interdisciplinare alle questioni correlate al diabete, per esempio collegando biochimica, biologia ed educazione alla salute. Vista la diffusione di questa malattia, il testo è utile come punto di partenza per promuovere un senso civico attivo ed un completo inserimento sociale degli studenti diabetici.
L’articolo potrebbe essere utilizzato per introdurre le tematiche dei carboidrati e delle proteine; il metabolismo (in biochimica); l’apparato digerente (in biologia); alimenti e salute (educazione alla salute); ed esercitazioni di laboratorio (in chimica).
La prima parte può essere utilizzata per verificare le conoscenze sul diabete, la seconda per verificare la comprensione degli aspetti tecnici. Esempi di domande sono:
Quale dei seguenti aspetti non è tipico del diabete mellito?
a) Elevati livelli di glucosio nel sangue
b) Insufficiente produzione di insulina o resistenza all’effetto dell’insulina
c) Bassi livelli di glucosio nel sangue
d) Urinazione frequente e aumento della sete
I dati riportati nella Tabella 2 significano che:
a) Il glucosio necessita di β-galattosidasi per produrre NADPH
b) Il Lattosio necessita di β-galattosidasi per produrre NADPH
c) Il Lattosio non necessita di β-galattosidasi per produrre NADPH
d) Il glucosio necessita di glucosio-6-fosfato deidrogenasi per produrre NADP+.
Giulia Realdon, Italia





