Modifier le microbiote intestinal ? En selles ! Understand article
Traduit par Claire Debrat. Répugnant ? À première vue, peut-être, mais ce traitement mérite qu'on se penche dessus.

l’aimable autorisation de Big
Pants Production /
shutterstock.com / Nicola Graf
Selles, crottes ou grosse commission, peut importe votre mot préféré. L’idée d’en transférer dans votre corps est probablement répugnante. Cependant, lorsqu’on souffre d’une infection intestinale à Clostridium difficile, potentiellement mortelle, une greffe fécale peut faire la différence entre la vie et la mort. Avant de tourner la tête ailleurs, essayons donc de comprendre le raisonnement derrière ce traitement médical a priori farfelu : c’est simple, les selles contiennent un ingrédient clé, des bactéries qui nous veulent du bien. Dans plus de 90 % des cas, la greffe fécale est efficace contre les infestions à C. difficile. Mieux encore, des chercheur du Laboratoire européen de biologie moléculairew1 (EMBL) pensent à présent qu’il serait possible de trouver des donneurs compatibles avec les patients pour redoubler d’efficacité et étendre les greffes fécales à d’autres applications.
Les bactéries et le microbiote intestinal
Si un médecin nous prescrit des antibiotiques, nous espérons que le médicament soignera l’infection. On ne s’attend pas à ce qu’il provoque une autre maladie. Cependant, les antibiotiques tuent certes les bactéries ciblées, mais aussi des bactéries bénéfiques. Cela est particulièrement vrai pour les antibiotiques à large spectre et déséquilibre la communauté complexe des micro-organismes de l’intestin, ou microbiote intestinal.
La bactérie C. difficile est présente dans la terre, dans l’eau et dans l’air. Elle fait aussi partie du paysage intestinal d’environ un adulte sain sur trente, sans causer de problèmes. En revanche, lorsque l’équilibre entre les microbes de l’intestin est rompu et qu’il y a moins de bactéries bénéfiques pour garder la main, C. difficile se multiplie rapidement dans l’intestin.
Plus elle se multiplie et se répand dans l’intestin, plus C. difficile produit de toxines. Ces toxines provoquent des diarrhées et, lorsque les bactéries sortent de notre corps, elles peuvent facilement contaminer d’autres personnes. Cette bactérie est donc un véritable casse-tête pour les hôpitaux et l’infection à C. difficile est une maladie nosocomiale (qu’on attrape dans les centres de santé) très problématique. Parmi les symptômes de cette infection, on trouve aussi les maux de ventre, la fièvre voire, dans les cas graves, la déshydratation, l’inflammation de l’intestin et même la perforation du gros intestin.
Chez la plupart des patients, l’infection est combattue à l’aide d’antibiotiques spécifiques contre C. difficile. Dans 20 % des cas, cependant, les symptômes réapparaissent et il faut reprendre le traitement. Ces traitements répétés deviennent de plus en plus compliqués, car de nouvelles souches de la bactérie apparaissent et elles sont résistantes. L’une des dernières manières de débarrasser les patients de cette « super-bactérie » est la greffe fécale, ou « fécalothérapie ».
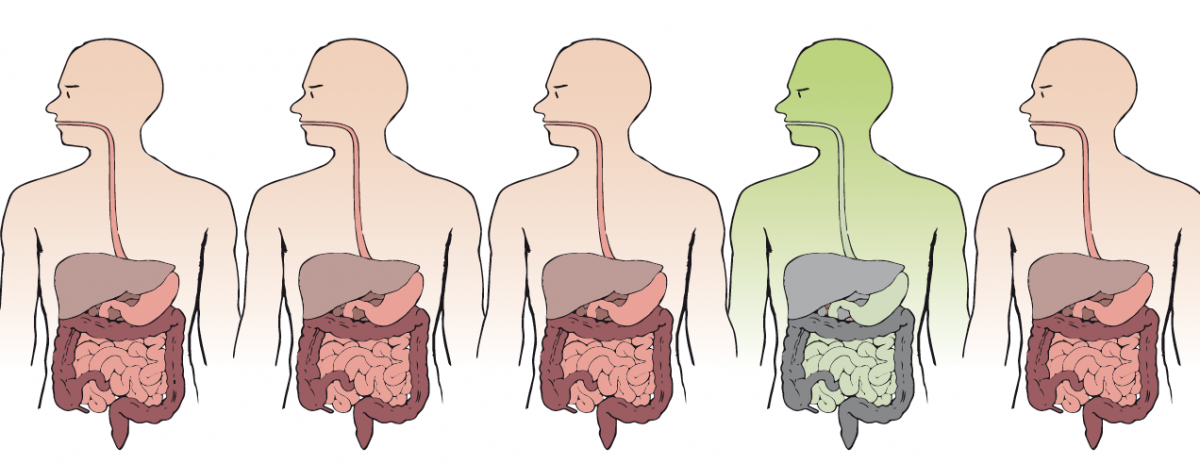
Image reproduite avec l’aimable autorisation de Nicola Graf
Soigner avec des selles
Les tests effectués sur les échantillons fécaux potentiels sont très rigoureux : seuls 3 % des dons bénévoles d’échantillons sont acceptés par la banque fécale OpenBiomew2. par exemple. Lors d’une greffe fécale, il existe un risque de transmettre une maladie infectieuse. De plus, nous avons de plus en plus de preuves d’un lien entre le microbiote et l’obésité, le diabète et les allergies : lors de la transplantation, peut-être que ces maladies pourraient aussi être transmises au patient. Par exemple, un cas a été signalé où une femme guérie d’une infection à C. difficile a observé un effet secondaire inattendu : le donneur de matière fécale était obèse et la patiente a rapidement grossi à son tour (Alang & Kelly, 2015). La greffe n’est peut-être pas la seule cause de cette prise de poids, cependant le cas pose des questions sur le rôle que les bactéries intestinales jouent dans notre métabolisme et notre bonne santé.
Si un échantillon fécal est considéré comme utilisable, il est liquéfié et administré lors d’une coloscopie. La communauté de microbes du donneur sain, qui vient avec leurs gènes sains et leur bon fonctionnement métabolique, peut alors restaurer l’équilibre du microbiote du patient infecté.
Malgré son efficacité contre les infections à C. difficile (plus de 90 % de réussite), la greffe fécale reste peu pratiquée, probablement car elle est surprenante et elle nous dégoûte. Nos selles, comme le sang ou le vomis, peuvent contenir des organismes qui causent des maladies. Il est donc normal que les humains les évitent, et bien sûr qu’ils ne les absorbent pas. La définition de règles strictes pour encadrer ces greffes en limite aussi la généralisation, tout comme le caractère plus invasif de ce traitement comparé à la prise d’antibiotiques.
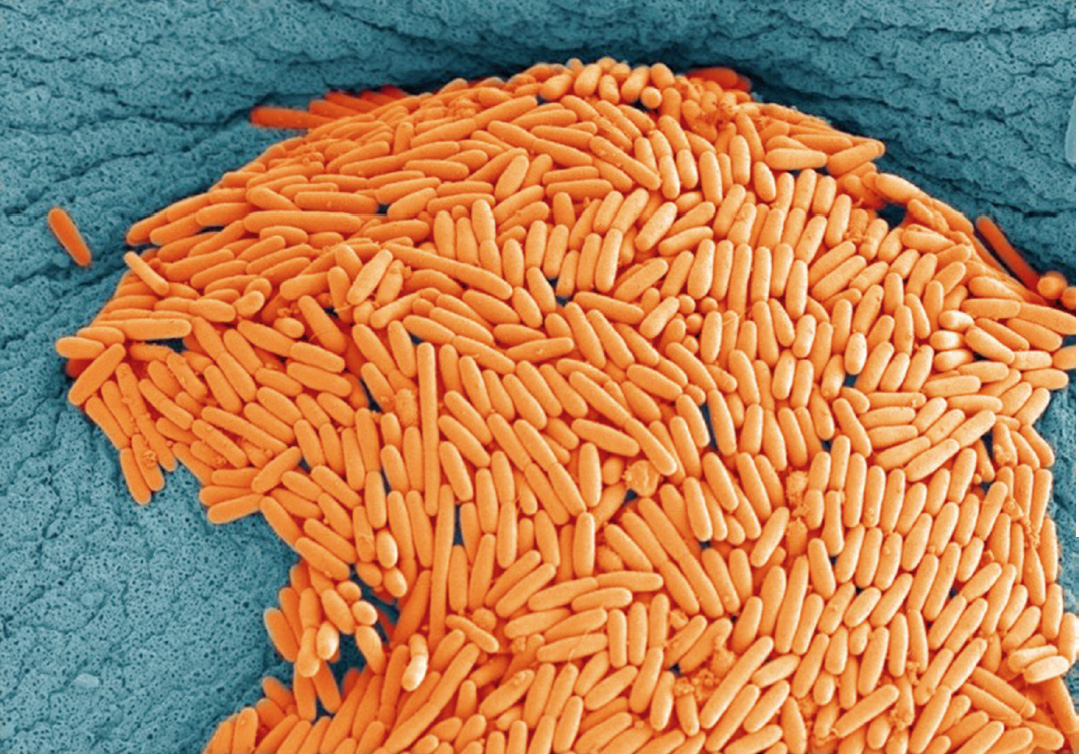
Image reproduite avec l’aimable autorisation de Wellcome Images (CC BY-NC 4.0)
Des comprimés sur-mesure
Pour être moins repoussantes, les greffes fécales changent de méthode d’administration. Au lieu des méthodes invasives, les patients peuvent avaler un comprimé, une sorte de « crotte-en-bouche ». C’est plus esthétique et plus facile. Dans une étude récente portée par des chercheurs de l’EMBL, avec la collaboration de l’université de Wageningen, du Centre médical académique (tous deux aux Pays-Bas) et de l’université de Helsinki (Finlande), les auteurs soulignaient la nécessité d’une approche sur-mesure (Li et al., 2016).
La clé du succès n’est pas d’étudier les espèces de bactéries dans l’intestin d’un patient, mais d’aller encore plus loin et de savoir quelles souches de chaque espèce sont présentes. L’étude a montré que les souches venues du donneur avaient plus de chances de coloniser l’intestin du patient si ce patient avait déjà hébergé les mêmes. Simone Li, qui a mené l’étude à l’EMBL, explique que l’objectif est de pouvoir prescrire « un cocktail bactérien personnel, pas un breuvage standard ». Vérifier rigoureusement la compatibilité entre patient et donneur pourrait améliorer l’efficacité des greffes fécales.
Et l’histoire ne s’arrête pas là. Les chercheurs se demandent si ces greffes pourraient soigner d’autres maladies dues à un déséquilibre du microbiote, par exemple les allergies, l’obésité et le diabète de type 2 (Bull & Plummer, 2014). Qui sait même si, à l’avenir, nous n’aurons pas tous une réserve de selles saines quelques part, au cas où ? Peut-être avalerons-nous des comprimés de matière fécale congelée venant de notre réserve personnelle ?
References
-
Alang N, Kelly CR (2015) Weight gain after fecal microbiota transplantation. Open Forum Infectious Diseases 2(1): ofv004. doi: 10.1093/ofid/ofv004
-
Bull MJ, Plummer NT (2014) Part 1: The human gut microbiome in health and disease. Integrated Medicine 13(6): 17–22
-
Li S et al. (2016) Durable coexistence of donor and recipient strains after fecal microbiota transplantation.. Science 352(6285): 586–589. doi: 10.1126/science.aad8852
Web References
-
w1 – L’EMBLest le laboratoire européen à la pointe de la recherche fondamentale en biologie moléculaire. Son siège se situe à Heidelberg, en Allemagne.
-
w2 – OpenBiome est une organisation à but non lucratif dont l’objectif est de faciliter l’accès à des greffes fécales sûres.
Resources
-
Pour en savoir plus sur l’étude récente sur l’amélioration des greffes fécales par l’approche sur-mesure, consulter les pages d’info de l’EMBL.
-
Pour en savoir plus sur les greffes fécales, consulter le site internet de Johns Hopkins Medicine website.
-
Pour en savoir plus sur les greffes fécales, lire l’article ‘Medicine’s dirty secret’ paru dans le magazine Mosaic.
-
La scientifique allemande et auteure à succès Giulia Enders nous dit tout sur la science du tube digestif, y compris sur les bactéries intestinales. Voir son livre Le charme discret de l’intestin :
-
Enders G (2015) Le charme discret de l’intestin : cet organe mal aimé. Arles, France: Actes Sud Editions. ISBN: 978-2330048815
-
Pour comprendre pourquoi l’être humain déteste autant les crottes, lire l’article suivant (en anglais) sur BBC Future Why do humans hate poo so much? .
Review
Les selles constituent un sujet amusant de discussion entre étudiants et amis. Le sujet « cra-cra » des greffes fécales peut aiguiser leur intérêt pour la physiologie, les inciter à en apprendre davantage sur le métabolisme et les processus physiologiques. Cet article est pertinent pour les sciences médicales mais peut aussi permettre de faire le lien avec la microbiologie et l’écologie.
Bartolome Piza, CC. Pedro Poveda, îles Baléares, Espagne





