Une introduction artistique aux encres à base d’anthocyanes Teach article
Traduit par Maurice Cosandey. La fabrication d’encres sensibles au pH à partir de fruits et légumes est une variation inédite de la célèbre expérience du chou rouge.
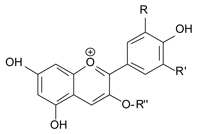
des anthocyanes, où R et R’
sont H, OH ou OCH3, et R’’ et
un sucre
Image de Gustavo Giraldi
Shimamoto et Adriana Vitorino
Rossi
Longtemps avant l’invention des colorants artificiels, on fabriquait des encres simples mais efficaces à partir de produits naturels (voir l’article de Farusi, 2012) comme on en voit encore aujourd’hui sur les peintures préhistoriques. Ces colorants naturels étaient d’origine minérale ou végétale. L’article de ce jour se concentre sur l’emploi des plantes produisant des anthocyanes (ACY, figure 1).
Natural colours are often less stable than many synthetic dyes, changing colour or disintegrating with temperature, light, pH variation and oxidising agents. This can lead to interesting lessons, and in our work with primary school students we have used anthocyanins as colourants for pH-reactive ink production.
L’origine de la couleur
Les anthocyanes sont des composés organiques dont la couleur peut passer de l’orange au rouge, au violet et au bleu. On les trouve dans certaines fleurs, fruits et racines. Les molécules d’anthocyane contiennent des cycles carbonés qui absorbent la lumière, et qui fonctionnent donc en écran qui protège les cellules de la plante. Les longueurs d’onde de lumière qui ne sont pas absorbées sont réfléchies, et donnent au fruit sa couleur visible. Ces couleurs attirent aussi les pollinisateurs et les disperseurs de graines, ce qui favorise la reproduction de la plante.
Les solutions d’anthocyanes changent de couleur avec le pH, et forment donc un indicateur naturel (figure 2). En général, les anthocyanes sont rouges en milieu acide et bleus en milieu alcalin. Mais souvent la couleur dépend de la nature et de l’origine de l’anthocyane. Ce changement de couleur est dû au fait que l’addition d’un ion H+ sur la structure moléculaire du pigment modifie ses propriétés électroniques, donc la valeur de la longueur d’onde qui sera absorbée. C’est pour cela que les extraits de plantes sont utilisés pour déterminer le pH des eaux claires, ou le point d’équivalence des titrages acide-base. Voir l’expérience du chou rouge (Terci & Rossi, 2002; Rossi & Shimamoto, 2010). Les anthocyanes peuvent aussi servir à former des encres pour la peinture à l’eau.

Image de Gustavo Giraldi Shimamoto and Adriana Vitorino Rossi
Qu’est-ce que c’est, une encre ?
Une encre est un mélange de colorants ou de pigments et d’un agent de liaison qui aide l’encre à adhérer sur la surface à peindre. Cette formulation a été utilisée pendant des milliers d’années. Mais aujourd’hui, les encres sont devenues plus sophistiquées, et peuvent par exemple réagir chimiquement avec le support sur lequel on les depose.
Le principal constituant d’une encre est le pigment ou le colorant qui lui donne sa couleur. Un pigment est un solide pulvérisé qui est insoluble dans l’eau ou dans le liquide formant l’encre. Un colorant par contre est un substance soluble dans l’eau ou le liquide de l’encre. Les anthocyanes sont des pigments. Les pigments confèrent opacité et solidité au dépôt.
Encre d’anthocyane pour la peinture au pinceau ou au rouleau, ou pour tampon
Matériel

produit par le vinaigre
Image de Gustavo Giraldi
Shimamoto and Adriana
Vitorino Rossi
- Des fruits ou des légumes riches en anthocyane, comme les mytilles, les fraises, les mûres, les framboises ou les choux rouges
- De l’éthanol à 94% en volume
- Du papier filter (un filtre à café peut faire l’affaire)
- Des boîtes de Pétri
- De l’eau
- Du papier de luxe, ayant une densité supérieure à 50 g/m2
- Des tampons, des pinceaux, des rouleaux
- Du vinaigre
- Un produit détergent multi-usage ayant des propriétés alcalines
Mode opératoire
- Ecraser le fruit ou le légume, et le mélanger pendant 30 minutes avec un volume d’éthanol égal à 3 fois le poids du légume.
- Filtrer sur papier et distribuer le filtrat dans plusieurs boîtes de Petri.
- Laisser les extraits de ces boîtes de Petri à l’air pendant 2 jours à l’abri du soleil, jusqu’à evaporation complete du solvant. On peut accélérer cette évaporation en travaillant sous une hotte ventilée.
- Quand l’extrait d’anthocyane est sec, il a un aspect pâteux, Ajouter à peu près 10 fois son poids d’eau, et homogénéiser.
L’encre ainsi obtenue peut être utilisée avec un pinceau, un tampon ou un rouleau encreur. Comme l’anthocyane est un indicateur, la couleur de l’encre se modifie au contact d’un acide ou d’une base. On peut utiliser une brosse pour appliquer une solution acide (vinaigre) ou basique (détergent ménage) sur du papier coloré avec cette encre. On peut aussi asperger une solution acide ou basique sur du papier teint au préalable. On peut aussi écrire un message illisible, donc secret, avec un pinceau imbibé d’acide ou de base. On laisse sécher. Puis on pulvérise la solution d’anthocyane avec un spray directement sur le papier afin de révéler le message.
Note sur la sécurité
Renseignez-vous sur la législation locale. Le port de lunettes de protection peut être obligatoire.
Ce qui s’est produit

different pH. (a) Aspect initial
(b) Aspect après traitement
acide (c) après traitement
basique
Image de Gustavo Giraldi
Shimamoto and Adriana
Vitorino Rossi
Les extraits d’anthocyane sont des indicateurs de pH aussi bien en solution que déposés sur papier. Le changement de couleur est dû à l’interaction entre les molécules d’anthocyane déposées sur le papier et l’acide acétique du vinaigre ou la base du detergent.
Le changement de couleur est lié à l’équilibre chimique décrit sous forme simplifiée en figure 2. Les anthocyanes sont des composés organiques qui ont plusieurs substituants sur lesquels les ions H+ peuvent se fixer ou s’éliminer, ce qui change leur couleur. La figure 2 montre les couleurs que les peintures à l’anthocyane prennent dans trois milieux différents : acide, neutre et basique. On peut aussi comparer les différentes anthocyanes en les trempant dans ces trois milieux.
L’encre à l’anthocyane peut être utilisée par des enfants de moins de 11 ans pour faire de la peinture. L’emploi de vinaigre ou de détergent devrait être réservé aux élèves plus âgés, qui sont plus aptes à établir des comparaisons entre eux. Il est bien sûr possible de modifier le mode opératoire, et la technique d’application de cette encre, car elle n’est pas toxique, et ses déchets et résidus peuvent être sans autre jetés à l’évier.
Le but principal de cette activité récréative est d’éveiller la curiosité des élèves. Mais on peut en élargir l’impact en envisageant une approche interdisciplinaire, qui incorpore une éducation à l’environnement et aux valeurs locales. Pendant la fabrication de l’encre, le maître peut également amener les élèves à réfléchir sur la nature, la biodiversité, et leur exploitation rationnelle, en vue d’obtenir des produits utiles.
Remerciements
Les auteurs remercient le Fondation de recherche de Sao Paulo (FAPESP) pour son support financier.
References
- Farusi G (2012) Indigo: Comment recréer le colorant des pharaons. Science in School 24: 40–46.
- Rossi AV, Shimamoto GG (2010) Antocianinas e gelo seco para visualizar equilíbrios ácido/base numa abordagem contextualizada. Educació Química EduQ 7: 31–36 [in Portuguese].
- Terci DBL, Rossi AV (2002) Indicadores naturais de pH: usar papel ou solução? Química Nova 25: 684–688 [in Portuguese].
Web References
- w1 – On trouvera plus d’information sur le Groupe de recherche de chimie analytique et d’éducation à l’Université de Campinas (UNICAMP) de São Paolo, Brésil.
Resources
- Beautiful Chemistry est un site basé en Chine, qui présente des vidéos et des images d’indicateurs de pH tirés des plantes.
- Les anthocyanes peuvent servir à fabriquer des cellules solaires à colorants, comme par exemple dans l’activité suivante :
- Shallcross D, Harrison T, Henshaw S, Sellou L (2009) Regarder vers le ciel: expériences sur le changement climatique. Science in School 12: 34–39.
- Si vous avez aimé cet article, vous lirez peut-être avec intérêt la référence suivante :
- Salamão AA, et al (2010) Jogo pedagógico que explora a propriedade indicadora de pH de extratos de antocianinas de espécies brasileiras. In de Rezende CM, Braibante HTS (eds) A Química Perto de Você – Experimentos de baixo custo para a sala de aula do Ensino Fundamental e Médio pp35–43. Cidade Universitária, São Paulo, Brazil: Sociedade Brasileira de Química. ISBN: 9788564099005 [in Portuguese]. Cet ouvrage peut être déchargé gratuitement.
Review
Ceci constitue une nouvelle façon d’enseigner un sujet ancien, en classe ou dans un club de sciences
L’introduction de cet article pourrait servir à un exercice de compréhension. L’article pourrait servir à engager une large discussion sur les acides, les bases et les indicateurs, les extractions chimiques, ou la science et l’art.
Tim Harrison, Bristol ChemLabS, University of Bristol, Royaume-Uni





