Regardez-le grandir: développement d un embryon digital Understand article
Traduit par Camille Ducoin. Et si vous pouviez assister au développement d'une nouvelle vie, en prenant votre temps pour étudier chaque détail, chaque cellule, sous tous les angles, instant par instant? Sonia Furtado a rencontré les chercheurs qui ont rendu cela possible en créant un…

Jochen Wittbrodt and Annette Schmidt
Image courtesy of EMBL Photolab
Imagine Google Earth™ prenant de nouvelles photos satellites à intervalles de temps réguliers: vous pourriez non seulement voir l’ensemble de la planète et zoomer sur des pays ou des villes, mais aussi repasser la séquence de photos et voir ce qui a changé en 10 ou 20 ans. Remplacez la Terre par un embryon de poisson-zèbre, et rassemblez quelques centaines de milliers de photos prises durant 24 heures: voici ce que les scientifiques du Laboratoire Européen de Biologie Moléculaire (EMBL)w1 ont appelé “embryon digital”.
Le biophysicien Philipp Keller, les biologistes Annette Schmidt et Jochen Wittbrodt, et le physicien Ernst Stelzer ont fait équipe pour obtenir une représentation en 3D des premières 24 heures d’un embryon de poisson-zèbre (Keller et al., 2008). Tout a commencé en 2006, quand un post-doctorant a suggéré à Philipp de simplement mettre un embryon dans le microscope pour suivre l’évolution de toutes les cellules. Stimulé par cette conversation, Philipp s’est intéressé de plus près à une tehnique d’imagerie en 3D développée par le groupe d’Ernst: la microscopie à feuille de lumière (SPIM: single-plane illumination microscopy. Voir glossary pour les termes en italique). Il a repris les principes de base de la SPIM pour l’adapter au suivi du développement embryonnaire. Cela a donné la microscopie digitale à fluorescence par balayage laser (DSLM, pour digital scanned laser light sheet fluorescent microscopy).
Les cellules d’un embryon en développement se multiplient et se déplacent sans cesse; il faut donc prendre des clichés séparés par des temps très courts pour suivre ces changements. Ceci requiert une imagerie à la fois rapide et de bonne qualité, afin de distinguer des cellules très proches les unes des autres. Pour suivre le développement de l’embryon, il faut bien sûr maintenir les cellules en vie et en évolution normale pendant au moins un jour ou deux. Enfin, le microscope ne doit pas endommager la substance fluorescente utilisée pour marquer les cellules.
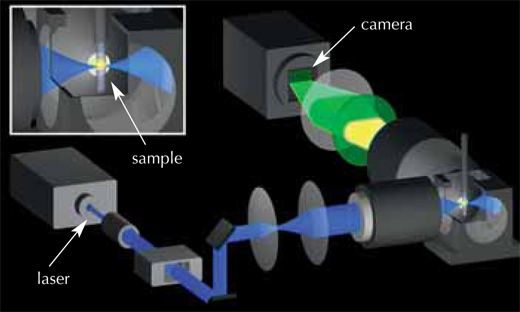
Image reproduite avec l’aimable autorisation de Petra Riedinger
La solution a été d’utiliser un faisceau laser très fin, minimisant l’impact sur le marqueur et sur l’embryon. Ce faisceau traverse l’embryon, excitant le marqueur fluorescent présent dans les cellules, qui émet alors de la lumière. Le faisceau se déplace verticalement, et la fluoresence émise par l’échantillon est détectée à un angle de 90° par un appareil photographique; ceci produit l’image d’une tranche de quelques millièmes de millimètres (voir film 1w2). L’embryon est ensuite déplacé horizontalement d’un très petit pas, et l’image suivante est scannée. Une fois que l’ensemble de l’embryon a été scanné sous un angle donné, il est tourné de 180° et scanné une nouvelle fois, afin de composer une image 3D. L’embryon vit et continue de se développer, ainsi le balayage peut être répété périodiquement sur le même embryon, faisant apparaître son évolution. Les chercheurs du EMBL ont scanné leurs embryons de poissons-zèbres toutes les 60 ou 90 secondes pendant 24 heures, obtenant autour de 400 000 images par embryon.
Le défi suivant était d’établir comment analyser les trois terabytes de données enregistrées pour chaque embryon. Les chercheurs ont choisi une approche automatisée: ils ont utilisé des groupes d’ordinateurs fonctionnant en parallèle, au EMBL à Heidelberd ainsi qu’à l’Institut de Technologie de Karlsruhe (Allemagne)w3. “Chaque ordinateur reçoit un cliché de l’embryon, et doit localiser les noyaux des cellules sur cette image”, explique Philipp. Chaque noyau représente une cellule. En combinant les informations de toutes les tranches, les chercheurs peuvent générer leur embryon digital: une représentation de toutes les cellules de l’embryon, où elles se trouvent à un moment donné, où elles se déplacent ensuite, quand et où elles se divisent. On obtient ainsi une vidéo en 3D du développement de l’embryon.
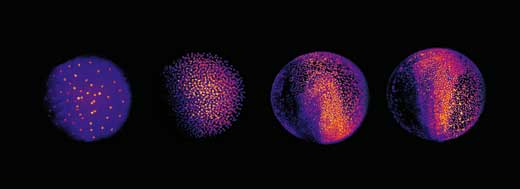
Image reproduite avec l’aimable autorisation de EMBL Photolab
Ceci a permis à Philipp, Annette et Jochen d’apporter des éclaircissements sur plusieurs étapes du développement embryonnaire des poissons-zèbres. À un stade très précoce, l’embryon se résume à un groupe de cellules installées sur la vésicule vitelline (source nutritive de l’embryon). Au début, les cellules se divisent suivant une onde qui part du centre dans toutes les directions, comme un cercle sur l’eau. La reconstruction a montré que, après les neuf premiers cycles de divisions, le schéma change: l’onde se propage du centre vers une direction donnée, puis se sépare en deux et continue vers la périphérie suivant deux demi-cercles (voir image ci-dessous et film 10w2). La ligne entre ces deux demi-cercles deviendra l’axe du corps, définissant la symétrie de l’animal. Ainsi, les chercheurs ont découvert que l’axe du corps des poissons-zèbres est défini à un stade de développement beaucoup plus précoce qu’on ne le pensait, à un moment où les gènes maternels (sous forme de ARNm déposé dans l’oeuf) sont encore le seul patron utilisé pour la production de protéines.
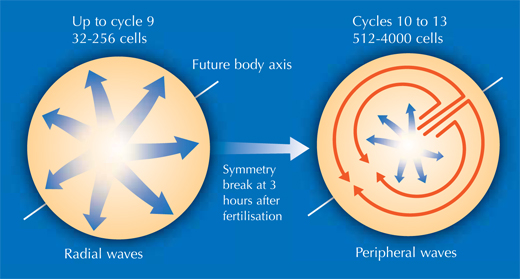
Image reproduite avec l’aimable autorisation de Nicola Graf
Les chercheurs ont aussi étudié la gastrulation, processus par lequel des cellules initialement situées sur la couche externe de l’embryon migrent vers l’intérieur pour former deux autres couches de cellules, chaque couche devenant un type de tissus différent. “Il faut deux ou trois pages de manuel pour décrire ce processus, mais en voyant les films de l’embryon digital, cela devient tout de suite plus facile à comprendre”, dit Annette. Et surtout, elle a découvert avec ses collègues que les manuels se trompent.
Depuis les années 1980, expliquer comment les cellules migrent pour former ces couches faisait l’objet d’un débat constant, et parfois fervent. Le point de vue dominant était que les cellules involuent; c’est à dire qu’elles migrent vers une ouverture dans l’embryon et roulent par-dessus bord pour former une couche en dessous, à l’intérieur. Cependant, certains chercheurs pensaient que des cellules individuelles de la couchent externe plongent directement de là où elles sont, ou ingressent,, pour former la couche interne.
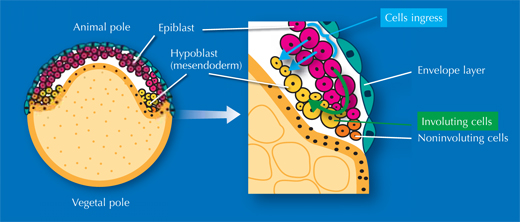
Image reproduite avec l’aimable autorisation de Nicola Graf
“Nous avons joliment résolu le problème”, dit Jochen. “Il apparaît que tout le monde avait raison!” Tout dépend où l’on regarde. D’un côté de l’embryon les cellules involuent, de l’autre elles ingressent (voir film 16w2). La controverse s’est déclenchée parce-que différents chercheurs observaient différentes régions de l’embryon. Ils ne pouvaient cependant pas déterminer exactement de quelle région il s’agissait, ne pouvant pas voir l’ensemble du processus. En surmontant ces restrictions, les chercheurs du EMBL ont pu découvrir ce qu’il en est.
Les chercheurs ont aussi utilisé l’embryon digital comme modèle de développement, pour découvrir l’origine des cellules contribuant à former un organe ou un tissus spécifique. Ils ont pris l’oeil comme premier exemple. Dans la représentation digitale, ils ont marqué les cellules dont ils savaient qu’elles seraient impliquées dans la formation de l’un des yeux du poisson-zèbre, repérables à un stade de développement avancé (tard dans la vidéo de 24h). Ils ont ensuite remonté le temps en suivant la trace de ces cellules pour découvrir d’où elles viennent (voir film 11w2).
L’équipe a rendu ses embryons digitaux disponibles sur Internetw2, ainsi que les outils permettant à d’autres chercheurs d’analyser leurs propres données microscopiques. Et après? Avec Google Earth, non seulement on peut voir l’ensemble de la planète et zoomer sur différentes régions, mais les utilisateurs peuvent aussi ajouter leurs propres notes et voir celles qui ont été ajoutées par d’autres. De même, Philipp, Annette, Jochen et Ernst voudraient voir leurs embryons digitaux devenir des “embryons virtuels”: des ressources permettant à d’autres chercheurs de visualiser des processus de développement, zoomer pour plus d’informations, ajouter leurs notes et résultats. À long terme, ils aimeraient appliquer l’idée de l’embryon digital à d’autres espèces: ceci permettraient aux scientifiques de comparer quantitativement le développement de différents embryons, ce qui apporterait de précieux éclaircissements sur l’évolution. L’embryon digital peut encore bien grandir, et avec un nombre croissant de personnes pour l’aider à se développer, il semble promis à un bel avenir.
Glossaire
Microscopie digitale à fluorescence par balayage laser (DSLM): version améliorée de la SPIM, qui utilise un faisceau laser fin plutôt qu’un feuillet de lumière entier; ceci réduit les dommages causés à l’embryon et au marqueur fluorescent.
Gastrulation: phase précoce de développement embryonnaire, durant laquelle se forment trois couches de cellules: ectoderme, mesoderme et endoderme. La durée et les mécanismes moléculaires de la gastrulation diffèrent d’un organisme à l’autre.
Lignée génétique: groupe d’animaux génétiquement uniformes, utilisé pour des expériences de laboratoire. Une lignée génétique peut être développée par croisement consanguin, mutation ou ingénierie génétique.
Microscopie à feuille de lumière (SPIM): cette méthode permet d’observer en trois dimensions les processus dans les organismes vivants, y compris dans les couches profondes des tissus. La fluorescence est détectée à un angle de 90° par rapport à l’axe du faisceau laser, ce qui permet une coupure optique. Le spécimen n’est pas placé sur une plaque de microscope, mais dans une chambre remplie de liquide que l’on fait tourner au cours de l’observation.
Le poisson-zèbre comme modèle d’organisme
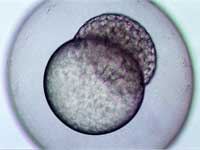
au stade de blastula, deux
heures et quarante-cinq
minutes après fertilisation
Image reproduite avec l’aimable
autorisation de Angharad Jones,
Wellcome Images
Pour des raisons éthiques, il est difficile d’étudier le développement embryonnaire humain. Cependant, le processus est similaire chez tous les vertébrés; nous pouvons donc utiliser d’autres animaux comme modèles pour comprendre notre propre développement. Mais pourquoi le poisson-zèbre? Nous le devons à George Streisinger, un biologiste hongrois de l’Université d’Oregon, aux États-Unis. Au début des années 1980, il rêvait d’appliquer les techniques moléculaires, avec lesquelles il avait étudié les virus, à des recherches sur la génétique et le développement d’un vertébré. En tant qu’aquariophile, il a choisi le poisson-zèbre, car il savait qu’il était facile à élever. Plusieurs raisons pratiques font de ces poissons un modèle attractif: d’abord, il sont assez petits pour être élevés en grand nombre, comme l’exigent les études de génétique, mais assez gros pour permettre des manipulations embryologiques classiques comme les transplantations.
Ils ont un temps de génération assez court (3 à 4 mois), produisent un grand nombre d’embryons (100 à 200 par accouplement) et l’on accède aisément à tous les stades du développement, du fait de la fertilisation externe. Comme les embryons sont transparents et se développent rapidement (toutes les structures importantes du poisson adulte étant en place au bout de trois jours), il est facile d’étudier leur évolution, que ce soit avec un simple microscope ou une technologie plus complexe comme il est décrit dans cet article. De plus, le génome du poisson-zèbre a été séquencé et des lignées génétiques définies sont disponibles, offrant la possibilité d’étudier non seulement l’embryologie, mais aussi les maladies héréditaires et la génétique qui se situe à la base de la biolobie du développement: le rêve de Streisinger est devenu réalité.
References
- Keller PJ, Schmidt AD, Wittbrodt J, Stelzer EH (2008) Reconstruction of zebrafish early embryonic development by scanned light sheet microscopy. Science 322: 1065-9. doi: 10.1126/science.1162493
Web References
- w1 – Pour en savoir plus sur le Laboratoire Européen de Biologie Moléculaire (EMBL), voir: www.embl.org
- w2 – Le site Internet de l’Embryon Digital comporte des vidéos montrant le développement de l’embryon de poisson-zèbre, ainsi que des données à télécharger: www.digital-embryo.org
-
Le film 1 donne une représentation schématique du principe de la DSLM.
-
Les films 2 et 3 montrent le développement d’un embryon de poisson-zèbre durant les premières 24 heures.
-
Le film 10 illustre la brisure de symétrie dans la division des cellules après les neuf premiers cycles, et la détermination précoce de l’axe du corps de l’embryon.
-
Le film 11 montre les parcours migratoires des cellules formant l’oeil du poisson-zèbre.
-
Le film 16 montre comment l’involution et l’ingression jouent toutes deux un rôle dans la gastrulation du poisson-zèbre.
-
- w3 – Pour plus d’informations sur l’Institut de Technologie de Karlsruhe, en Allemagne, voir: www.kit.edu
Resources
- Patterson L (2010) Getting ahead in evolution. Science in School 14: 16-20.
- Hodge R (2006) A search for the origins of the brain. Science in School 2: 68-71.
- Un ensemble de ressources pour l’apprentissage et la recherche sur le développement embryonnaire se trouve sur: http://people.ucalgary.ca/~browder/virtualembryo
Institutions
Review
Cet article décrit des avancées de pointe en biologie du développement. Le résultat potentiel – un embryon virtuel qui pourrait être partagé et annoté par d’autres chercheurs, tout comme des photos et commentaires sont ajoutés sur Google Earth – est un exemple stimulant, montrant comment les résutats scientifiques peuvent être transmis, commentés, et peut-être étendus. Ceci renvoit aux notions de science intégrée et de communication qui apparaissent dans certains programmes.
Beaucoup de choses dans cet article peuvent enthousiasmer les élèves amateurs de biologie. L’emploi de microscopie sophistiquée pour repousser les frontières de la science pourrait susciter des discussions sur la limitation des découvertes par la technologie disponible, et combien cela rend les connaissances actuelles éphémères et incertaines.
L’utilisation d’embryons de poissons-zèbres peut aussi donner lieu à un débat éthique. Est-il acceptable de faire des expériences sur des embryons de poissons? Et sur des embryons humains? Ceci peut amener à discuter certains aspects de la législation sur ce type de recherches.
Cet article peut être utile à des enseignants de biologie pour mettre à jour leurs propres connaissances. Il peut aussi être utisé comme lecture de culture générale, peut-être pour des élèves participant aux olympiades de biologie ou devant passer un entretien d’entrée dans un établissement d’enseignement supérieur. De plus, le support vidéo est utile pour illustrer un cours abordant le développement embryonnaire.
Quelques questions pertinentes:
- Décrivez et discutez les questions éthiques concernant le travail des chercheurs.
- Imaginez comment le travail sur les embryons de poissons pourrait aider à l’avenir à traiter des maladies humaines.
Sue Howarth, Royaume Uni





