Obserwując jak rosną: rozwój cyfrowych zarodków Understand article
Tłumaczenie Karolina Ciosek. Chciałbyś być świadkiem powstawania nowego życia? Śledzić każdy szczegół, każdą pojedynczą komórkę, chwila po chwili? Sonia Furtado rozmawia z naukowcami, dzięki którym jest to możliwe, którzy stworzyli cyfrowe zarodki rybki danio pręgowanej.

Jochen Wittbrodt i Annette
Schmidt
Zdjęcie dzięki uprzejmości
EMBL Photolab
Wyobraź sobie, że program Google Earth™ robi nowe zdjęcia satelitarne Ziemi w regularnych odstępach czasu, tak że sekwencje zdjęć, zarówno widoku całej planety, jak i zbliżenia na poszczególne kraje i miasta, możesz odtworzyć i obserwować zmiany, które zaszły w ciągu 10 czy 20 lat. Teraz wyobraź sobie, że zastępujesz Ziemię rozwijającym się zarodkiem rybki danio pręgowanym i przez 24 h na dobę powstaje jego kilkaset tysięcy zdjęć – to właśnie „cyfrowy zarodek”. Nazwali go tak jego twórcy z Europejskiego Laboratorium Biologii Molekularnej (EMBL)w1 have dubbed ‘the digital embryo’.
Biofizyk Philipp Keller, biolodzy Annette Schmidt i Jochen Wittbrodt oraz fizyk Ernst Stelzer połączyli siły, aby wspólnie opracować technikę pozwalającą na uzyskanie obrazu 3D z pierwszych 24 godzin rozwoju zarodka rybki danio (Keller et al., 2008). Wszystko zaczęło się na początku 2006 roku, kiedy znajomy naukowiec zasugerował Phillipp’owi, aby ten włożył zarodek pod mikroskop i obserwował wszystkie komórki. Zainspirowany tą rozmową, Philips na nowo spojrzał na single-plane illumination microscopy (jednopłaszczyznową mikroskopię świetlną, SPIM) (patrz słowniczek wszystkich pojęć pisanych kursywą), technikę obrazowania 3D opracowaną wcześniej przez zespół Ernst’a. Udoskonalił podstawowe zasady działania SPIM, aby mikroskop rejestrował rozwój embrionalny: w rezultacie powstała digital scanned laser light sheet fluorescent microscopy (cyfrowa mikroskopia fluorescencyjna z laserowym skanowaniem powierzchni, DSLM).
Ponieważ komórki w rozwijającym się zarodku cały czas dzielą się i poruszają, zdjęcia muszą być robione w bardzo krótkich ostępach czasu, aby zarejestrować zmiany. To wymaga mikroskopu, który łączy w sobie wysoką prędkość przetwarzania obrazu i wysoką jakość obrazu, aby rozróżnić komórki, które znajdują się bardzo blisko siebie. Oczywiście, aby móc obserwować postępy w rozwoju embrionu, komórki muszą cały czas pozostawać przy życiu oraz zachowywać się naturalnie przez jeden do dwóch dni. Poza tym mikroskop nie może uszkadzać fluorescencyjnych barwników, które są używane do oznaczania komórek.
Zdjęcie dzięki uprzejmości Petra Riedinger
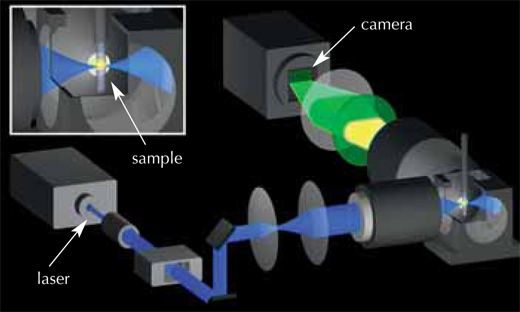
Rozwiązaniem było użycie bardzo cienkiej wiązki lasera, co minimalizuje uszkodzenia zarówno znaczników jak i zarodka. Promień przechodząc przez zarodek, wzbudza fluorescencyjny barwnik w komórce i powoduje jego świecenie. Wiązka lasera porusza się w linii pionowej. Fluorescencja emitowana z próbki pod kątem 90° do wiązki lasera, jest rejestrowana przez kamerę tworząc obraz w kawałkach grubości tysięcznych milimetra (zobacz film 1w2). Następnie zarodek jest przenoszony o maleńką odległość w poziomie i zaczyna się skanowanie następnego obrazu. Kiedy cały embrion zostanie zeskanowany z jednego punktu obserwacji, jest następnie przekręcany o 180° i ponownie skanowany, tak aby później mógł powstać pełny obraz 3D. Zarodki żyją i rozwijają się, co oznacza, że powstające „kawałki” obrazu embrionu mogą być okresowo odtwarzane i porównywane, aby śledzić zmiany. Naukowcy z EMBL rejestrowali „kawałki” zarodków rybki danio co 60 do 90 sekund przez 24 godziny uzyskując około 400 000 obrazów dla każdego zarodka.
Kolejnym wyzwaniem było opracowanie sposobu analizy wszystkich trzech terabajtów danych dla każdego zarodka. Naukowcy wybrali zautomatyzowane podejście: użyli grupy komputerów pracujących równolegle w EMBL w Heidelbergu oraz w Karlsruhe Institute of Technology w Niemczechw3. „Każdy komputer dostał jedno ujęcie zarodka i miał znaleźć w tym obrazie jądro komórkowe”, wyjaśnia Philipp. Każde jądro reprezentuje komórkę, dlatego łącząc informacje, że wszystkich kawałków obrazu, naukowcy mogą generować cyfrowy zarodek: czyli wizualną podobiznę wszystkich komórek zarodka: gdzie się znajdowały w danym momencie, gdzie się następnie przemieściły oraz kiedy i gdzie się podzieliły. Rezultatem jest film 3D w przyspieszonym tempie z rozwijającym się zarodkiem.
Zdjęcie dzięki uprzejmości EMBL Photolab
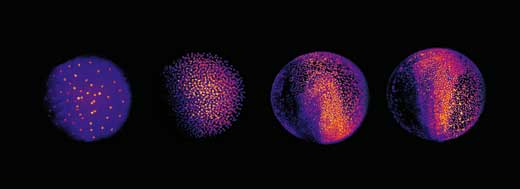
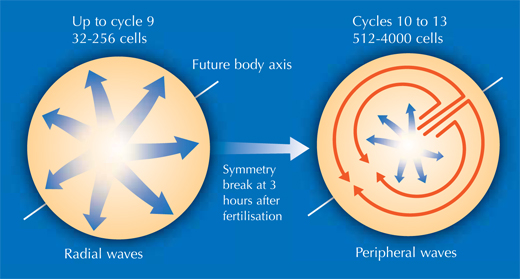
To pozwoliło Philipp, Annette i Jochen rzucić nowe światło na różne stadia rozwoju embrionalnego rybki danio. W bardzo wczesnym stadium, zarodek rybki danio jest w zasadzie grupą komórek znajdujących się na szczycie pęcherzyka żółciowego (pierwszego źródła substancji odżywczych dla zarodka). Na początku komórki dzielą się w falę, która przenosi się z centrum zarodka we wszystkie kierunki, jak woda wypływająca z wypływu na basenie. Rekonstrukcja pokazuje, że po pierwszych dziewięciu cyklach komórkowych, wzór podziału komórek zmienia się w falę, która porusza się z centrum tylko w jednym kierunku. Następnie rozdziela się i kontynuuje wzdłuż obrzeża w dwa półkola (patrz obraz poniżej i film 10w2). Granica pomiędzy tymi dwoma półkolami stanie się później osią ciała zwierzęcia, określaną jako oś symetrii ciała. Tym samym naukowcy odkryli, że oś symetrii ciała rybki danio powstaje dużo wcześniej niż sądzono, w czasie kiedy matczyne geny (w formie mRNA zdeponowanego w jaju) są nadal jedyną kopią używaną do produkcji białek.
Zdjęcie dzięki uprzejmości Nicola Graf
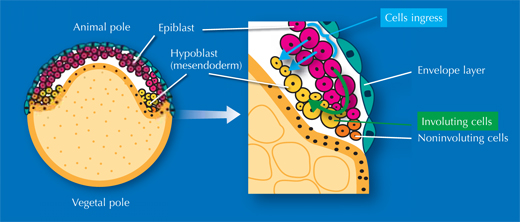
Naukowcy przebadali także gastrulację, czyli proces, w którym komórki embrionalne z pierwotnej pojedynczej warstwy zewnętrznej, migrują do wewnątrz i tworzą pozostałe dwa listki zarodkowe. Z wszystkich trzech powstałych listków zarodkowych powstaną trzy różne typy tkanek. „Potrzeba by dwóch lub trzech stron książki, aby opisać ten proces, ale kiedy widzisz film z cyfrowym zarodkiem, staje się to całkiem proste do zrozumienia,” twierdzi Annette. I co więcej – ona i jej koledzy dowiedli, że dotychczasowe opisy w książkach są złe.
Od lat 80 XX wieku trwa, czasami bardzo żarliwa, debata na temat tego, jak komórki migrują do listków zarodkowych. W książkach przeważa pogląd, że komórki poruszają się spiralnie (inwolucja komórek) – czyli migrują do otwarcia w zarodku zwijając się na brzegach i tworząc warstwę pod spodem, jak krawędź ręcznika kąpielowego, który owija się wokół głowy. Wreszcie niektórzy naukowcy twierdzą, że pojedyncze komórki z zewnętrznej warstwy po prostu się zanurzają, albo dostają do środka, od razu w miejsce, gdzie tworzą warstwę pod spodem.
Zdjęcie dzięki uprzejmości Nicola Graf
„Naprawdę dobrze rozwiązaliśmy ten problem” twierdzi Jochen. „Okazało się, że każdy miał rację!” Wszystko zależy od tego, gdzie patrzysz. Po jednej stronie zarodka komórki ulegają inwolucji, podczas gdy po drugiej stronie, zanurzają się do środka (patrz film 16w2). Kontrowersje pojawiły się ponieważ różni naukowcy obserwowali zarodki z różnych stron. Ponieważ nie mogli obserwować całego procesu rozwoju, nie byli oni w stanie określić, na którą stronę zarodka patrzą. Przezwyciężając te ograniczenia, naukowcy z EMBL byli w stanie odkryć prawdę.
Naukowcy użyli też cyfrowych embrionów jako plan rozwoju, aby dowiedzieć się, gdzie komórki tworzą konkretne organy lub skąd biorą się tkanki. Jako pierwszy przykład użyli oka. W cyfrowym opisie, w zaawansowanym stadium rozwoju (to znaczy pod koniec 24-godzinnego filmu), naukowcy oznaczyli komórki, które wiedzieli, że są zaangażowane w formowanie jednego oka rybki danio. Następnie obserwowali komórki cofając film w czasie, aby zobaczyć jakie jest ich pochodzenie (zobacz film 11w2).
Naukowcy udostępnili cyfrowe zarodki w Interneciew2, razem z narzędziami umożliwiającymi innym naukowcom analizę ich danych z mikroskopu. I co dalej? Dzięki Google Earth, można oglądać całą planetę jak i przybliżać różne miejsca, ale też użytkownicy mogą dodawać swoje własne notatki, znaczniki i przeglądać te dodane przez innych ludzi. Analogicznie, Philipp, Annette, Jochen, i Ernst wyobrażają sobie cyfrowe embriony, które staną się, jak to nazywają „wirtualnymi zarodkami”: zasoby, w których każdy inny naukowiec będzie mógł obserwować procesy rozwojowe, robić zbliżenie po więcej informacji i dodawać swoje własne notatki i wyniki. Na dłuższą metę naukowcy chcieliby poszerzyć zakres cyfrowych zarodków o inne gatunki, co pozwoliłoby naukowcom porównać ilościowo, jak rozwijają się różne zarodki. To dostarczyłoby też ważnego wglądu w ewolucję. Technika cyfrowych zarodków ma duży potencjał, aby się rozwijać, jest też wielu ludzi, którzy chcą pomóc w jej doskonaleniu. Wygląda na to, że ma przed sobą obiecującą przyszłość.
Słownik terminów
Digital scanned laser light sheet fluorescent microscopy (cyfrowy mikroskop fluorescencyjny z laserowym skanowaniem powierzchni, DSLM): Jest to udoskonalona wersja SPIM, która wykorzystuje cienką wiązkę lasera zamiast pełnej wiązki światła, zmniejszając w ten sposób uszkodzenia zarówno próbki jak i barwnika fluorescencyjnego.
Gastrulacja: Faza we wczesnym stadium rozwoju embrionalnego, podczas której formują się trzy listki zarodkowe: ektoderma, mezoderma i endoderma. Czas trwania i molekularny mechanizm gastrulacji różnią się pomiędzy organizmami.
Szczepy genetyczne: Genetycznie jednolita grupa organizmów używana w doświadczeniach laboratoryjnych. Szczepy genetyczne mogą powstawać poprzez chów wsobny, mutację lub inżynierię genetyczną.
Single-plane illumination microscopy (jednopłaszczyznowy mikroskop świetlny, SPIM): Ta metoda pozwala na obserwację w 3D procesów w organizmach żywych, nawet w głębokich warstwach tkanek. Rejestruje fluorescencję pod kątem 90° w stosunku do osi oświetlenia z warstwy wiązki lasera, co pozwala na optyczne cięcie obrazu. Próbka nie jest umieszczona na szkiełku mikroskopowym, ale w wypełnionej płynem komorze, która obraca się podczas obserwacji.
Ryba danio pręgowany, jako organizm modelowy
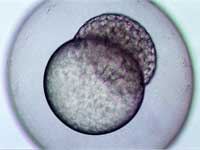
stadium blastuli, 2 godziny i
45 minut po zapłodnieniu
Zdjęcie dzięki uprzejmości
Angharad Jones, Wellcome
Images
Z powodów etycznych nie możemy obserwować wczesnych stadiów rozwoju (embrionalnego) u ludzi. Aby je poznać możemy prowadzić obserwacje u innych zwierząt – organizmów modelowych, ponieważ u wszystkich kręgowców przebiegają one podobnie. Ale dlaczego właśnie rybka danio? Zawdzięczamy to George’owi Streisinger, węgierskiemu biologowi z Uniwersytetu w Oregonie, USA. Na początku lat 80 XX wieku, marzył on o zastosowaniu technik biologii molekularnej, które wcześniej stosował na wirusach, do badania genetyki i rozwoju kręgowców. Jako miłośnik ryb, wybrał rybę danio pręgowany, bo wiedział, że są one łatwe w utrzymaniu i rozmnażaniu. Istnieje kilka praktycznych powodów, dlaczego rybka danio stała się atrakcyjnym organizmem modelowym: po pierwsze, są one wystarczająco małe, aby utrzymać ich dużą liczbę wymaganą do badań genetycznych, ale jednocześnie wystarczająco duże, aby wykonywać klasyczne embriologiczne manipulacje, takie jak transplantacje.
Rybki mają też stosunkowo krótki cykl życiowy (3-4 miesiące), produkują dużą liczbę zarodków (100-200 na krycie) i zapewniają łatwy dostęp do wszystkich stadiów rozwojowych ze względu na zewnętrzne zapłodnienie. Dzięki temu, że embriony są całkowicie przezroczyste i bardzo szybko się rozwijają – już po trzech dniach rozwijają się wszystkie struktury ważne dla dorosłego osobnika, można bardzo łatwo badać ich rozwój – za pomocą prostego mikroskopu optycznego lub bardziej zaawansowanej technologii, takiej jak ta opisana w tym artykule. W dodatku ostatnio został zsekwencjonowany genom rybki danio oraz są dostępne jej genetyczne szczepy, co daje wyjątkową okazję, aby badać nie tylko embriologię, ale także choroby uwarunkowane genetycznie i genetyczne podłoże biologii rozwojowej – marzenie Streisinger’a się urzeczywistniło.
References
- Keller PJ, Schmidt AD, Wittbrodt J, Stelzer EH (2008) Reconstruction of zebrafish early embryonic development by scanned light sheet microscopy. Science 322: 1065-9. doi: 10.1126/science.1162493
Web References
- w1 – Aby dowiedzieć się więcej o EMBL, Europejskim Laboratorium Biologii Molekularnej (ang. European Molecular Biology Laboratory), zobacz: www.embl.org
- w2 – Strona internetowa Cyfrowego Zarodka zawiera filmy ukazujące rozwój zarodków ryby danio pręgowanej oraz dane do pobrania: www.digital-embryo.org
-
Film 1 jest schematycznym przedstawieniem zasady działania DSLM.
-
Filmy 2 i 3 pokazują pierwsze 24 godziny rozwoju zarodka rybki danio.
-
Film 10 ilustruje symetryczną granicę w dzielących się komórkach po dziewięciu cyklach komórkowych i wczesne stadium powstawania osi symetrii zarodka.
-
Film 11 ukazuje szlaki migracji komórek we wczesnym stadium formujących oko ryby danio.
-
Film 16 ilustruje rolę inwolucji i zanurzania się komórek do wewnątrz w procesie gastrulacji u rybki danio.
-
- w3 – Aby uzyskać więcej informacji o Karlsruhe Institute of Technology w Niemczech, zobacz: www.kit.edu
Resources
- Patterson L (2010) Getting ahead in evolution. Science in School 14: 16-20.
- Hodge R (2006) A search for the origins of the brain. Science in School 2: 68-71.
- Materiały szkoleniowe i źródła naukowe dotyczące rozwoju embrionalnego, zobacz: http://people.ucalgary.ca/~browder/virtualembryo
Institutions
Review
W tym artykule opisano najnowsze osiągnięcia w rozwoju biologii. Potencjalny rezultat – wirtualny zarodek, który może być udostępniany i komentowany przez różnych naukowców, podobnie, jak zdjęcia i komentarze są dodawane do Google Earth – to ekscytujący przykład tego, jak wyniki badań mogą być rozpowszechniane, wyjaśniane, i być może rozwijane. Może to również korelować z pomysłami na temat globalnej nauki i komunikacji, które pojawiają się w niektórych programach nauczania.
Jest w tym artykule wiele tematów, które mogą zaciekawić zainteresowanych biologią uczniów. Korzystanie z zaawansowanych technik mikroskopii w przekraczaniu naukowych granic, może doprowadzić do dyskusji na temat, jak technologia hamuje odkrycia lub, jak bardzo naukowa „wiedza” jest przejściowa i wątpliwa, będąc zależną od istniejących technologii.
Wykorzystanie zarodków rybki danio może również sprowokować debatę natury etycznej. Czy mamy prawo do eksperymentowania na zarodkach ryb? Co z zarodkami ssaków? A co z ludzkimi zarodkami? Może to doprowadzić do dyskusji na temat prawnych aspektów tego rodzaju badań.
Uogólniając, artykuł może być przydatny dla nauczycieli biologii, którzy chcą zaktualizować swoją wiedzę. Może być również stosowany jako tekst pomocniczy – dla uczniów przygotowujących się do olimpiady biologicznej lub egzaminów wstępnych na studia. Ponadto materiały filmowe są pomocne w zilustrowaniu rozwoju zarodkowego podczas zajęć, które obejmują ten temat.
Sugerowane tematy do przedyskutowania:
- Opisać i omówić wszelkie kwestie etyczne wynikające z prac prowadzonych przez naukowców.
- Zaproponuj, jak praca na zarodkach ryb może być w przyszłości przydatna w leczeniu chorób u ludzi.
Sue Howarth, Wielka Brytania





