Supporting materials
Download
Download this article as a PDF

Traduit par Camille Ducoin. Aimez-vous le spectacle de la science? Les couleurs, les odeurs, les intrications? Pourquoi ne pas suivre les suggestions suivantes de Bernhard Sturm, enseignant de science: laissez vos élèves apporter encore plus de spectacle dans la classe, en (re)jouant la…

Le théâtre peut combiner des éléments d’art, de musique et de sport, développant la créativité des élèves et leur forme physique aussi bien que leur sensibilité émotionnelle et esthétique. En tant qu’activité d’équipe, il favorise la communication et la coopération entre jeunes condisciples. Alors, pourquoi ne pas employer le théâtre en cours de science?
Cet article propose quelques activités théâtrales pour jouer ou rejouer la science en classe de physique-chimie.
Voici une méthode pour visualiser les échanges d’oxygène entre différents métaux d’une série redox (d’après Lavoisier). Chaque élève porte un maillot de couleur, à choisir parmi trois couleurs représentant les atomes d’oxygène et de deux métaux différents (il en faut le même nombre de chaque couleur). En groupes de 8-10, les élèves répètent des réactions rédox simples de stoechiométrie 1:1, telles que CuO + Fe → Cu + FeO, puis ils les représentent devant toute la classe. Les élèves trouvent souvent des façons créatives d’exprimer l’énergie d’activation et l’énergie libérée dans ces réactions.
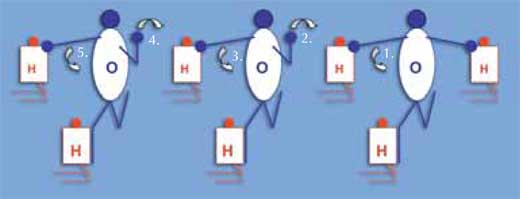
On peut utiliser la méthode suivante pour montrer comment passe un courant électrique dans l’eau sans que les protons se déplacent: il y a transmission d’une charge positive. Les élèves doivent porter des maillots de deux couleurs, représentant les atomes d’hydrogène et d’oxygène (proportion 2:1). Formez une ligne de molécules d’eau: chaque molécule est composée de deux hydrogènes (à genoux) et un oxygène (debout). L’atome d’oxygène touche un hydrogène avec sa main droite, et l’autre avec son pied droit (voir schéma à droite). Les bras et jambes des atomes d’hydrogène n’ont pas de fonction. Un hydrogène supplémentaire est attaché à l’oxygène situé à l’une des extrémités, touché par sa main gauche (H3O+). Les bras et jambes des élèves oxygènes représentent les paires d’électrons. La paire d’électrons en plus passe d’un bout à l’autre de la chaîne de molécules d’eau: l’oxygène de la molécule H3O+ lâche l’hydrogène qu’il tenait de sa main droite, qui est récupéré par la main gauche de l’oxygène suivant; et ainsi de suite, jusqu’au bout de la ligne.
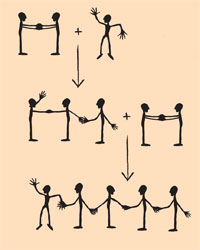
La méthode suivante est utile pour comprendre le mécanisme de polymérisation et faire la différence entre la synthèse de polymères linéaires ou réticulés. On illustre la polymérisation de l’éthène en intégrant les élèves un par un. Chaque buste représente un atome de carbone, chaque pied un hydrogène, et chaque bras un électron de valence. Un élève isolé (représentant un radical méthyle) agite le bras (un électron non apparié). Deux élèves se tiennent par les deux mains (une double liaison), représentant la molécule d’éthène. Le radical vient se lier à la molécule d’éthène: l’un des composants de cette molécule doit lâcher une des mains occupées par la double liaison pour prendre la main du radical (nouvelle liaison). La molécule résultante, constituée de trois carbones, est un nouveau radical, qui se lie à une autre molécule d’éthène, et ainsi de suite (voir schéma à gauche).
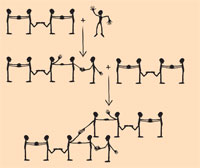
Ce modèle peut être étendu pour représenter la réticulation du buta-1,3-diène: les élèves représentant les atomes C2 et C3 de la molécule mettent un de leurs pieds en contact pour sympoliser la liaison simple (voir schéma à gauche). L’arrivée d’un radical méthyle provoque la rupture d’une des doubles liaisons (doubles poignées de mains) du buta-1,3-diène; une nouvelle liaison (poignée de mains) est formée entre le radical méthyle et, par exemple, l’atome C4. La nouvelle molécule obtenue est aussi un radical, avec un électron libre en C3. L’atome C1d’une autre molécule de buta-1,3-diène peut s’y lier, en cassant son double lien et en formant une laison réticulée (nouvelle poignée de mains) avec l’atome C3 ode la première molécule. La molécule résultante, à neuf carbones, est aussi un radical, avec un électron non apparié en C2 de la seconde molécule de buta-1,3-diène.
Selon que l’eau soit dans son état solide, liquide ou gazeux, l’espacement et la vitesse de ses molécules varient. Dans cet exercice, les élèves jouent les molécules d’eau. Selon mon expérience, il vaut mieux pratiquer dehors, où il y a plus d’espace; cela aide aussi à séparer la classe entre filles et garçons – un groupe joue, l’autre regarde. L’enseignant explique comment se déplacer selon les saisons. On commence par l’hivers (0 °C), les élèves doivent se tenir immobiles et former un réseau. Au fur et à mesure que l’année avance, arrivent le printemps, puis l’été: les molécules bougent plus vite (jusqu’à 40 °C), mais restent toujours en contact. Pour finir, les molécules se retrouvent dans une bouilloire, chauffent et s’evaporent (100 °C).
À chaque phase, l’enseignant prend un instantané de l’état en criant “Stop!”. Les acteurs (par exemple les filles) et spectateurs (par exemple les garçons) décrivent ce qu’il se passait avant et ce qu’ils voient maintenant.
Cette activité peut être modifiée pour illustrer l’expension thermique du benzène, avec huit élèves entourant une vingtaine d’élèves “benzènes” avec une corde détendue, jusqu’à ce que la pression générée par chauffage devienne trop forte et que les élèves tenant la corde soient obligés de la lâcher.
L’histoire du vide peut être enseignée en s’appuyant sur la peinture de Joseph Wright of Derby, Expérience sur un Oiseau dans la Pompe à Airw1 (1768).
Séparez la classe en groupes de trois, et donnez à chaque groupe une copie de la peinture et une feuille de travail où sont représentées en silhouette les appareils et personnages principaux (voir image à droite; téléchargeable en lignew2). Les trois questions suivantes permettent de démarrer la discussion autour de la peinture:



Après la discussion, la scène peut être rejouée par les élèves en utilisant une pompe à vide, avec un ‘Schokokuss’ (petit gâteau à la crème recouvert de chocolat) à la place de l’oiseau.
Cette activité permet d’introduire la notion d’électrons en tant que charges mobiles transportant de l’energie.Un élève représente la source d’energie (un batterie): il ou elle se tient dans un coin de la classe et tend des petits sachets de bonbons (l’énergie). À l’autre bout de la classe, un autre élève représente le ‘consommateur’ d’énergie: il ou elle reçoit les sachets. Vous pouvez former un circuit en disposant des tables au centre de la pièce.
Les autres élèves représentent les électrons: ils font la queue à la source d’énergie et, un par un, reçoivent un sachet de bonbons; puis ils entrent dans le ‘circuit électrique’ et marchent ou courent vers le ‘consommateur’ pour lui remettre les sachets (énergie). Puis ils retournent vers la source et refont la queue. L’électricité continue de circuler jusqu’à ce que l’élève source soit à court de sachets (la batterie est à plat). Cette activité peut être étendue pour représenter des circuits en parallèle ou en série.
Cette activité permet de montrer que la conductivité des métaux diminue lorsque la température augmente; un effet qui, autrement, ne peut être déterminé qu’expérimentalement. À l’extérieur, tracez à la craie un rectangle de 2 x 5 m pour représenter la section d’un câble conducteur. Demandez à une vingtaine d’élèves de se tenir dans le rectangle: ils représentent les atomes du métal. Les 10 élèves restants (électrons) essaient de courir à travers le câble, tandis que les atomes restent immobiles (basse température), ou oscillent en s’agitant (haute température). Le temps mis par les ‘électrons’ pour traverser le ‘câble’ est chronométré.

our introduire ce sujet, demandez à un élève (élève No 1) de lire à voix haute l’histoire de la découverte de la chute librew3. Pendant qu’un des assistant de Galilée (élève No 2) marque le temps en jouant des accords de guitare réguliers, Galilée lui-même (élève No 3) et son deuxième assistant (élève No 4) effectuent leurs expériences avec un balle de tennis (ou autre – une balle plus rigide donne de meilleurs résultats) et un plan incliné muni de cordages métalliques à différentes hauteurs (voir image à gauche).
On laisse la balle rouler jusqu’en bas du plan incliné, à partir de différentes hauteurs. L’élève No 4 note:
En une seule leçon, cette méthode donne une excellente illustration de l’idée de demi-vie, sans le moindre appareil expérimental compliqué ou dangereux.
Un plateau de jeu de 6 x 6 cases est occupé par 36 jetons rouges. On lance deux dés, faciles à distinguer: leurs nombres sont utilisés comme valeurs de X (dé No1) et Y (dé No2). Le jeton rouge de la case de coordonnées (X,Y) est remplacé par un jeton bleu (il s’est désintégré). Si une même paire de nombres est à nouveau obtenue, rien ne se passe pour les pièces, mais le double coup est compté. Après chaque ensemble de 10 doubles coups, on note le nombre total de fois que les dés ont été lancés (t) et le nombre de jetons rouges restants (N). Une courbe représentant N en fonction de t sert à déterminer la demi-vie.
Pour illustrer différentes demi-vies, vous pouvez utiliser un dé à huit faces et un plateau de 8 x 8 cases, ou changer les règles de façon à ce que chaque case doive être désignée deux fois avant que le jeton rouge ne se désintègre.
Une partie des activités décrites dans cet article ont été inspirées par le travail d’autres personnes. L’auteur souhaite donc reconnaître sa dette envers Pöpping (2003; Radical polymerisation of ethene to polyethylene), Schreiber (2004; Physical states of water), Fallscheer (2006; Electric circuit), Bührke (2003), Drake (1975), Hepp (2004), Riess et al. (2005; Galileo’s law of free fall), et Barke & Harsch (2001; Nuclear disintegration and half-life).
Pour des informations détaillées sur la peinture de Joseph Wright, reportez-vous à sa description sur http://en.wikipedia.org/wiki/An_Experiment_on_a_Bird_in_the_Air_Pump
Cet article donne des idées claires et précises sur la façon dont les enseignants peuvent utiliser le théâtre pour aider les élèves à apprendre des concepts abstraits en physique et chimie. Ces activités peuvent être menées tout en abordant des sujets standards du programme.
Les activités proposées ne demandent pas d’équipement cher ni compliqué, ce qui les rend faciles à pratiquer en classe. Des instructions claires et concises sont données aux enseignants sur la manière d’introduire l’écriture créative et le jeu de rôles dans leurs cours. Non seulement cela rend le cours de science plus intéressant et amusant pour les élèves, mais cela leur permet aussi de se sentir plus impliqués et responsables de leur propre expérience d’apprentissage. Cette approche plaira aussi aux étudiants qui ont plus d’affinités avec les matières littéraires et artistiques, car elle stimule leur imagination et leur créativité. Cet article peut aider les enseignants à appliquer progressivement des petits changements dans leurs cours, et donner de nouvelles idées à ceux qui pratiquent déjà ce genre d’activités en classe.
Catherine Cutajar, Malte
Download this article as a PDF