Supporting materials
Download
Download this article as a PDF

Tradus de Gabriela Badea. Vă bucuraţi de spectacolul ştiinţei?Culoarea, mirosul,chichiţele? De ce să nui urmezi sfaturile profesorului Bernhard Sturm: lăsaţi studenţii să aducă mai multă dramă la ore prin redecretarea ştiinţei, să îi ajutăm să vizualizeze şi să reţină…

Teatrul poate combina elemente din artă, muzică şi sport şi dezvoltă creativitatea şi iscusinţa studenţilor la fel de bine ca şi simţul estetic şi emoţional. Ca activităţi de echipă, ele favorizează comunicarea şi cooperarea dintre tineri. Aşa că de ce să nu folosim teatrul la predarea ştiinţelor?
Articolul oferă o selecţie de activităţi bazate pe teatru, pentru a reprezenta sau reinterpreta ştiinţa la orele de chimie şi fizică.
Aceasta este o metodă de a vedea schimbul de oxigen dintre diferiţi atomi de metale din seria redox(după Lavoisier). Fiecare student poartă un tricou cu una din cele trei culori, care reprezintă atomii de oxigen şi două metale diferite (ar trebui să fie un număr egal din fiecare culoare). În grupuri de câte 8-10, studenţii reprezinta reacţii redox simple cu raportul stoichiometric 1:1, cum ar fi CuO + Fe → Cu + FeO, după care se prezintă in faţa clasei. Studenţii găsesc de cele mai multe ori moduri creative de reprezentare a energiei de activare şi eliberare a energiei in aceste reacţii.
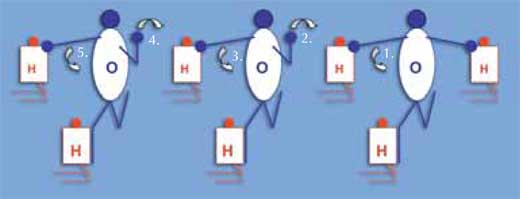
Urmatorea metodă se poate folosi pentru a demonstra cum un curent electric trece rapid prin apă, deşi protonii nu se mişcă: în schimb, o sarcină pozitivă este transmisă. Studenţii trebuie sa poarte tricouri cu una din cele două culori, reprezentând atomii de hidrogen şi oxygen (raport 2:1). Se aranjează într-o linie de molecule de apă: fiecare moleculă constă din doi atomi de hidrogen (îngenunchiaţi) şi un atom de oxygen (staţionar). Atomul de oxigen atinge cu mâna dreaptă un atom de hidrogen şi celălalt atom de hidrogen cu piciorul drept (vezi diagrama de pe dreapta). Mâinile şi picioarele atomului de hidrogen nu au nici o funcţie. Un atom suplimentar de hidrogen este ataşat la atomul de oxigen (atins de mâna stângă sau piciorul stâng) la unul din capete (H3O+). Mâinile şi picioarele studenţilor oxigen reprezintă perechi electronice. Surplusul de legături de perechi este transferat de la un capăt al moleculei de apă la celălalt capăt, în timp ce oxigenul din molecula H3O+ dă drumul la un atom de hidrogen cu mâna lui dreaptă; în schimb, atomul de oxigen din molecula învecinată atinge acest atom cu mâna lui stângă, şi tot aşa în continuare.
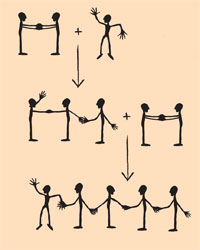
Urmatoarea metodă este folositoare în întelegerea mecanismului de polimerizare şi diferenţiere între sinteza polimerilor liniari şi a celor încrucişaţi. Polimerizarea etenei este ilustrată integrând toţi studenţii unul câte unul. Fiecare corp reprezintă un atom de carbon, fiecare picior un atom de hidrogen si fiecare mână un electron legat. Un singur student (reprezentând un radical metil) îşi unduieşte mâna (un electron fără pereche). Doi studenţi ţinând ambele mâini (o dublă legatură) reprezintă o moleculă de etenă. Radicalul se leagă la molecula etenei: una dintre componentele moleculei de etenă trebuie să rupă o legutară a mainilor (electron legat) şi să se lege la un electron liber al radicalului (noua legatură a mâinilor). Molecula cu trei atomi de carbon rezultată este iar un radical. Acesta se leagă la o altă moleculă de etenă şi tot aşa (vezi diagrama de pe stânga).
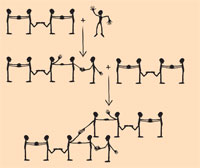
Acest model se poate extinde pentru a reprezenta legatura încrucişată a buta-1,3-dienei: studenţii care reprezintă atomii C2 si C3 C3 din moleculă îşi ating picioarele pentru a simboliza legatura simplă (vezi diagrama de pe dreapta). Venirea unui radical metil face ca una din dublele legaturi din buta-1,3-dienă să se spargă şi o nouă legatură se formează între radicalul metil si, de exemplu, atomul C4. Molecula nou formată este tot un radical, cu un electron liber la C3. Atomul C1 de la o a-II-a moleculă de buta-1,3-dienă poate să se lege, rupând dubla legatură şi formând o legatură în cruciş cu atomul C3 al moleculei originale. Molecula cu 9 atomi de carbon rezultată este tot un radical, cu un electron liber la C2de la molecula a-II-a de buta-1,3-diena.
Distanţa şi viteza dintre moleculele de apă diferă de la stările de solidă,lichidă şi gazoasă. În acest exerciţiu, studenţii joacă rolul moleculelor de apă. Din experienţa mea, este mai bine dacă se face afară, unde este mai mult spaţiu, şi se poate împărţi clasa în adolescenţi băieţi şi fete- un grup joacă,celălalt se uită. Profesorii le spun elevilor cum să se mişte: începând cu iarna (0 °C), studenţii ar trebui să stea nemişcaţi şi într-o formaîie de reţea. În timp ce anul curge uşor, devine primăvara şi vara, şi moleculele se mişca mai repede(pana la 40 °C),dar tot rămân în legatură. În final, moleculele sfârşesc într-un ibric, se încălzesc şi se vaporizeaza(100 °C).
In fiecare fază, profesorul captează un instantaneu ţipând”Opriti-vă!” Actorii (de ex.fetele) si privitorii(ex.baieţii) descriu ce se intamplă înainte şi ce pot vedea în jurul lor acum.
Grupul de actori si spectatori isi schimbă apoi rolurile şi moleculele se “răcesc” iar la 0 °C.
Această activitate poate fi modificată pentru a demonstra dilatarea benzenului, cu opt studenţi înconjurând aproximativ 20 de studenţi “benzen” cu o funie slăbită, până când presiunea prin “încălzire” devine prea puternică şi studenţii înconjurători sunt forţaţi să dea drumul la funie.
Tabloul Un Exeriment pe o Pasăre într-o Pompă de Aerw1 de Joseph din Derby(1768) poate fi folosit pentru a învăţa istoria vacuum-ului.
Împarte clasa în grupe de câte trei, şi oferă fiecărui grup o reeditare a picturilor şi o foaie de lucru reprezentând dispozitivele principale şi personajele (vezi imaginea din dreapta; a fi downloadată onlinew2). Următoare trei întrebări tind să promoveze discuţiea despre tablou:



După discuţie, întreaga scenă poate fi reinterpretata de catre studenţi folosind o pompă de vid, cu un ‘Schokokuss’ ( o mică prăjitură de ciocolată) petru a înlocui pasărea.
Această activitate este folositoare pentru introducerea ideii de electroni ca sarcini care se deplasează şi care transportă energie. Un elev reprezinză sursa de energie (o baterie): el sau ea stă la un capăt al clasei şi împarte punguţe cu jeleuri (energie). La celălalt capăt un alt elev reprezintă “consumatorul” energiei: el sau ea colectează pungile. Puteţi pune nişte mese în centrul camerei pentru a marca un circuit.
Elevi rămaşi reprezintă electronii: ei stau la rând în dreptul sursei de energie şi , fiecăruia, i se dă o punga cu jeleuri, apoi intră în “circuitul electric” şi merge/aleargă la “consummator” pentru a-i da dulciurile(energia). Apoi ei merg din nou la sursă ca să se aşeze la coadă. “Electricitatea”continuă să circule până când sursa student rămâne fără pungi(bateria este descărcată). Această activitate se poate extinde şi să reprezinte circuite în serie şi in paralel.
Această activitate este utilă pentru a demonstra că odată cu creşterea temperaturii conductivitatea metalelor scade, un lucru care poate fi demonstrate altfel numai experimental. Afară, foloseşte cretă pentru a desena un dreptunghi de 2 x 5 m pentru a reprezenta intersecţia unui cablu conductor. Roagă aproximativ 20 de elevi să stea in dreptunghiul respectiv; ei reprezintă atomii de metal. Ceilalţi 10 stundeţi (electronii) rămaşi încearcă să alerge prin cablu în timp ce atomii stau pe loc (temperatură redusă) sau să oscileze prin a-şi mişca corpurile (temperatură ridicată). Timpul alocat trecerii “electronilor” să treacă prin “cablu” este masurat cu un cronometru.

Pentru a introduce subiectul, roagă un elev (elevul 1) să citească serios despre descoperirea legii căderii liberew3. În timp ce unul dintre asistenţi lui Galileo (elevul 2) marcheză timpul prin ritmuri de chitară, Galileo însuşi (elevul 3) şi cel de-al doilea asistent al său (elevul 4) îşi continuă experimentele cu o minge de ping-pong (sau ceva asemănător – o bilă mai solidă dă rezultate mai bune) şi un plan înclinat cu legături (din metal) la diferite înălţimi (vezi imaginea din stânga).
Mingea este lăsată să se rostogolească pe planul înclinat de la diferite înălţimi. Elevul 4 înregistrează:
În doar o lecţie, acestă metodă produce material excelent pentru a ilustra ideea timpului de injumatatire, fară aparatură experimentală complicată sau periculoasă.
Un joc de societate de 6 x 6 câmpuri este umplut cu 36 de piese roşii de joc. Două zaruri sunt aruncate şi numerele lor sunt folosite ca valori X (zarul 1) şi Y(zarul 2). Piesele roşi de pe câmp care corespund coordonatelor (X, Y) de pe zar se descompun (sunt înlocuite de) într-o piesă albastră. Dacă o pereche de numere este aruncată a doua oară, nu se întâmplă nimic cu piesele , dar aruncarea dublă se notează.După fiecare set de 10 duble, numărul total de aruncări ale celor două zaruri (t) şi numărul pieselor roşii rămase (N) sunt notate. Graficul reprezentarii lui N in functie de t este folosit pentru a determina timpul de înjumătăţire.
Pentru a ilustra timpi de înjumătăţire diferiti, ai putea folosi zaruri cu 8 feţe şi un joc de societate cu 8 x 8 câmpuri, sau să schimbi regulile pentru ca fiecărui camp să îi fie necesar o dublă lovitură pentru ca piesele roşii să dispară.
Câteva dintre activităţile din acest articol au fost inspirate din munca altora. Autorul, pentru acest motiv, ar dori să isi confirme datoria fata de Pöpping (2003; Radical polymerisation of ethene to polyethylene), Schreiber (2004; Physical states of water), Fallscheer (2006; Electric circuit), Bührke (2003), Drake (1975), Hepp (2004) şi Riess et al. (2005; Galileo’s law of free fall), şi Barke & Harsch (2001; Nuclear disintegration and half-life).
Acest articol ofera idei clare şi specifice despre cum profesorii se pot folosi de teatru pentru a facilita învăţarea conceptelor abstracte în fizică şi chimie de către elevi. Activităţile pot fi folosite în principal pentru a aborda subiecte standard în curriculum.
Ideea că activităţile sugerate nu necesită resurse complicate sau costisitoare, le face să fie uşor de utilizat în clasă. Profesorilor le sunt date îndrumări clare şi concise despre cum să includă scrisul creativ şi jocul pe roluri în lecţiile lor. Acest lucru nu face lecţiile mai interesante şi distractive pentru elevi, ci îi face să se simtă mai implicaţi şi responsabili petru experineţa lor a învăţa. Acest lucru va atrage de asemenea elevi care sunt orientaţi mai mult către limbi şi arte ,deoarece le stimulează imaginaţia şi creativitatea. În plus, poate ajuta profesorii să aplice mici schimbări asupra modului lor de predare, cât şi pentru a aduce noi idei pentru profesorii care au început să implementeze activităţi similare la clasă.
Catherine Cutajar, Malta
Download this article as a PDF