Smarphones en el laboratorio, ¿es muy azul el azul? Teach article
Traducido por Luis Cebollada. Exploramos los colores de la química con un smartphone
Si disolvemos cobre en un ácido nítrico acuoso la disolución se vuelve azul. Cuanto más cobre haya más intenso será el color. Pero, ¿cómo podemos saber exactamente cuánto cobre hay disuelto analizando el color?
Sabemos que cuando disolvemos un sirope en agua, el color se aclara. Sucede porque la absorción de la luz, que es la responsable del color, es proporcional a la concentración del colorante disuelto (de acuerdo con la ley de Beer-Lambert). En esta actividad, estudiantes de 13 a 18 años comprueban esta ley usando aplicaciones de móvil que caracterizan los colores.

Esta actividad está planteada para química, pero puede ser adaptada a matemáticas. Los alumnos tienen la oportunidad de practicar el método científico. Tienen que contestar una pregunta –cuánto cobre hay disuelto. Tienen que elegir el método antes de medir, recoger datos, organizarlos en una tabla y hacer una gráfica para estimar el contenido de cobre en la disolución.
Sugerimos cuatro posibles protocolos:
- La clásica receta que contiene todos los detalles sobre el proceso.
- Un protocolo para la clase de matemáticas: todas las disoluciones están preparadas con anterioridad y los estudiantes sólo hacen las medidas y el análisis posterior.
- Un protocolo abierto en el que los alumnos reciben algo de información y una pregunta para contestar.
- Un protocolo cooperativo que sugiere la colaboración entre centros.
Receta química
El profesor o el laborante preparan una disolución desconocida de cobre con, al menos, un día de antelación (ver cuadro). Después, los estudiantes trabajan en la actividad que durará aproximadamente una hora y media.
Preparación de la disolución problema de cobre
Nota de seguridad
El ácido nítrico (HNO3) es corrosivo y debe manejarse con guantes y gafas bajo campana de humos. La reacción produce grandes cantidades de gases tóxicos por lo que se debe preparar en la campana, al menos con un día de antelación.

cobre
Imagen cortesía de Science on
Stage
Materiales
- 1.5–3.5 g de cobre
- 7.5–17.5 cm3 65% HNO3
- Agua destilada
- Vaso de precipitados de 50 cm3
- Matraz de 100 cm3
Procedimiento
- Toma entre 1.5 y 3.5 g de cobre (anota la masa exacta m(Cu)).
- Añade 5m(Cu) cm3 de HNO3 al 65% en un vaso de 50 cm3 (p.e. 2 g de cobre necesitan 5 x 2 = 10 cm3 de ácido nítrico).
- Añade el cobre (con cuidado si está en polvo), cierra la campana de humo y espera hasta que el cobre esté disuelto.
- Después, añade gota a gota 30 cm3 de agua y transfiere la solución a un matraz aforado de 100 cm3, enrasa con agua hasta 100 cm3 y cierra el matraz. Agita bien.
La escala de calibración
Materiales
- 30 g de nitrato de cobre hidratado (Cu(NO3)2∙3H2O)
- Agua destilada
- Tres matraces de 100 cm3
Procedimiento
- Etiqueta los matraces 1, 2 y 3.
- Añade 5g, 10g o 15g de Cu(NO3)2∙3H2O a cada matraz. Calcula las masas exactas m1, m2 y m3 de cobre en cada matraz.
- Enrasa a 100 cm3; cierra los matraces y agita bien. Esta es la escala 1, 2 y 3.
Nota: puedes sustituir el Cu(NO3)2∙3H2O que absorbe con facilidad agua, por sulfato de cobre (CuSO4·5H2O – usa las mismas cantidades) o por la sal anhidra, CuSO4 (en este caso toma 3.3 g, 6.6 g y 10 g).
Medida de los valores H con un smartphone
Materiales
-

Los alumnos van a medir el
valor H con el teléfono
Imagen cortesía de Science on
StageMatraces 1, 2 y 3 (con las disoluciones de referencia preparadas según las instrucciones)
- Un smartphone con la aplicación Color Grab (android) o ColorAssist Free Edition (iOS)w1
- Hoja grande de papel blanco
- Lápiz
Procedimiento
- Coloca el matraz 1 sobre un trozo de papel blanco (de manera que la base y la parte posterior del matraz tengan fondo blanco) y marca con el lápiz la posición exacta del matraz.
- Coloca el smartphone sobre la mesa para que el centro de la cámara apunte a la parte ancha del matraz (enfoca en horizontal).
La distancia entre el matraz y el fondo debe de ser de unos 4 cm, y entre el teléfono y el matraz, de unos 14 cm. - Abre la aplicación para leer en valor H (o el modelo de color HSV o HSL, que se explica más adelante).
- Repite los pasos con 2 y 3, usando la misma disposición.
Medida de la disolución problema
- Usa los valores m1, m2, y m3 que hemos calculado antes para dibujar una gráfica del valor H frente a la masa de cobre. El valor H es proporcional a la concentración del soluto, así la gráfica debe de ser una recta.
- Siguiendo el protocolo, mide el valor H de la disolución desconocida.
- Utiliza la gráfica para determinar la masa de cobre en la disolución problema.
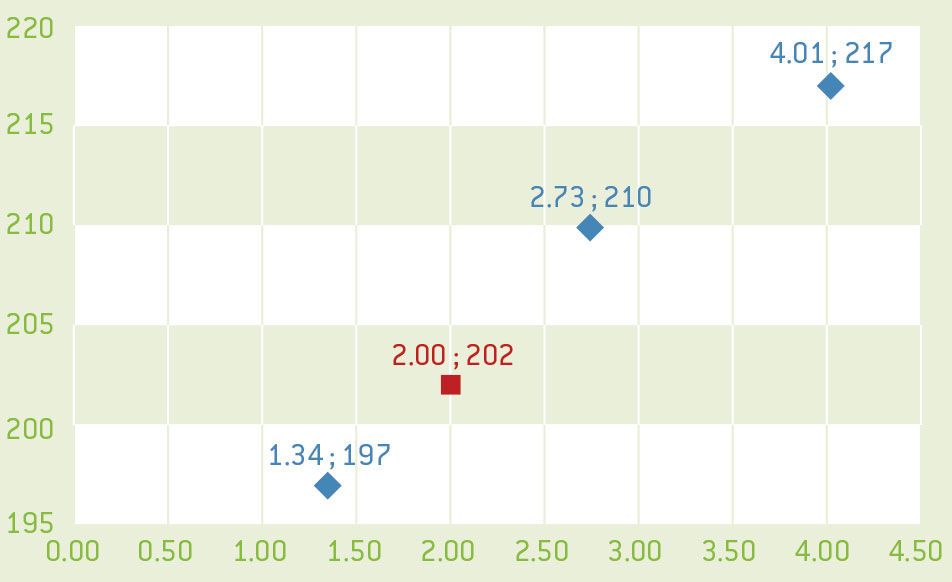
Imagen cortesía de Science on Stage
Protocolo de clase de matemáticas
El profesor prepara las cuatro disoluciones y etiqueta los matraces de referencia indicando la masa exacta de cobre. Prepararemos con antelación las disoluciones que nuestros alumnos necesitarían para conducir el experimento con éxito. Este procedimiento requiere unos 45 minutos.
Procedimiento
- Instala la app en tu teléfono averigua cómo saber el color. Tendrás que saber cómo detener la medición de colores y utilizar el flash para hacer las medidas.
- Mide los valores H de las disoluciones de los tres matraces que están etiquetados con la masa de cobre que contienen.
- Dibuja la gráfica que relaciona el valor H con el contenido de cobre. Cuanto más cobre contenga la disolución más oscura será.
- El cuarto matraz contiene una cantidad desconocida de cobre. Mide el valor H de la disolución y usa la gráfica para determinar la masa de cobre.
Protocolo abierto
Pide que instalen la aplicación y que averigüen cómo funciona. Dales tres matraces con las masas de cobre en cada una de ellas pregunta cómo obtener de manera fiable el contenido de cobre en el cuarto matraz usando el valor H.
Variante cooperative
Los estudiantes hacen el experimento y con sus teléfonos graban un vídeo en el que explica cómo hacer el experimento. Este vídeo se envía a otra clase (del mismo centro o de otro país) quienes tienen que seguir el mismo protocolo.

Cómo funciona la app
La aplicación identifica los colores que capta la cámara y muestra los valores numéricos de los colores en diferentes formatos (RGB, HSV, LAB, etc.). Puede ser útil si quieres comprar pintura de un determinado color; basta con medir el color con tu smartphone y pedir justo ese color en la tienda.
La más conocida es RGB (que es la misma que forma imágenes en las pantallas), pero los valores no están relacionados con la longitud de onda del color. El sistema RGB utiliza una longitud de onda para cada color primario. El valor H (Hue significa matiz) de las codificaciones HSV ó HSL distingue diferentes tonalidades de azul (azul marino, flor de maíz, azul vaquero, lila, etc). Podemos utilizar este valor en lugar de la absorción para hacer determinaciones en un determinado rango de concentraciones.
Aunque no lo hemos probado aún, creemos que este método podría funcionar con otras sustancias (el permanganato de potasio o los líquidos de colorante alimenticio). Para eso hay que identificar el rango en el que el valor H es proporcional a la concentración de la disolución.
Hemos probado con la col lombarda y los colores que da como indicador pero no funcionan porque las longitudes de onda de los diferentes rojos de la col no varían linealmente con el pH. La aplicación no es ni siquiera capaz de diferenciar las tonalidades entre pH 3 y pH 10, los colores de la col lombarda (rosa, púrpura, verde o amarillo) por sí mismos nos ayudan a deducir posibles valores de pH. Como lo que podemos apreciar a simple vista, no vale la pena usar smarphones.
Agradecimientos
Esta actividad se llevó a cabo por primera vez en Science on Stage y se publicó en una colección de artículos sobre el uso de smartphones en ciencia, iStage 2w1. Se desarrolló por la colaboración entre profesores que comenzó en Viena, Austria, y que siguió por correo electrónico y a través de la plataforma de enseñanza de código abierto Moodle. Trabajaron 20 profesores de 14 países y publicaron 11 unidades que muestran cómo usar los smartphones y las aplicaciones en clases de matemáticas, física, química o biología.
iStage 2 es una colección de ejemplos recogidos por toda Europa de cómo integrar los smartphones en las clases. Esta es la segunda publicación de la serie iStage que aborda la integración de recursos digitales en las clases de ciencias y matemáticas. Está disponible e impreso en inglés y alemán, financiado por SAP. Hay versión en ebook además de la versión impresa.
Web References
- w1 – Todas las apps y los materiales están disponibles en la web de Science on Stage.
Institutions
Science on StageReview
He visto a uno de los autores, Marc Montangero, realizar esta práctica en mi centro. El artículo es una nueva aproximación a la enseñanza de la ley de Lambert-Beer sin espectrómetro; se usa un Smartphone por lo que el equipamiento es muy sencillo. Pero hay que instalar una aplicación en cada aparato.
Esta actividad puede usarse para reflexionar sobre cuándo estudiar la concentración en masa y concentración molar; la relación entre el color y la longitud de onda; la ley de Lambert-Beer; el espectro visible.
Maurice Cosandey, Ecole Polytechnique Fédérale de Lausanne, Switzerland





