Gefangen im eigenen Leib Understand article
Übersetzt von Stefan Mockenhaupt. Die Gruppe um Winfried Weissenhorn am Europäischen Laboratorium für Molekularbiologie in Grenoble, Frankreich, hat Möglichkeiten entdeckt, mit einer ganzen Reihe von gefährlichen Viren fertig zu werden – indem man sie in ihrer Hülle gefangen…
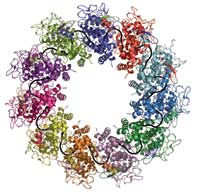
(in verschiedenen Farben) binden
an ein RNA Molekül (schwarz) um
einen Komplex zu bilden
Mit freundlicher Genehmigung von
Winfried Weissenhorn
Es ist eine der gefürchtetsten Krankheiten der Welt. Die klassischen Symptome – Verwirrtheit, Sabbern, Angst vor Wasser, Lähmungen -, führen nach ihrem Auftreten fast immer zum Tod. Nur fünf Personen haben jemals einen Tollwutausbruch überlebt, und alle außer einer litten danach an permanenten neurologischen Schäden. Obwohl Impfungen und Präventivmaßnahmen im Anschluss an mutmaßliche Infizierungen den Einfluss dieser Krankheit in Europa und Nordamerika dramatisch verringert haben, gibt es immer noch kein Heilmittel. Tollwut bleibt weiterhin eine ernsthafte Bedrohung in vielen Entwicklungsländern und tötet bis zu 70000 Menschen pro Jahr.
Beunruhigenderweise könnten Tollwut und ähnliche Viruserkrankungen auch in Industrieländern wieder auftauchen, indem Menschen in Kontakt mit Fledermäusen geraten. Daher kommt die Entdeckung von Winfried Weissenhorn, Rob Ruigrok und Kollegen zur Bekämpfung der Viren sehr passend. Die Gruppen, die am Europäischen Laboratorium für Molekularbiologie in Grenoble, Frankreich, und der benachbarten Abteilung für Wechselwirkungen zwischen Virus und Wirtszelle (Unit of Virus Host Cell Interactions – UVHCI), angesiedelt sind, haben die Struktur des Proteins entschlüsselt, welches das genetische Material des Virus ummantelt und es vor dem körpereigenen Immunsystem versteckt, bis es die Chance hat sich zu vervielfältigen. Es könnte möglich sein, mit Hilfe von Medikamenten das Genom in dieser schützenden Hülle einzuschließen und somit die virale Replikation zu unterbinden.
Diese Arbeit hat jedoch Auswirkungen, die über die einzelne Krankheit Tollwut hinaus gehen. Denn interessanterweise besitzen viele andere Viren, u.a. Ebola, Bornavirus und Masern, ähnliche Hüllen für ihre Genome, sodass die Ergebnisse auch Aufschluss darüber geben könnten, woher solche Viren kamen und wie sie entstanden sind. Das Tollwutvirus bildet genau wie auch mehrere andere Viren sein Genom aus einer einzelsträngigen RNA, einem Molekül, das der DNA ähnelt, welche unsere Gene trägt. Aber anders als bei DNA kann die Information, die von der Virus RNA kodiert wird, nicht direkt benutzt werden, um die Proteine zu produzieren, welche benötigt werden, um das Virus aufzubauen. Statt dessen verhält es sich wie eine komplementäre Kopie, eine Art chemisches Photonegativ der benötigten Sequenz. Bevor das Virus also die Proteine produzieren lassen kann, welche die Schutzhülle für ihr Genom bilden, muss dieser „negative RNA-Strang“ in einen „positiven“ überführt werden, welcher in Proteine übersetzt werden kann. Ausserdem muss es sein Genom vervielfältigen, damit neue Viren entstehen.

Mit freundlicher Genehmigung
von EMBL Photolab
Für das Virus sind all diese Prozesse mit Gefahren verbunden. Säugerzellen, also auch menschliche Zellen, besitzen Verteidigungssysteme, die fremde RNA angreifen und zerstören. Deshalb versteckt das Virus sein verwundbares Genom, indem es es fest in eine aus so genannten Nukleoproteinen aufgebaute Hülle verpackt, welche als Nukleokapsid bezeichnet wird. Dadurch wird es geschützt bis es die Möglichkeit hat, in eine Zelle einzudringen, wo es die zelluläre Maschinerie des Wirts unter seine Kontrolle bringt, um sich zu replizieren und virale Proteine zu produzieren. Neben dem Schutz des Genoms übernehmen Nukleoproteine auch die Funktion, die Balance zwischen der Produktion von Proteinen, die für die virale Replikation nötig sind, und der Replikation selbst zu kontrollieren, denn es kann nicht beides gleichzeitig stattfinden. Auf diese Weise spielt das Nukleokapsid eine Schlüsselrolle im „Lebenszyklus“ eines Virus.
Bisher kamen die einzigen Erkenntnisse der Forscher über die Funktionsweise von Nukleoproteinen jedoch von verschwommenen elektronenmikroskopischen Bildern, die zeigten wie die Nukleoproteinmoleküle auf dem Genom polymerisieren, um die Nukleokapside zu bilden, aber sie gaben wenig Aufschluss über die Struktur des Proteins selbst. Um mehr darüber herauszufinden, gab es eine Zusammenarbeit zwischen Rob Ruigrok vom UVHCI und Winfried Weissenhorn zur Herstellung von Nukleoproteinkristallen und der Bestimmung ihrer Struktur durch Bestrahlung mit hoch energetischen Röntgenstrahlen, die an der European Synchroton Radiation Facility, auch in Grenoble – verfügbar waren. Kristalle sind symmetrische Strukturen und produzieren bei Röntgenbestrahlung ein hochgeordnetes Beugungsmuster, von dem die Forscher die exakte Form eines Moleküls ableiten können. Über die Bestimmung der Nukleoproteinstruktur würden die Forschern dazu in der Lage sein, die Medikamente zu entwickeln, welche das virale Genom in ihrer schützenden Hülle gefangen halten.
Das Projekt begann in Robs Labor, wo sein Team seit Mitte der 1990er Jahre an Nukleoproteinen einer ganzen Reihe von „negativ Strang RNA Viren“ arbeiteten. Das Tollwutvirus war nur zufällig jenes, welches sich als das am einfachsten zu manipulierende erwies. Aurélie Albertini, eine Doktorandin im Labor, hatte es geschafft, Gewebekulturen aus Insektenzellen zu etablieren, um das Nukleoprotein des Tollwutvirus zu produzieren. Das Protein wickelte sich um die RNA Moleküle der Wirtszelle, indem es Ringe aus 9 – 13 Proteinmolekülen bildete. Rob Ruigroks Gruppe hatte schon früher festgestellt, dass diese sich wie Miniaturnukleokapside verhielten, und ein elektronenmikroskopischer Einblick in ihre Struktur offenbarte, dass sie dem Tollwutnukleokapsid tatsächlich sehr ähnlich sind und daher dazu genutzt werden könnten, die Struktur von Nukleoproteinen, die um RNA gewickelt sind, zu untersuchen.
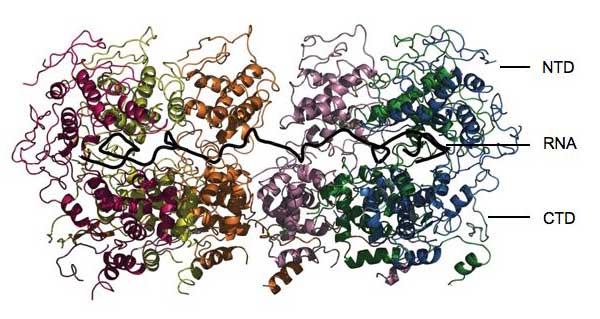
Mit freundlicher Genehmigung von Winfried Weissenhorn
Aurélie begann ihre Arbeit damit, Nukleoprotein-RNA Kristalle herzustellen, ein Projekt, zu dem später Amy Wernimont hinzustieß, eine Postdoc aus Winfrieds Labor. Aber die Moleküle spielten nicht mit und sowohl Aurelie als auch Amy mühten sich eine lange Zeit ab, die Kristalle zu erhalten, die es Amy erlauben würden, die Struktur mit ein Auflösung von 4 Ångström zu bestimmen, was scharf genug ist, um verschiedene Proteinfaltungen zu unterscheiden, aber nicht ganz ausreichend, um die Sequenz der Aminosäuren, der individuellen Grundbausteine des Proteins, zu zeigen. Ein Problem war, dass die Zellen, mit denen sie arbeitete, nur winzige Menge des Nukleoproteins produzierten.
Glücklicherweise war die Hochdurchsatzkristallisationseinrichtung von Josan Márquez verfügbar, um das Problem zu lösen, indem nur kleine Proteinproben verwendet wurden. „Die Kristallisierungsroboter sind einfach wunderbar,“ erinnert sich Winfried. „Hätten wir große Proben benötigt, wären wir niemals dazu in der Lage gewesen, nach den richtigen Kristallisierungsbedingungen zu suchen.“ Das Team fand letztendlich die richtigen Bedingungen, die genaue Proteinkonzentration und eine komplexe Mischung von Reagenzien, die für die Kristallisation nötig sind, und schafften es, eine Auflösung von 3.5 Ångström herauszukitzeln – genug um ein detailliertes Modell der Proteinstruktur zu konstruieren. Beistand gab es auch von Raimond Ravelli, der bei der Datenerfassung und der Feineinstellung der Röntgenbelichtungszeit für die besten Ergebnisse half und der kontinuierlich Ratschläge in den verschiedenen Etappen der Strukturanalyse gab.
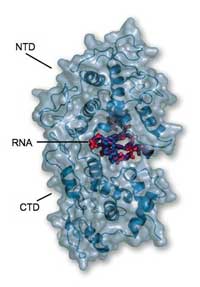
offenbart, dass die RNA vollständig
zwischen NTD (oben) und CTD
(unten) eingeklemmt ist und daher
für angreifende Wirtsenzyme oder
Polymerasen nicht zugänglich ist
Mit freundlicher Genehmigung von
Winfried Weissenhorn
Die Ergebnisse offenbarten, dass das Nukleoprotein sich vollständig um die RNA herum klammert und sie sozusagen wie die Familienjuwelen im Tresor einschließt. „Sie ist für kein anderes Enzym zugänglich, um sie zu attackieren,“ sagt Winfried. Das Protein besteht aus zwei Hauptfunktionseinheiten, auch Domänen genannt. Eine davon, die CTD, umschlingt eine Seite der RNA und klebt auch an den CTDs von anderen Nukleoproteinmolekülen, was die Ausbildung eines helixförmigen Kokons fördert. Die andere Domäne, die NTD, sitzt auf der anderen Seite der RNA und stellt keinen weitreichenden Kontakt zu anderen Nukleoproteinen her. Die Gesamtstruktur ist wie eine Klammer, die um die RNA herumgreift und alles andere fernhält. „Das Nukleoprotein verhindert, dass die RNA vom angeborenen Immunsystem erkannt wird,“ sagt Winfried. „Aber wie wird sie zugänglich für Replikation und Translation?“
Die Antwort liegt in den zwei fadenähnlichen Strukturen, die aus jeder Domäne herausragen. Diese könnten als Scharnier dienen und die NTD Region nach oben schwingen lassen, wodurch die Nukleoproteinklammer geöffnet würde und viralen Proteinen Zugang zu kleinen Teilen des Genoms gestattet würde. Ein bestimmtes Protein, welches Phosphoprotein P genannt wird, könnte beteiligt sein. Dieses verknüpft die RNA Polymerase -das Enzym, welches für die Vervielfältigung des Genoms benötigt wird- mit dem Nukleoprotein und könnte an eines der Scharniere binden um die NTD aus dem Weg schwingen zu lassen.
Dieser Scharniermechanismus legt den Einsatz von Medikamenten nahe, die diesen behindern, um mit Viren wie dem Tollwutvirus fertig zu werden. „Sollte unser Konzept, welches sich auftut, das richtige sein, könnte man es in geschlossener Form festhalten,“ meint Winfried. „Dies würde die virale Replikation blockieren.“ In seiner Schutzhülle eingeschlossen, wäre das Virus machtlos und würde letztlich von der Zelle entsorgt werden. Der nächste Schritt in Richtung solcher Medikamente wäre die systematische Suche nach kleinen chemischen Verbindungen mit der Fähigkeit, an das Scharnier zu binden und damit das Öffnen des Nukleokapsids zu verhindern.
„Diese Befunde könnten auch Aufschluss darüber geben, wie „negativ Strang RNA Viren“ evolviert sind,“ sagt Winfried. Verwandte Virusarten können sehr unterschiedliche Genomsequenzen haben, was es schwierig macht, Schlussfolgerungen über den evolutionären Werdegang nur über den Vergleich der Sequenzen zu machen. Strukturen jedoch sind eine andere Sache. Die gleiche physische Struktur kann aus einer Vielfalt an verschiedenen Gen- oder Aminosäuresequenzen konstruiert werden. Auch wenn Gene evolvieren und sich dramatisch verändern, können die von ihnen kodierten Strukturen tiefe evolutionäre Brücken zwischen Viren offenbaren.
Elektronenmikroskopische Bilder von RNA Molekülen anderer „negativ Strang RNA Viren“ wie des Masernvirus und des Marburgvirus sowie ein Kristallstruktur eines Bornavirus lassen vermuten, dass ihre Nukleoproteine eine ähnliche Klammerstruktur mit Scharnier aufweisen. Das legt nahe, dass diese Viren eine ähnliche Taktik wie das Tollwutvirus anwenden, um ihre RNA zu schützen, und könnten daher auch durch Medikamente anvisiert werden, die sie in ihren Kokons einschließt. „Man kann überdies vermuten, dass alle einen gemeinsamen Vorfahren haben,“ meint Winfried. „Über die Sequenzanalyse würde man niemals denken, dass sie verwandt sind,“ fügt er hinzu. „Ich glaube, es gab einmal ein Urnukleokapsid, doch dann liefen sie auseinander als die Viren evolvierten, um unterschiedliche Zelltypen zu infizieren.“
Resources
- Die Arbeit, die in diesem Artikel beschrieben wird, wurde publiziert als:Albertini AA, Wernimont AK, Muziol T, Ravelli RB, Clapier CR, Schoehn G, Weissenhorn W, Ruigrok RW (2006) Crystal structure of the rabies virus nucleoprotein-RNA complex. Science 313: 360-363.
- Um mehr über die Arbeit von Winfried Weissenhorn und Rob Ruigrok herauszufinden, besuchen Sie: www2.ujf-grenoble.fr/pharmacie/laboratoires/gdrviro/
Institutions
Review
Dieser Artikel illustriert die wissenschaftliche Forschung als eine fortlaufende, dynamische Gesamtheit. Sobald ein molekulares Geheimnis des Lebenszyklus von sogar dem einfachsten Organismus durch die Anwendung von ausgeklügelten Technologien aufgedeckt wird, gibt es Rückwirkungen auf den Fortschritt der medizinischen Behandlungsmethoden und der Kontrolle von Krankheiten.
Marie Walsh, Republik Irland





