Kafesi Kilitleme Understand article
Fransa, Grenoble’daki Avrupa Moleküler Biyoloji Laboratuvarından (EMBL) Winfried Weissenhorn’un grubu bir dizi tehlikeli virus ile başetmek için muhtemel bir yol buldu; onları kozalarının içerisine hapsetmek. Claire Ainsworth araştırıyor.
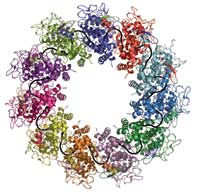
kompleks oluşturmak üzere bir
RNA molekülüne (siyah)bağlanır
Resim Winfried Weissenhorn izniyle
Bu muhtemelen dünyada en çok korkulan hastalıklardan birisidir. Klasik belirtiler olan salya akması, su korkusu ve felcin bir kez ortaya çıktığı her vakada bunlar hemen hemen herzaman ölümün habercisidir. Sadece beş insan kuduz başlangıcı sonrası hayatta kalmış ve birisi dışında hepsi kalıcı sinirsel hasara uğramıştır Avrupa ve Kuzey Amerika’da aşı ve hastalığa yakalanma sonrası önleyici tedavilerin hastalığın etkisini çarpıcı bir şekilde azaltmasına rağmen bu hastalığa karşı hala bir çare yoktur. Kuduz gelişmekte olan birçok ülkede her yıl 70 000 insanın ölümüne yol açan ciddi bir tehdit olmaya devam etmektedir.
Endişelendirici bir şekilde kuduz ve benzer virüsler şu an gelişmiş ülkelerde tekrardan ortaya çıkabilmekte, yarasalarla temas ile insanlara bulaşabilmektedir. Bu yüzden Winfried Weissenhorn, Rob Ruigrok ve onların uzun yol arkadaşları tarafından virüslere saldırı için yapılan keşif tamda zamanındadır. Fransa, Grenoble’daki Moleküler Biyoloji Laboratuvarından ve yakınındaki Virüs Ev Sahibi Hücre Etkileşimleri Biriminden (UVHCI) takımlar virüsün genetik maddesini saran ve kendi kendini kopyalama fırsatı buluncaya kadar onu vücudun bağışıklık sisteminden saklayan proteinin yapısını ortaya çıkardılar. Genomları bu koruyucu kafeslerin içerisine kilitlemek ve böylece virüsün kendini kopya ederek çoğalmasını önlemek için ilaçları kullanmak mümkün olabilir.
Fakat çalışma kuduz hastalığının alanı ötesinde uzantılara sahiptir. Bu araştırma Ebola, Borna hastalıkları ve kızamık virüslerini de içeren birçok virüsün genomlarını korumak için buna benzer kozalara sahip olduklarını ortaya çıkarmıştır. Bunun anlamı bu buluşun, bu gibi virüslerin nereden geldikleri ve nasıl geliştikleri üzerine de ışık tutabilecek olmasıdır. Birçok diğer virüsler gibi kuduz virüsü genomunu, genlerimizi taşıyan DNAya benzer bir molekül olan RNAnın tek sarmalı dışında oluşturur. Ama DNAnın aksine virüslerin RNAları tarafından şifrelenen bilgiler virus oluşturmak için gerekli proteinleri üretmek için doğrudan kullanılamazlar. Bunun yerine ihtiyaç duyulan şey bir tür kimyasal fotografik negatif olan bir dizi tamamlayıcı kopyadır. Böylece virus genomunu koruyacak kabuğu oluşturan proteinleri yapmadan önce bu negatif RNA sarmalını proteine dönüştürülebilen pozitiflerine dönüştürmek zorundadır. Ayrıca daha fazla virüse dönüştürmek için genomunun daha fazla kopyasına ihtiyacı vardır.

Resim EMBL Photolab izniyle
Virüsler için bu süreçler tehlikelerle doludur. İnsan hücrelerinin de dahil olduğu memeli hücreleri yabancı RNAlara saldıran ve onları yok eden savunma sistemlerine sahiptirler. Bu nedenle virus hassas genomunu nükleprotein denilen bir proteinden yapılmış bir kabuk olan nükleokapsül içerisine sıkıca paketleyerek saklar ve kendi kendini kopyalamak ve virüs proteinleri üretmek için hücresel mekanizmasını gasp edeceği ev sahibi hücre içerisine girinceye kadar onu korur. Nükleoprotein genomu korumak kadar viral kopyalama için gerekli protein üretimi ile kopyalama işleminin kendisi arasındaki dengeyi kontrol etmeye de yardım eder. Çünkü ikisi eş zamanlı olarak gerçekleşemez. Bu bağlamda nükleokapsül virüsün hayat hikayesinde bir anahtar rolü oynar.
Bununla birlikte şu ana kadar bilim adamları nükleoproteinlerin nasıl çalıştıkları hakkındaki tek ipuçlarını fuzzy electron mikroskobu görüntülerinden elde etmişlerdir ki bunlar nükleoprotein moleküllerinin nükleokapsül oluşturmak üzere genom üzerine nasıl polimerleştiklerini göstermişlerdir. Fakat proteinin kendi yapısı hakkında çok az şey açığa çıkarmışlardır. Daha fazlasını bulmak için UVHCI da Rob Ruigrok ve Winfried Weissenhorn nükleoprotein kristalleri yapmak ve yapılarını yüksek hassasiyetli X-ışını demetleri kullanarak belirlemek için birlikte çalışmışlardır. X-ışını demetleri Grenoble’daki Avrupa Parçacık Hızlandırıcı Radyasyon Tesisi’nde mevcuttur. Kristaller simetrik yapılardır ve X-ışını demetlerine maruz bırakıldıklarında bilim adamlarının moleküllerin kesin şeklini anlayabildikleri yüksek düzenlilikte kırınım çifti üretirler. Araştırmacılar nükleoproteinin yapısını belirleyerek viral genomları virüsün koruyucu kabuğuna kilitleyebilecekleri ilaçların tasarımına başlayabileceklerdir.
Proje Rob’un laboratuvarında başlamıştır. Burada Rob’un takımı 1990 ortalarından bu yana bir dizi negatif sarmal RNA virüslerinin nükleoproteinleri üzerinde çalışmaktadır. Kuduz virüsü üretilebilecek en kolay virüslerden birisi olarak ortaya çıkmıştır. Laboratuvardaki PhD öğrencisi Aurélie Albertini kuduz nükleoproteini üretmek için doku kültüründe böcek hücreleri elde etmeyi başarmıştır. Protein kendini 9-13 protein molekülünden oluşan halkalar oluşturmak üzere ev sahibi hücrelerin RNA molekülleri etrafına sarmıştır. Rob Ruigrok’un grubu daha önce bunların minyatür nükleokapsüller olarak davrandıklarını düşünmüşlerdir ve elektron mikroskopisi çalışmaları bunların kuduz nükleoplazmitlerine benzediklerini ve böylece RNA çevresinde düzenlenmiş nükleoproteinlerin yapısını irdelemek için kullanılabileceklerini ortaya çıkaran yapılarına ilişkin kaba taslak fikirler sağlamıştır.
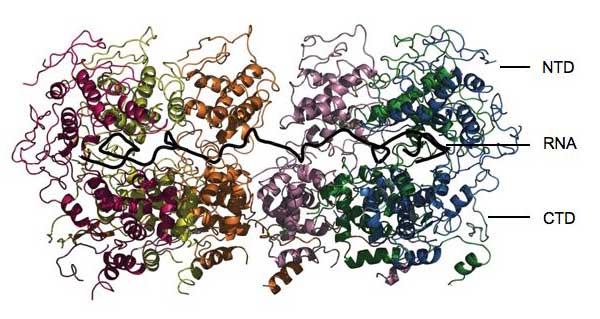
Resim Winfried Weissenhorn izniyle
Aurélie, Winfried’in laboratuvarında doktora sonrası araştırmacı olan Amy Wernimont’un da daha sonra katıldığı nükleoprotein-RNA kristalleri üretimi üzerinde çalışmaya başladı. Ancak moleküller işbirliği yapmıyorlardı ve Aurélie ve Amy’nin ikisi de 4 Ångstrom çözünürlükteki yapıları belirlemesi için Amy’e olanak sağlayan kristaller elde etmek için uzun bir süre uğraştılar. Bu 4 Ångstrom değeri proteinin nasıl katlandığını, düzenlendiğini ayırdetmek için yeterince keskin ancak proteinin özel yapı taşları olan amino asitlerin sırasını göstermek için yeterli değildir. Tek problem Amy’nin çalıştığı hücrelerin çok küçük miktarlarda nükleoprotein üretmesiydi.
Şans eseri Josan Márquez’in sadece küçük protein örneklerini kullanan yüksek verimli kristalleştirme kolaylığı imdada yetişti. “Kristallendirme robotikleri kesinlikle harikaydı” diyor Winfried. “Eğer daha büyük miktarlarda örneklere ihtiyaç duymuş olsaydık doğru kristallendirme koşularını belirleyemeyebilirdik.” Takım, sonunda doğru koşulları buldu; kristallendirme işlemi için gerekli protein derişimi, kimyasalların karışımı ve onları protein yapısının detaylı bir modelini oluşturmaya yetecek 3.5 Ångstrom çözünürlük kazanmak için bükmede başarılı olmak. Veri toplama ve en iyi sonucu almak için X-ışınına maruz bırakma zamanını ayarlamada yardımcı olan ve protein yapısı araştırmalarının farklı aşamalarında sürekli tavsiyeler veren Raimond Ravelli’den de yardımlar geldi.
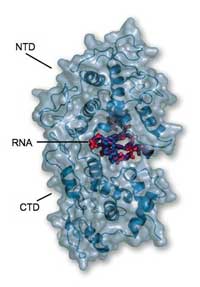
nın NTD(üst) ve CTD(alt)
yüzeylerinde tamamıyla
tutturulduğunu ve böylece ev
sahibi enzimleri ve polimerazları
parçalamaya elverişli olmadığını
ortaya koymaktadır
Resim Winfried Weissenhorn izniyle
Sonuçlar nükleoproteinin kendini tamamen RNA etrafına kenetlediğini ve onu banka kasasındaki aile mücevherleri gibi kilit altında tuttuğunu ortaya çıkarmıştır. “Başka bir enzimin ona saldırması olası değildir.” diyor Winfried. Protein iki ana çalışma parçasından oluşmaktadır. CTD olarak adlandırılan ilki RNAnın bir tarafını sarar ve ayrıca diğer nükleoprotein moleküllerinin CTDlerine sarmal bir kafes oluşumuna yardım edecek şekilde saplanır. NTD olarak adlandırılan diğeri RNAnın diğer tarafında bulunur ve diğer nükleoproteinlerle geniş çaplı bir temas oluşturmaz. Genel yapı RNAyı sıkıştıran ve diğer herşeyi dışarıda tutan bir kelepçeye benzer. “Nükleoprotein RNAnın kalıtsal bağışıklık sistemi tarafından tanınmasını önleyecektir.” diyor Winfried. “Fakat RNA kendini kopyalamaya(replication) ve dönüşüme(translation) açık hale nasıl gelir?”
Cevap her iki yapıdan çıkan sarmal iplik benzeri yapıların içinde saklıdır. Bunlar NTD bölgesini yukarı sallayan ve nükleoprotein kelepçesini açacak şekilde büken ve viral enzimlerin genomun küçük bölmelerine girişine izin veren menteşeler gibi davranabilirler. Fosoprotein P denilen özel bir protein ilişkili olabilir. Bu, genomu kopyalamak için gerekli enzim olan RNA polimerazı nükleoproteine bağlar ve NTD yi dışarı sallamak için menteşelerin birisine bağlanabilir.
Bu menteşe mekanizması kuduz virüsü gibi virüslerle onlara müdahale edici ilaçlar kullanarak başa çıkmak için bir yol önerir. “Eğer düşüncemiz doğru ise onu sıkıştırabiliriz.” diyor Winfried. “Bu, virüssel kopalamayı engeller.” Virüs genomları protein kafesinin içerisine kapatılarak güçsüz bırakılabilir ve sonunda hücre tarafından uzaklaştırılabilirler. Bu gibi ilaçlar konusunda bir sonraki adım menteşe bölgesine bağlanabilecek ve böylece nükleoproteinin açılışını engelleyebilecek küçük kimyasallar için sistematik araştırmalar olacaktır.
“Bulgular ayrıca negatif sarmal RNAlı virüslerin nasıl geliştiklerine dair fikir verebilir.” diyor Winfried. İlgili virus türleri tek başına seri kıyaslamasından evrimleşme tarihçesi hakkında herhangi bir sonuç çıkarmayı zorlaştıran çok farklı genom dizilerine sahip olabilirler. Diğer taraftan yapılar farklı bir hikayedir. Aynı fiziksel yapı bir çeşit gen ve amino asit serisinden inşa edilebilir. Böylece genler şaşırtıcı bir şekilde gelişip değişse bile şifreledikleri yapılar virüsler arasında derin evrimsel bağlantılar ortaya çıkarabilir.
Kızamık virüsü, Marburg virüsü ve Borna virüsünün kristal yapısı gibi diğer negatif sarmal RNA virüslerinin elektron mikroskopi RNA resimleri bunların nükleoproteinlerinin benzer menteşe tutunma yapılarının olduğunu önerir. Bu, bu virüslerin RNAlarını korumak için kuduz virüsününkine benzer bir yöntem kullandıklarını önerir ve böylece kafeslerine sıkıştırarak kapatabilen ilaçlara hedef olabilirler. “Ayrıca bunların ortak bir atayı paylaştıklarını da ileri sürebilir.” diyor Winfried. “Seri analizlerden akraba olduklarını düşünemezsiniz” diye ekliyor. “Bence muhtemel bazı atasal nükleokapsüller vardı. Fakat bunlar virüslerin farklı hücre türlerine bulaşmak için gelişmelerinden dolayı farklılaştılar.”
Resources
- Bu yazıda tanımlanan çalışma şöyle yayımlanmıştır:Albertini AA, Wernimont AK, Muziol T, Ravelli RB, Clapier CR, Schoehn G, Weissenhorn W, Ruigrok RW (2006) Crystal structure of the rabies virus nucleoprotein-RNA complex. Science 313: 360-363.
- Winfried Weissenhorn ve Rob Ruigrok’un çalışması hakkında daha fazla bilgi edinmek için bakınız: www2.ujf-grenoble.fr/pharmacie/laboratoires/gdrviro/
Institutions
Review
Bu yazı devam eden, dinamik bir varlık olarak bilimsel araştırmanın doğasını tanımlar. En basit organizmalar da dahil olmak üzere yaşam döngüsünün her moleküler sırrı karmaşık teknolojiler kullanılarak açığa çıkarıldığından dolayı ortamda tıbbi tedavi ve hastalık kontrollerindeki gelişmeler için yankılar bulunmaktadır.
Marie Walsh, İrlanda Cumhuriyeti





