Supporting materials
Download
Download this article as a PDF

Vertė Urtė Neniškytė. Pramoninė veikla ir netgi geologiniai pokyčiai gali paveikti vandens kokybę, sukeldami taršą, kuri kelia grėsmę žmonių sveikatai ir aplinkai. Sužinok, kaip tapti nepriklausomu tyrėju, užtikrinančiu gerą mūsų vandens kokybę.

Pramoninė veikla ir netgi geologiniai pokyčiai gali būti labai žalingi vandens kokybei, užteršdami jį trąšomis, pesticidais, metalų jonais ar organiniais junginiais, kurie kelia grėsmę žmonių sveikatai ir aplinkai. Todėl yra būtina nuolat stebėti gėlo vandens šaltinių, tokių kaip upės, kokybę.
Apsaugant mus nuo vandens taršos pagrindinį vaidmenį atlieka kokybės tyrėjai. Jie reguliariai tikrina vandens kokybę, kiekybiškai tirdami (pavyzdžiui, nustatydami jonų kiekį tirpale) bandinius, kurie buvo surinkti įvairiose vietose prieš, per ir po vandens valymo.
Šioje užduotyje mokiniai įsivaizduos esą vandens kokybės tyrėjai, dirbantys šalia įmonės, panašios į Tata Steel plieno gamyklą, esančią Scunthorpe, JK. Jie turės reaguoti į konkrečią situaciją, atlikti tinkamus tyrimus ir nustatyti, ar gamykla efektyviai pašalina tiocianatą iš savo nutekamųjų vandenų.

Tiocianato jonai (SCN–) yra nuodingi vandens organizmams ir sukelia skydliaukės pažeidimus žmonėms, sumažindami šios liaukos gebėjimą išskirti hormonus, reikalingus normaliai organizmo funkcijai.
Tiocianatai į aplinką patenka iš įvairių šaltinių. Pavyzdžiui, anglis verčiant dujomis ir iš anglių išgaunant pramonėje naudingus cheminius junginius, susidaro dideli kiekiai tiocianato jonų kartu su daug įvairių kitų nuodingų junginių, tokių kaip fenoliai ar amoniakas. Šie šalutiniai produktai patenka į gamyklos nutekamuosius vandenis.
Tiocianatų taip pat susidaro ten, kur išgaunant tauriuosius metalus naudojamas cianidas. Cianidas virsta tiocianatu reaguodamas su siera, kurios yra gamtinėse rūdose:
8 CN– + S8 → 8 SCN–
Kai kuriuose pesticiduose tiocianato jonai yra jų aktyvusis, nuodingas, komponentas. Tiocianatų pėdsakai natūraliai nustatomi žmogaus organizme kaip šalutinis cisteino metabolizmo ir cianido detoksikacijos produktas – jie galiausiai pašalinami su šlapimu. Tiocianatai gali patekti į žmogaus kūną rūkant arba kaip šalutinis kai kurių vaistų nuo hipertenzijos metabolizmo produktas.
Tiocianatai iš nutekamųjų vandenų šalinami milžiniškuose atviruose betoniniuose rezervuaruose su aktyviu dumblu – biologiškai aktyvia medžiaga, sudaryta iš įvairių mikroorganizmų, galinčių suskaidyti tiocianato jonus ir kitus teršalus į mažiau pavojingus junginius. Cheminė reakcija, vykstanti neutralizuojant tiocianatus, yra tokia:
SCN– + 3H2O + 2O2 → HCO3– + NH4+ SO42- + H+
Ši reakcija yra bioremediacijosw1 pavyzdys. Tai procesas, kurio metu mikrobai naudojami išvalyti užterštai dirvai ir požeminiams vandenims. Augalai taip pat gali būti naudojami užterštai žemei valyti; šis procesas vadinamas fitoremediacijaw2.
Prieš ir po valymo lengva patikrinti, ar nutekamuosiuose vandenyse yra tiocianato jonų. Jeigu įdėjus geležies (III) chlorido tirpalas paraudonuoja, tai reiškia, kad jame buvo tiocianato jonų ir vyko ši reakcija:

Fe3+(aq) + SCN–(aq) → [FeSCN]2+(aq)
arba tiksliau:
[Fe(H2O)6]3+(aq) + SCN–(aq) →
[Fe(H2O)5SCN]2+(aq) + H2O(l)
Ši reakcija gali būti naudojama kiekybiškai nustatyti nedidelėms tiocianato jonų koncentracijoms. Naudodami kolorimetrą, galite išmatuoti [Fe(H2O)5SCN]2+ komplekso sugertį ties 480 nm ir apskaičiuoti tikslią tiocianato jonų koncentraciją, jei tik ji nėra per didelė. Taip pat galite naudoti paprastą spalvų palyginimą, tačiau tuomet rezultatai bus ne tokie tikslūs ir tik kokybiniai.
Kaip paaiškinta 1 darbalapyjew3, mokiniai turėtų įsivaizduoti esantys kokybės tyrėjai iš mažos nepriklausomos kokybės kontrolės tarnybos, kuri tikrina rezultatus, kad užtikrintų, jog jie atitinka JK Aplinkosaugos agentūros reikalavimus.

Žinoma, kad nuotekose iš pramonės įmonių, tokių kaip Tata Steel gamykla Scunthorpe, yra apie 250 mg/dm3 (250 ppm) tiocianato jonų. Tačiau saugi jonų koncentracija, nustatyta JK Aplinkosaugos agentūros, yra 10 mg/dm3, todėl nuotekos yra valomos ir tiocianato koncentracija yra sumažinama iki 1 mg/dm3 koncentracijos, gerokai žemesnės nei saugi riba. Tiocianato jonai iš nuotekų pašalinami prieš jas išleidžiant į Trento upę.
Pastaruoju metu laikėsi itin šalti orai, kurie galėjo paveikti mikroorganizmų aktyvumą. Įmonė yra susirūpinusi, kad tai galėjo pakenkti nuotekų valymo įrenginiams ir galėjo sumažinti jų veiksmingumą iš nuotekų šalinant tiocianato jonus.
Paprastai gamykoje tiocianato koncentracija vandenyje tiriama tris kartus per dieną, naudojant paprastą bandymą: į vandens bandinį įdedama rūgštinio geležies (III) chlorido ir tiocianato koncentracija nustatoma fotometriškai išmatavus geležies (III) tiocianato komplekso sugertį. Kiekvieną savaitę atliekama 16 nepriklausomų bandymų. Tiksliems tyrimams taip pat paimami atitekančių nuotekų ir išleisti į upę paruošto vandens bandiniai.
Įmonės tyrėjas ištyrė bandinius, tačiau įmonė kreipiasi į nepriklausomą tyrėją – tave!
Dirbdami su rūgštimis ir tiocianatais, turėtumėte dėvėti tinkamas akių ir rankų apsaugos priemones. Saugos gaires rasite Science in School svetainėje ir šio leidinio pabaigoje.
Ši užduotis skirta 16–18 metų mokiniams ir užtrunka apie 2 valandas.

1. Iš anksto paruoškite šiuos tirpalus:
a– Kalio tiocianato (KSCN) tirpalas, 250 mg/dm3 (250 ppm). Ištirpinkite 4,5 g kalio tiocianato 500 cm3 distiliuoto vandens. Tuomet atskieskite 50 cm3 šio tirpalo iki 1 dm3 – gauto tirpalo tiocianato jonų koncentracija yra 250 mg/dm3.
b– Rūgštinis geležies (III) chlorido (FeCl3(H2O)6) tirpalas, 0,41 mol/dm3. Ištirpinkite 50 g FeCl3(H5O)6 maždaug 250 cm3 1 mol/dm3 koncentracijos druskos rūgšties (HCl) tirpalo.
c– Dvylika pažymėtų bandinių su skirtingomis tiocianato jonų koncentracijomis:
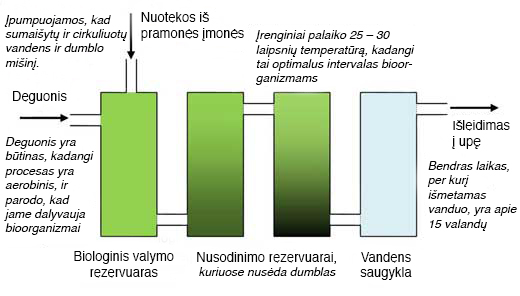
2. Mokiniams pateikite gamyklos planą (1 paveikslas), 1 darbalapįw3, aprašantį situaciją, ir 2 darbalapįw4, kuriame tiksliai aprašyta visa bandymo eiga.
3. Mokiniai turėtų parašyti laišką įmonei, valdančiai vandens valymo įrenginius, ir paprašyti bandinių tyrimams. Jie turėtų nurodyti, kuriuose valymo etapuose turėtų būti paimti nuotekų bandiniai, kiek bandinių jiems reikia ir kada jie turėtų būti paimti. Jie taip pat turėtų nurodyti, kokio kiekvieno bandinio tūrio jiems reikia, kaip bandiniai turėtų būti paimti ir į kokią tarą jie turėtų būti surinkti.
4. Mokiniai, dirbdami poromis, turėtų ištirti savo bandinius pagal 2 darbalapyjew4 aprašytą metodiką.

Atsargiai: dėvėkite akių apsaugą. Geležies (III) chlorido tirpalas yra dirginantis.
1. Sudarykite kalibravimo kreivę
a. Užpildykite tris biuretes: vieną kalio tiocianato tirpalu, kuriame yra 250 ppm tiocianato jonų, vieną distiliuotu vandeniu ir vieną geležies (III) chlorido tirpalu.
b. Į šešias 100 cm3 matavimo kolbas įpilkite 0,0, 2,0, 4,0, 6,0, 8,0 ir 10,0 cm3 250 mg/dm3 kalio tiocianato tirpalo ir sužymėkite jas nuo A iki F.
c. Į kiekvieną kolbą įpilkite tiek distiliuoto vandens, kad bendras tirpalo tūris būtų apie 80 cm3.
d. Į kiekvieną kolbą įpilkite po 10 cm3 geležies (III) chlorido tirpalo ir tuomet pripilkite distiliuoto vandens iki 100 cm3 tūrio. Kruopščiai sumaišykite tirpalus.
|
Kolba |
a |
b |
c |
d |
e |
f |
|---|---|---|---|---|---|---|
|
Kalio tiocianato tirpalo tūris (cm3) |
0,0 |
2,0 |
4,0 |
6,0 |
8,0 |
10 |
|
Tiocianato koncentracija (ppm) |
0 |
5 |
10 |
15 |
20 |
25 |
e. Kolorimetru išmatuokite kiekvieno tirpalo sugertį.
f. Sudarykite kalibravimo kreivę, grafike atidėdami visų šešių tirpalų sugerties (y ašis) priklausomybę nuo tiocianato jonų ppm koncentracijos (x ašis).
2. Ištirkite bandinį
a. Į 100 cm3 matavimo kolbą įpilkite 10 cm3 nežinomos koncentracijos tiocianato tirpalo ir pripilkite tiek distiliuoto vandens, kad bendras tūris būtų apie 80 cm3.
b. Į kolbą įpilkite 10 cm3 geležies (III) chlorido tirpalo ir tuomet pripilkite distiliuoto vandens iki 100 cm3 tūrio. Kruopščiai sumaišykite tirpalą.
c. Kolorimetru išmatuokite tirpalo sugertį.
d. Naudodami kalibravimo kreivę, nustatykite koncentraciją.
3. Parašykite ataskaitą vandens valymo įrenginių įmonei, apibendrindami savo išvadas ir pateikdami rekomendacijas, ar nuotekos gali būti išleidžiamos į upę, ar ne. Mokiniai turėtų aprašyti duomenis, kuriais jie grindžia savo rekomendacijas, ir pakomentuoti savo duomenų patikimumą, turėdami omenyje galimas procentines paklaidas, kurios galėjo atsirasti tyrimo metu.
Buvo parodyta, kad laboratoriniai darbai yra labai vertingi susiejant teorines idėjas su „tikrų“ tiriamųjų darbų situacijomis arba gyvenimišku kontekstu. Ši praktinė užduotis yra geras pavyzdys, kaip klasikinė analitinė chemija susiejama su gyvenimišku kontekstu. Ji taip pat suteikia galimybę vystyti bendrąsias duomenų apdorojimo ir bendravimo kompetencijas.
Marie Walsh, Limerick technologijų insitutas (Limerick Institute of Technology), Airija
Download this article as a PDF