Biologiniai kristalai: sandūroje tarp fizikos, chemijos ir biologijos Understand article
Išvertė Kauno regioninio inovacijų centro užsakymu. Dominique Cornuéjols iš Europos sinchrotrono radiacijos infrastruktūros pristato mums kristalografijos pasaulį. Ne viskas yra spindintys deimantai…

BlackJack3D/iStockphoto
Galvojant apie biologiją, pirmiausia į galvą tikrai neateina mintys apie „kristalus“. Kristalai geriau žinomi kaip puikūs mineralų pasaulio atstovai. Nuo neatmenamų laikų mus žavėjo brangakmeniai – spindinčios požeminio pasaulio žvaigždės, o žymiausias brangakmenis deimantas tapo tvirtumo ir amžinybės simboliu.
Priešingai, dauguma biologinių audinių yra minkšti, ir, visi žino, kad jie nėra amžini. Tačiau gyvas molekules (pvz. proteinus) įmanoma izoliuoti ir iš jų laboratorijoje išauginti kristalus. Tokių dirbtinai užaugintų biokristalų tyrimai veda link visiškai atskiros disciplinos, žinomos makromolekulinės kristalografijos vardu.
Kristalai ir struktūra
Moksliniai mineralinių kristalų tyrimai (kristalografija) buvo pradėti XVII a. pabaigoje. Iš pradžių jais siekta aprašyti ir išmatuoti skirtingų kristalinių struktūrų paviršių ir kampus bei suklasifikuoti jas pagal jų geometrines savybes. Greitai kristalografai nustatė, kad tiksli geometrija, pastebima makroskopiniu lygiu, gali būti paaiškinama taisyklingu labai mažų plika akimi (ir net per mikroskopą) nematomų dalelių (atomų, molekulių arba jonų) išdėstymu. Dar tik prasidėjus atomistinei teorijai, šis modelis buvo plačiai aptarinėjamas XVIII ir XIX amžiuje, nors taip ir neprieita prie galutinių išvadų.
Fizikos srityje įvyko keletas esminių lūžių, sukėlusių revoliuciją šioje srityje:
- 1895 m. V. C. Rentgenas atrado rentgeno spindulius. Šie spinduliai pasižymi neįprastu sugebėjimu prasiskverbti pro daiktus ir kūnus, taip atskleisdami jų vidines savybes. Rentgeno spinduliai nedelsiant buvo panaudoti medicinai, tačiau jų prigimtis (kaip elektromagnetinės bangos) išliko mįsle dar 17 metų.
-
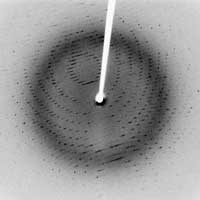
Rentgeno spindulių difrakcijos
modelis kristalizuotoje 3Clpro
SŪRS(sunkus ūminis respiracinis
sindromas – vert.pastaba) proteazėje
Paveikslėlio autorinės teisės priklauso J
eff Dahl; image source: Wikimedia
Commons1912 m. Laue atrado rentgeno spindulių difrakciją, kai jam kilo puiki mintis į rentgeno spindulių pluoštą įdėti kristalą. Kristale atomai ir molekulės yra tvarkingai išdėstytos skirtingose padėtyse: tai įprasta atomų tvarka. Kadangi atomai veikia kaip rentgeno spindulių sklaidytojai, dėl tvarkingo atomų išsidėstymo kristale išsklaidyti spinduliai yra konstruktyviai trikdomi ir todėl skleidžiami specialiomis kryptimis. Detektorius šiuos skleidžiamus spindulius užregistruoja kaip taškus, o gaunamas vaizdas vadinamas difrakcijos modeliu. Laue eksperimentas įrodė du dalykus: kristaluose atomai išsidėstę labai taisyklingai, o rentgeno spindulių bangos ilgis labai nedidelis (keletas manometro dešimtųjų dalių – tai tipiškas atstumas tarp atomų).
- 1913 m. Braggai (tėvas ir sūnus) sukūrė taip vadinamą Brago dėsnį (detalesnio Brago dėsnio aprašymo ieškokite Hughes, 2007), kuriuo nustatytas ryšys tarp rentgeno spindulių bangos ilgio (λ), atstumo (d) tarp dviejų atomų plokštumų kristale ir rentgeno spindulių kritimo kampo (θ): 2 d sin θ = n λ, kur n yra sveikasis skaičius. Šis svarbus atradimas žymi rentgeno spindulių kristalografijos pradžią, t.y. galimybę iššifruoti kristalo struktūrą, naudojant rentgeno spindulius. Pirmasis atominio skaidymosi struktūros uždavinys (1914 m.) buvo susijęs su valgomąja druska, o paskui greitai pereita prie deimanto. Skatinamas ankstyvos sėkmės, galingas rentgeno spindulių difrakcijos metodas suteikė mokslininkams galimybę suvokti ir paaiškinti įvairių rūšių kristalų atomo ir molekulinę struktūrą. „Tai priminė sąnašinio aukso lauko atradimą, kuriame grynuoliai tik ir laukė, kada bus paimti“, pripažino Bragai.
Tuo pačiu metu buvo išauginti pirmieji biologiniai kristalai, todėl atsirado galimybė tirti biologines molekules naudojant rentgeno spindulius. Pirmasis difrakcinis proteino vaizdas, gautas dar 1930 m. buvo enzimo, vadinamo pepsinu. Greitai mokslininkai išmoko izoliuoti virusą, jį kristalizuoti ir pademonstruoti, kad jis nepraranda savo biologinės galios: tabako mozaikinis virusas po kristalizacijos vis dar galėjo infekuoti tabako augalus. Makromolekulinės kristalografijos pamatai buvo padėti!
Įdomu tai, kad atliekant ankstyvuosius molekulinių struktūrų tyrimus, nedalyvavo nei vienas biologas. Tyrimus atliko chemikai, fizikai ir kristalografai, o tai rodo, kad pirmoje XX amžiaus pusėje daug kitų sričių mokslininkų domėjosi biologija. Tai geriausiai parodo 1944 m. gerai žinomo kvantinės mechanikos fiziko, Erwin Schrödinger, parašyta knyga What is Life? („Kas yra gyvenimas?“). Molekulinė biologija, atsiradusi 1940-aisiais kaip biochemijos ir genetikos junginys, nuo pat pradžių apjungė kelias disciplinas. Žinoma, šiai naujai disciplinai labai padėjo fizikų išrasti novatoriški įrankiai. Kalbant abstrakčiau, mintis, kad gyvybę galima paaiškinti paprastais cheminiais ir fiziniais mechanizmais buvo labai kontraversiška, todėl dauguma manė, kad gyvojo pasaulio sudėtingumo negalima sumenkinti iki biomolekulių sąveikos. Šiandien struktūrinė molekulinė biologija pripažįstama pagrindine biologijos šaka, kuri vis dar labai sparčiai vystosi.
Ši šaka stipriai priklauso nuo makromolekulinės kristalografijos ir remiasi tuo, kad kiekviena proteino molekulė turi savo elektronų debesį, kuris išsklaido rentgeno spindulių pluoštą, naudojamą kristalografijoje. Elektronų debesies forma ir dydis nustato, kaip bus sklaidomi rentgeno spinduliaiw2 – tai molekulės signalas. Daug mažų signalų, gaunamų iš didelio proteinų molekulių skaičiaus kristale, sudaro išmatuojamą signalą.
Iš keleto besisukančio kristalo kampų gaunamas difrakcijos vaizdas matematiškai transformuojamas (ši operacija vadinama Fourier transformacija) į proteino elektronų tankio žemėlapį, kuris vaizduoja proteino elektronų debesį. Pasitelkiant kompiuterinio modeliavimo ir tobulinimo technikas, proteino amino rūgščių seką galima priderinti prie šio elektronų debesies ir taip nustatyti trimatį atomų pasiskirstymą proteine. Tai yra galutinė struktūra.
Tačiau kodėl jų trimatė struktūra yra tokia svarbi proteinų ir kitų biologinių molekulių tyrimams?
Struktūra ir funkcija
Paveikslėlio autorinės teisės priklauso
geopaul / iStockphoto
Mūsų rankos ir akys, kaip ir kiti anatominiai augalų ir gyvūnų bruožai, evoliucijos metu keitėsi, kad galėtų patenkinti gyvybinius poreikius. Panašiai ir mikroskopinė kiekvienos subląstelinės organoidinės bei biologinės makromolekulės struktūra yra glaudžiai susijusi su jos funkcija. Taisyklingos formos molekulės yra atsakingos už genų įjungimą ir išjungimą, nuo ląstelių įsiveržėlių ginančios sudėtingos gyvybės chemijos kanalizavimą, ląstelių skaidimąsi skatinančių jungiklių bei kontrolės įjungimą.
Geriausiai molekulinės struktūros įtaką jos funkcijai išreiškia DNR. Paprasta ir graži dvigubos spiralės, pagrindinės poros DNR struktūra greitai puikiai išaiškina genetiką cheminiais terminais. Genai, anksčiau laikyti paslaptingais reiškiniais, kontroliuojančiais tam tikrų savybių paveldėjimą, buvo DNR molekulių segmentai, kuriuos galima išvyti besisukančio stiklinio virbo gale kaip cukraus vatą ant lazdelės (žr. Madden, 2006, paprastas DNR išgryninimo klasėje protokolas), taip gaunant pluoštą, kurį galima tirti naudojant rentgeno spindulių difrakciją. Nuostabios, bet paprastos DNR struktūros nustatymas tapo svarbiu struktūrinės biologijos žingsniu.
Priešingai tam, proteinų struktūros tyrimai nesuteikė paprasto ir viską apimančio paaiškinimo apie proteinų struktūrą ir funkciją. Nepaisant to, kad yra žinoma apie 45000 skirtingų proteinų rūšių struktūra, mes vis dar negalime nustatyti bendrų taisyklių rinkinio, leidžiančio numatyti trimatę proteino struktūrą, remiantis jo polipeptidų grandinės amino rūgščių seka. Proteinai atlieka daug daugiau biologinių funkcijų nei DNR, o funkcinė įvairovė apsprendžia ir struktūrinę įvairovę.
Struktūrinės genomikos silpnoji vieta: proteinų kristalizacija
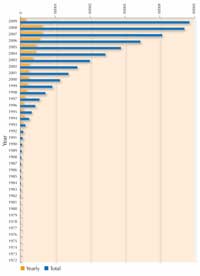
atskleidžiama rentgenu. Pastaba:
ieškomos struktūros laikui bėgant
keičiasi, nes kai kurios pasensta ir
būna pašalintos iš duomenų bazės.
Paspauskite čia, norėdami padidinti
paveikslėlį.
Lyginant su molekuline genetika, proteinų struktūros tyrimų pažanga labai lėta. Iš dalies tai įtakoja ir tokia paprasta techninė problema ‑ proteinų kristalų, kurie yra pakankamai dideli kristalografinei analizei, pakankamai gerai sklaido rentgeno spindulius ir leidžia nustatyti didelės skiriamosios gebos (atominę) struktūrą, gavimas. Be to, nors jie ir atrodo kaip mažų molekulių kristalai (pvz. virimo druskos kristalai), proteinų kristalai yra daug mažesni ir labai trapūs.
Todėl proteinų kristalizacija visada buvo netikslus užsiėmimas be nuspėjamos teorijos. Kai kurie proteinai lengvai kristalizuojasi, kiti atkakliai atsisako sudaryti tinkamus kristalus; atrodo, kad kai kurie tyrėjai turi „žalius pirštus“ kaip geri sodininkai, galintys užauginti kristalus ten, kur kiti nepajėgia. Todėl proteinų kristalizacija dažnai laikoma labiau menu nei mokslu.
Kiekvieno naujo proteino atveju mokslininkai turi išnagrinėti daugybę sąlygų, kad nustatytų tas, kuriomis jis gali kristalizuotis. Pagal sąlygas kintamieji gali būti: proteino koncentracija, temperatūra, pH bei plataus diapazono nusėdimo agentų, kuriuos galima naudoti kartu su įvairiomis druskomis, koncentracija. Norėdami išmėginti geriausias proteino kristalizacijos sąlygas klasėje ir ištirti savo rezultatus, naudojant rentgeno spindulių difrakciją tikroje kristalografijos laboratorijoje, žiūrėkite Blattmann & Sticher (2009). Kadangi proteinų kristalizacija sukelia tiek sunkumų, iki šiol daugiausiai buvo ištirti lengvai besikristalizuojantys proteinai, kuriuos galima gauti dideliais kiekiais, o ne įdomiausi proteinai. Visgi pastaruoju dešimtmečiu buvo padaryta nemaža pažanga. Paveikslėlyje matyti, kaip nuo 1983 m. augo proteino struktūrų nagrinėjimas naudojant rentgeno spindulių kristalografiją. Šią pažangą įtakojo patobulinta technika trijose srityse: kristalų paruošimas, sinchrotronų rentgeno spindulių kristalografija ir programinės įrangos raida.
Proteino kelionė iš vienos laboratorijos į kitą
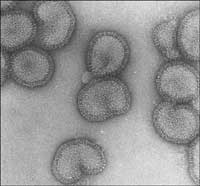
gripo virusas
Paveikslėlio autorinės teisės priklauso
Rob Ruigrok/ UVHCI
Norėdami iliustruoti, kaip proteino struktūra išsprendžiama, naudojant šiandieninius moderniausius instrumentus, mes panagrinėsime, kaip mokslininkai identifikavo vieno iš gripo viruso proteinų, polimerazės, struktūrą. Grupė Europos molekulinės biologijos laboratorijos (EMBL Grenoblio stoties) ir Viruso šeimininko-ląstelės sąveikos padaliniow4 (UVHCI, Grenoblis) mokslininkų nagrinėjo šį proteiną, kuris yra įtrauktas į procesą, kai virusas perima savo infekuoto žmogaus ląstelių veikimą (daugiau duomenų apie tyrimus ir rezultatus žr. Ainsworth, 2009). Šio projekto tikslu mokslininkai pasinaudojo Struktūrinės biologijos partnerystew5 (PSB), kad iššifruotų biologinių molekulių struktūras, keliančias susidomėjimą medicinai.
Klonavimas ir išreiškimas (UVHCI, EMBL ir PSB)
Parinkus proteiną tyrimams, atitinkamas jo genas buvo sustiprinamas, t.y. klonuojamas į specialią išraiškos sistemą. Tai leidžia gauti didelius proteinų kiekius, naudojant užkrėtimo sistemą, paprastai bakterijas.
Išgryninimas (PSB) ir kokybės vertinimas (IBS)
Tada bakterijų ląstelės buvo surenkamos centrifugavimo būdu, o ląstelių nuolaužos arba galimi teršalai (pvz. nukleino rūgštys) pašalinamos. Tada proteinui taikomas ilgas, bet svarbus daugiaetapis išgryninimo procesas, nes kristalizacijai reikia mažiausiai 95% grynumo. Proteino kokybę įvertino Jean Pierre Ebel struktūrinės biologijos institutew6 (IBS), naudodamas masės spektrometriją (trumpo masės spektrometrijos pristatymo ieškokite Wilson & Haslam, 2009). Sintezatoriumi buvo tikrinama, ar išgrynintas proteinas yra tas, kurį norėta gauti – gripo viruso polimerazė.
Kristalizacija (PSB)
Mokslininkai stengėsi kristalizuoti proteiną, naudodami multifaktorinį filtrą. Kitaip sakant, skirtingoms proteinų koncentracijoms jie naudojo skirtingus kristalizacijos agentus, buferius, temperatūras ir pan. Vadinamasis mikropartijos metodas (žr. paveikslėlį žemiau) skirtas maksimaliam informacijos kiekiui apie proteiną, kurį ketinama kristalizuoti, gauti naudojant minimalų pavyzdžio kiekį.
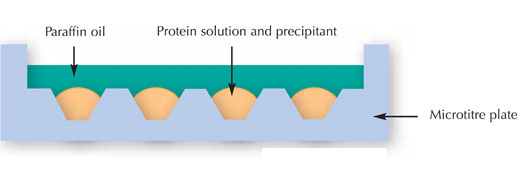
Paveikslėlio autorinės teisės priklauso Nicola Graf
Rentgeno spindulių difrakcija sinchrotrono pluošto linijoje ir duomenų gavimas (ESRF)

Paveikslėlio autorinės teisės
priklauso ESRF

pluošto linijos
Paveikslėlio autorinės teisės
priklauso ESRF
Gavę polimerazės kristalus, mokslininkai užšaldė juos skystame azote ir pernešė į Europos sinchrotrono radiacijos infrastruktūros (ESRF)w1 pluošto liniją. Čia kristalas buvo pritvirtintas prie goniometro galvutės – tai paprastai daro robotas – ir veikiamas sinchrotrono rentgeno spinduliais, kurie yra labai intensyvūs. Goniometras – tai instrumentas, leidžiantis sukti tokį objektą kaip kristalas iki tikslaus kampo.
Goniometro galvutė buvo sukama rentgeno spindulių pluošte, siekiant gauti maksimalų atspindžių kiekį arba išsklaidytus pluoštus. Taip gaunamas milžiniškas duomenų kiekis (tai įprasta renkant duomenis iš sinchrotrono šaltinių), todėl faktinė proteino struktūra nustatoma automatiškai, naudojant specialiai šiam tikslui sukurtą programinę įrangą.
Modelio sukūrimas, žemėlapio pritaikymas, patobulinimas ir patvirtinimas (UVHCI ir EMBL)
Remiantis surinktais ir apdirbtais duomenimis, buvo sudarytas atominis polimerazės modelis ir palygintas su elektronų tankio žemėlapiu. Tuomet, naudojantis galinga programine įranga ir interaktyvia molekuline grafika, modelis buvo pakartotinai patobulintas, kad geriausiai atitiktų pastebėtus duomenis. Patvirtinus modelį, struktūra buvo paskelbta ir pateikta viešai prieinamame proteino duomenų bankew7.
ESRF: vienas didžiausių rentgeno spindulių šaltinių pasaulyje
ESRF yra puikus didelės kasdien ir kasnakt veikiančios infrastruktūros pavyzdys, skirtas tūkstantiems vartotojų iš viso pasaulio. „Vartotojas“ – tai mokslininkas, dažnai esantis didesnės komandos dalimi, kuriam kartais reikia galingo įrankio informacijai apie tam tikrą pavyzdį gauti (pvz., medžiagos dalis, proteino kristalas, suakmenėjusi iškasena, katalitinė reakcija). Dauguma vartotojų kelis kartus per metus vyksta į Grenoblį susirinkti duomenis iš ESRF.

infrastruktūra
Paveikslėlio autorinės teisės
priklauso P. Ginter/ESRF
Būdama trečios kartos šaltiniu, ESRF išgauna labai intensyvius rentgeno spindulius, vadinamus sinchrotrono radiacija. Šiuos rentgeno spindulių pluoštus skleidžia didelės energijos elektronai (6 GeV), kurie cirkuliuoja po didelį „saugojimo žiedą“, kurio perimetras yra 844 metrai. Sinchrotrono rentgeno spinduliai labai vizuojami, panašiai kaip lazerio spinduliai (vizuojamos šviesos spinduliai yra beveik analogiški).
Rentgeno spindulių pluoštai yra nukreipti į pluošto linijas, supančias saugojimo žiedą eksperimentinėje salėje. Kiekvienai iš 42 ESRF pluošto linijų taikoma speciali metodika ar tyrimo tipas. Maždaug 10 jų specializuojasi proteinų kristaluose. ESRF pluošto linijos automatizuojamos, kad jas būtų lengviau naudoti, o mokslininkai galėtų dirbti su jomis iš toli. Tai leidžia vartotojams atlikti sinchrotrono eksperimentus, fiziškai neišeinant iš namų laboratorijos. Kristalai į ESRF yra siunčiami, o ne pristatomi asmeniškai, net jeigu mokslininkai ten ir vyksta patys, kadangi dabartiniai saugumo apribojimai apsunkina kelionę, vežantis jautrius biologinius pavyzdžius.
Sinchrotrono radiacija sudaro maždaug 80% šiuo metu proteinų duomenų bankew7 banke esančių makromolekulinių kristalo struktūrų (1995 m. tik 17% buvo gauta iš sinchrotrono duomenų, Žr. paveikslėlį viršuje). ESRF išgauna maždaug 20% bendro kiekio.
References
- Ainsworth C (2009) Outmanoeuvering influenza’s tricks. Science in School 11: 25-29. www.scienceinschool.org/2009/issue11/influenza
- Blattmann B, Sticher P (2009) Growing crystals from protein. Science in School 11: 30-36. www.scienceinschool.org/2009/issue11/lysozyme
- Hughes D (2007) Taking the stress out of engineering. Science in School 5: 61-65. www.scienceinschool.org/2007/issue5/stress
- Madden D (2006) Discovering DNA. Science in School 1: 34-36. www.scienceinschool.org/2006/issue1/discoveringdna
- Schrödinger E (1944) What is Life? Cambridge, UK: Cambridge University Press
- Wilson A, Haslam S (2009) Sugary insights into worm parasite infections. Science in School 11: 20-24. www.scienceinschool.org/2009/issue11/schistosomiasis
Web References
- w1 – Daugiau informacijos apie ESRF žr.: www.esrf.eu
- w2 – Daugiau informacijos apie protein kristalizacijos teoriją ir retgeno spindulių disfrakciją žr.: www-structmed.cimr.cam.ac.uk/Course
- w3 – daugiau informacijos apie EMBL žr.: www.embl.fr
- w4 – daugiau informacijos apie Viruso šeimininko-ląstelės sąveikos padalinį žr.: www.uvhci.fr
- w5 – Struktūrinės biologijos bendrija (PSB) bendradarbiauja su EMBL, Institut de Biologie Structurale, ESRF ir Institut Laue-Langevin – lyderiaujančiu pasauliniu neutronų šaltiniu. PSB užtikrina integruotą struktūrinės biologijos aplinką, pagrįstą tokiomis technologijomis, kaip: klonavimas ir ekspresija, kristalų produkcija, fizikiniu-cheminiu-biocheminiu charakterizavimu, rentgeno spindulių bei neutronų kristalografija, atominiu magnetiniu rezonansu (NMR), elektronų mikroskopija ir tomografija, mažo kampo rentgeno spindulių ir neutronų sklaida, masine spektroskopija bei pažangia šviesos mikroskopija. Žr.: www.psb-grenoble.eu
- w6 – Daugiau informacijos apie IBS žr.: www.ibs.fr
- w7 – Daugiau informacijos apie Proteinų duomenų banką žr.: www.rcsb.org/pdb
Resources
- Abad-Zapatero C (2002) Crystals and Life: A Personal Journey. La Jolla, CA, USA: International University Line. ISBN: 9780972077408
- Blow D (2002) Outline of Crystallography for Biologists. Oxford, UK: Oxford University Press
- Branden C, Tooze J (1991) Introduction to Protein Structure. New York, NY, USA: Garland
- Michette A, Pfauntsch S (1996) X-rays: the first hundred years. Chichester, UK: John Wiley & Sons
- Wood EA (1972) Crystals – A Handbook for School Teachers. Chester, UK: International Union of Crystallography
- Kristalų auginimo eksperimentai, žr.: www.sciencecompany.com/sci-exper
- Tarptautinė kristalografijos sąjunga, žr.: www.iucr.org





