Supporting materials
Come allestire la vostra fermentazione (Word)
Come allestire la vostra fermentazione (Pdf)
Download
Download this article as a PDF

Tradotto da Marianna Pizzetti. I paesi europei sono i maggiori produttori di realizzandone più della metà a livello mondiale – e gli europei sono anche tra i maggiori consumatori! Queste semplici attività pratiche scolastiche rivelano i segreti della scienza per un vino perfetto.

L’età a cui è legale bere bevande alcoliche è diversa da nazione a nazione, la maggior parte degli insegnanti sarà sicuramente d’accordo nell’affermare che bere vino nel corso delle lezioni di chimica è inopportuno (ed anche potenzialmente pericoloso!). Nonostante questo, la produzione del vino e la sua analisi a scuola può rivelarsi molto interessante e divertente.
Le attività sviluppate al centro scientifico Experimentaw1 coinvolgono studenti di età compresa tra i 15 e i 18 anni nell’utilizzo di tecniche analitiche per esplorare i processi che avvengongono durante la vinificazione.
La produzione del vino avviene per fermentazione del succo di uva (che contiene una alta percentuale di zucchero) utilizzando delle cellule di lievito specifiche. Lo zucchero viene trasformato in etanolo e anidride carbonica in condizioni anaerobiche:
C6H12O6 + 2 ADP + 2 Pi = 2 C2H5OH + 2 CO2 + 2 ATP
Experimentaw1 ad Heilbronn è il principale centro scientifico di apprendimento interattivo nel sud della Germania. Oltre alle mostre interattive e al giardino scientifico, Experimenta offre più di trenta programmi basati su attività di laboratorio per scolaresche o alunni individuali, dall’asilo fino all’istruzione secondaria. Questi programmi riguardano le nuove tecnologie e tutte le scienze della vita oltre ad un supporto nell’insegnamento di queste discipline.

La qualità finale del vino è legata principalmente a tre fattori: la dolcezza, il contenuto di alcol e il tasso di acidità. Le tre attività proposte per gli studenti, basate su metodi standard utilizzati da laboratori di analisi di vini commercializzati, esplorano la correlazione tra la qualità dell’uva spremuta, il mosto (il succo dell’uva fermentato) e il prodotto finale. Ogni attività richiede un tempo di circa 20-30 minuti.


Possono essere inoltre scaricate altre quattro attivitàw2:
Per avere a disposizione il mosto necessario per svolgere gli esperimenti sarà necessario iniziare una semplice fermentazione del succo di uva almeno con un giorno di anticipo, utilizzando succo ottenuto da uva rossa (e.g. del supermercato). Sarà inoltre necessario della semplice attrezzatura da laboratorio, un vinometro per la misurazione del contenuto di etanolo (noto anche come una bottiglia da gravità specifica) e un rifrattometro. Una descrizione di come condurre la fermentazione è disponibile per essere scaricataw2.

La dolcezza del vino è data dalla quantità residua di zucchero che rimane dopo il processo di fermentazione insieme all’acidità totale. Un vino secco contiene fino a 9 g/l di zucchero ed un livello di acidità inferiore di almeno 2 g/l rispetto al contenuto zuccherino. Un vino mediamente secco ha un contenuto di zucchero tra 9 e 18 g/l ed un’acidità non più bassa di 10 g/l rispetto al contenuto di zucchero. Un vino dolce ha un contenuto zuccherino compreso tra 18 e 45 g/l. Perché il bilanciamento della dolcezza, dell’acidità e del contenuto alcolico nel prodotto finito sia corretto, è molto importante la determinazione della concentrazione di zucchero iniziale; se necessario prima della fermentazione possono essere aggiunte delle limitate quantità di zucchero.
Il mosto (se confrontato con l’acqua) presenta una densità più elevata, dovuta allo zucchero in fermentazione. Sia la misurazione della densità che la rifrattometria possono essere utilizzate per misurare il contenuto di zucchero, parametro che in Germania viene espresso come peso del mosto e misurato in Oechsle (°Oe). Nei paesi anglofoni, il contenuto di zucchero è invece espresso in Brix (°B), unità che esprime la concentrazione dello zucchero dissolto, in peso per cento (wt%).
Il peso del mosto è calcolato attraverso la formula:
peso del mosto= (densità – 1) x1000
Dove il peso del mosto è espresso in °Oe e la densità in g/l.
In linea di massima 1 °Oe corrisponde a 2.37 g/l di zucchero (i.e. circa 0.237 °Bx). Quindi la concentrazione di zucchero può essere espressa come:
concentrazione di zucchero = peso del mosto x 2.37
Dove la concentrazione dello zucchero è misurata in g/l.
In una soluzione di 100 °Oe (concentarzione di zucchero di 237 g/l o 23.7 °Bx) la fermentazione di tutto lo zucchero presente porta all’ottenimento di circa 100 g/l di etanolo (o al 10%wt di alcol). Poichè l’etanolo ha una densità di 0.79 g/ml questo porta a 12.67 vol% di etanolo. Quindi:
Concentrazione di alcol (in volume%) = concentrazione di alcol (in g/l) x 0.1267
La quantità di zucchero contenuta nel succo di uva va a determinare sia il contenuto di alcol sia la dolcezza finale del vino prodotto. In questa attività l’indice di rifrazione verrà utilizzato come parametro per la misurazione del contenuto di zucchero.
Il fenomeno della rifrazione è basato sul cambiamento che la direzione della luce subisce passando da un mezzo ad un altro (ad es. dall’aria all’acqua). La capacità di riflettere la luce di una soluzione cambia all’aumentare della concentrazione dei soluti (sostanze disciolte). Questo principio è alla base del funzionamento del rifrattometro per la determinazione della concentrazione delle particelle sciolte in una soluzione. Nel vino i soluti sono rappresentati principalmente dal saccarosio.
La maggior parte dei rifrattometri manuali fornisce una misura della concentrazione delle sostanze disciolte sia in Brix (°Bx), scala basata sul contenuto di saccarosio, che in Oechsle (°Oe). Una soluzione al 20% wt di saccarosio in acqua è 20 °Bx. La conversione in Oechsle può essere effettuata semplicemente moltiplicando per 0.237.

| 20 wt% di saccarosio | Succo d’uva | |
|---|---|---|
| Peso del mosto (°Oe) | ||
| Concentrazione di zucchero (°Bx) | ||
| Resa possibile dell’alcol (vol%) |
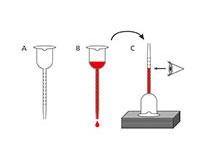
La quantità di alcol ottenuta per fermentazione dipende dal contenuto zuccherino del succo dell’uva e dalla tolleranza dell’alcol del tipo di lievito: la maggior parte dei ceppi di lievito tollerano fino al 16% di alcol. La quantità di alcol può essere misurata in modo abbastanza accurato utilizzando un vinometro, uno strumento semplice sviluppato per chi produce il vino solo per hobby. Questo apparecchio è basato sul principio che la tensione superficiale diminuisce all’aumentare del contenuto alcolico.
In questa attività misurerete il contenuto alcolico del mosto.
| Contenuto di alcol (vol%) | |
|---|---|
| Mosto (filtrato) | |
| vino |
Nota: Il contenuto alcolico del mosto è probabilmente molto inferiore a quello del vino. Questo può essere dovuto al fatto che il processo di fermentazione non è terminato. Può anche essere indice del fatto che lo zucchero rimanente ha portato ad un aumento nella tensione superficiale e questo influenza la lettura.

Diversi tipi di acidi possono essere contenuti nei succhi della frutta, inclusi l’acido tartarico, malico, citrico ed ossalico, in rapporti diversi a seconda del tipo di frutto. Nel vino l’acido tartarico, che ha un pH compreso tra 3 e 4, è quello predominante. La semplice misura del pH del vino comunque non è una misura attendibile da cui stimare il contenuto totale di acido a causa della presenza di una complessa miscela di acidi e basi, sali e proteine. La titolazione dell’acido tartarico è invece un metodo che permette di determinare il contenuto totale espresso come quantità totale di acido tartarico in g/l. Il contenuto di acido nel vino è tipicamente 4-8.5 g/l ma può raggiungere anche valori di 15 g/l. Deve comunque sempre essere considerato in correlazione alla quantità di zucchero residuo (vedi ‘Determinazione del contenuto di zucchero’).
L’acido tartarico (peso molecolare 150 g/mol) è un acido diprotico (contiene cioè due atomi di idrogeno che in acqua possono dissociare come protoni) che può essere neutralizzato completamente con idrossido di sodio. Poichè 1 mol di NaOH neutralizza 0.5 mol di acido tartarico (75 g/l), 1 ml di NaOH 0.1 M neutralizza 7.5 mg di acido tartarico.
HOOC-CH(OH)-CH(OH)-COOH + 2NaOH → Na+-OOC-CH(OH)-CH(OH)-COO– Na+ + 2H2O
Tutti i vini contengono una certa quantità di specie acide. I produttori di vino sono soprattutto interessati alla determinazione della quantità totale di acido, dovuta principalmente all’acido tartarico. L’acidità totale viene determinata per titolazione con una soluzione di idrossido di sodio.
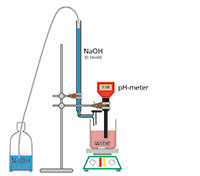
Per ciascun campione (mosto o vino):
Esempio: Abbiamo usato 14 ml di NaOH 0.1 M per neutralizzare 10 ml della soluzione. La concentrazione dell’acido quindi è (14 x 7.5 mg/ml x 100) = 10.5 g/l.
| Mosto | vino | |
|---|---|---|
| pH iniziale | ||
| Volume iniziale NaOH (ml) | ||
| Volume finale NaOH (ml) | ||
| Volume utilizzato di NaOH (ml) | ||
| Concentrazione di acido (g/l) |
Indossare occhiali di sicurezza e guanti. Consultare anche le norme di sicurezza generali.

Nelle attività 1-3 avete analizzato i tre fattori principali che determinano la qualità del vino prodotto: la dolcezza, il contenuto di alcol e di acido. E’ arrivato il momento di dare una valutazione del vostro vino.
L’autore desidera ringraziare il laboratorio vinicolo di Pfäffle GmbH ad Heilbronn, in Germania per il supporto durante l’ideazione delle attività proposte. Un ringraziamento per la loro collaborazione in particolare a Christine Dietrich e Karsten Wiese del centro di educazione degli insegnanti di Heilbronn.
Come allestire la vostra fermentazione (Word)
Come allestire la vostra fermentazione (Pdf)
Download this article as a PDF