Supporting materials
Het opzetten van je gisting (Word)
Het opzetten van je gisting (Pdf)
Download
Download this article as a PDF

Vertaald door Piet Das. Europese landen produceren meer dan de helft van de wijn in de wereld – en drinken er ook veel van op! Dit practicum voor scholen onthullen de wetenschap achter de perfecte wijn.

De leeftijd waarop het legaal is om alcohol te drinken varieert van land tot land, maar de meeste leraren zullen beamen dat wijn drinken in scheikunde lessen ongepast (en mogelijk gevaarlijk) is. Het maken en analyseren van wijn op school is echter leuk en leerzaam. Deze activiteiten, ontwikkeld in het science center Experimentaw1, nodigen leerlingen van 15-18 jaar uit om gedurende één dag wijnboer te worden, waarbij ze met behulp van analytische technieken de veranderingen onderzoeken die plaatsvinden tijdens het wijnbereidingsproces.
Wijn wordt geproduceerd door het vergisten van druivensap (dat bijzonder grote hoeveelheden suiker bevat) met behulp van gespecialiseerde gistcellen . De suiker wordt omgezet in ethanol en koolstofdioxide onder anaerobe omstandigheden :
C6H12O6 + 2 ADP + 2 Pi = 2 C2H5OH + 2 CO2 + 2 ATP
Experimentaw1 in Heilbronn is het grootste natuurwetenschappelijke centrum in Zuid-Duitsland op het gebied van informeel leren en interactief met natuurwetenschappen bezig zijn. In aanvulling op de interactieve tentoonstellingen en wetenschapstuin, biedt Experimenta meer dan 30 in het laboratorium ontwikkelde programma’s voor schoolklassen en individuele leerlingen, van kleuterschool tot hoger middelbaar onderwijs . Deze programma’s richten zich op technologie en alle biowetenschappen maar ook op het opleiden van leraren.

De drie belangrijkste factoren die de kwaliteit van het eindproduct bepalen zijn: zoetheid, alcohol- en zuurgehalte. Met behulp van standaard methoden van een commercieel wijnlaboratorium , wordt bij deze drie activiteiten voor het schoolpracticum onderzocht hoe de kwaliteit van het uitgangsmateriaal, druivensap en most ( gistende druivensap), het eindproduct beïnvloeden. Elk practicum duurt ongeveer 20-30 minuten.

Er kunnen nog vier andere practica worden gedownloadw2:

Om te voorzien in voldoende most voor deze experimenten moet u ten minste een dag van tevoren een eenvoudige druivensapgisting opzetten, waarbij u rood druivensap (bijvoorbeeld uit de supermarkt) gebruikt. U zult ook wat simpele laboratoriumbenodigdheden nodig hebben, plus een vinometer voor het meten van het alcoholgehalte, een pyknometer (ook bekend als dichtheidsmeter) en een refractometer . U kunt een beschrijvingn downloaden hoe de gistingw2 opgezet moet worden.

De zoetheid van de wijn wordt bepaald door de hoeveelheid suiker die overblijft na vergisting samen met de totale zuurgraad van de wijn. Een droge wijn heeft tot 9 g/l suiker en een zuurgraad die ten minste 2 g/l lager dan het suikergehalte. Een halfdroge wijn heeft een suikergehalte van 9-18 g/l en een zuurgraad die niet meer dan 10 g/l lager mag zijn dan het suikergehalte. Een zoete wijn bevat 18 tot 45 g/l suiker. Om de juiste balans tussen suiker, alcohol en zuur in de uiteindelijke wijn te krijgen is het belangrijk om de aanvankelijke suikerconcentratie te bepalen en, indien nodig, beperkte hoeveelheden suiker toe te voegen voordat de vergisting begint.
De verhoogde dichtheid van de most (ten opzichte van het water ) wordt vooral veroorzaakt door de vergistbare suikers . Dichtheidsmetingen of refractometrie kunnen worden gebruikt om het suikergehalte, dat in Duitsland wordt uitgedrukt als het mostgewicht en gemeten in Öchsle ( ° Oe ) te meten. In het Engels taalgebied wordt het suikergehalte uitgedrukt in Brix ( ° Bx ) , dat de concentratie van opgeloste suiker in gewichtsprocenten (massa %) weergeeft.
Het mostgewicht wordt berekend door:
mostgewicht = (dichtheid – 1) x 1000
Waarbij het mostgewicht wordt gemeten in °Oe en de dichtheid in g/l.
Ruw geschat komt 1 ° Oe overeen met 2,37 g / l suiker ( dat wil zeggen ongeveer 0,237 ° Bx ). Derhalve kan de suikerconcentratie worden geschat op:
suikerconcentratie = mostgewicht x 2.37
Waarbij de suikerconcentratie wordt gemeten in g/l.
De vergisting van vergistbare suiker in een oplossing van 100 ° Oe ( suikerconcentratie 237 g / l of 23,7 ° Bx ) geeft ongeveer 100 g/l ethanol (of 10 massa % alcohol) . Omdat ethanol een dichtheid heeft van 0,79 g/ml , komt dit overeen met 12,67 vol% ethanol . Dus:
alcoholconcentratie (in volume %) = alcohol concentratie (in g/l) x 0,1267
De hoeveelheid suiker in het druivensap zal bepalend zijn voor zowel het alcoholgehalte als de zoetheid van de uiteindelijke wijn. In dit practicum ga je gebruik maken van de brekingsindex om het suikergehalte te schatten.
Breking van het licht (refractie) is de verandering in de richting van het licht die optreedt als het van het ene medium naar het andere gaat (bijvoorbeeld van lucht naar water). Het licht verstrooiende gedrag van een oplossing verandert als de concentratie van opgeloste stoffen (in de oplossing) toeneemt. Een refractometer gebruikt dit principe om de concentratie van opgeloste deeltjes in een oplossing te bepalen. In wijn zijn dit voornamelijk de saccharose deeltjes
De meeste handrefractometers geven de concentratie van de opgeloste stof óf in Brix (° Bx ), waarbij een schaal is vastgelegd aan de hand van het saccharosegehalte óf in Oechsle (° Oe ) . Een oplossing van 20 massa % saccharose in water is 20 ° Bx. Öchsle kan ongeveer worden omgezet in Brix door vermenigvuldiging met 0,237.

| 20 massa % saccharose | Druivensap | |
|---|---|---|
| Gewicht van de most (°Oe) | ||
| Suikerconcentrati (°Bx) | ||
| Mogelijke alcoholopbrengst (vol%) |
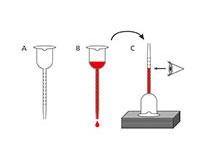
De hoeveelheid alcohol verkregen door gisting is afhankelijk van het suikergehalte van het druivensap en de alcoholtolerantie van de gist stam : de meeste giststammen tolereren tot 16% alcohol. De hoeveelheid alcohol kan vrij nauwkeurig worden gemeten met behulp van een vinometer, een eenvoudig apparaat ontwikkeld voor hobbywijnmakers. Het is gebaseerd op het principe dat de oppervlaktespanning afneemt naarmate het alcoholgehalte toeneemt.
In dit practicum meet je het alcoholgehalte van je most.
| Alcoholgehalte (vol%) | |
|---|---|
| Most (gefilterd) | |
| Wijn |
NB: Het alcoholgehalte van de most is waarschijnlijk veel lager dan van de wijn. Dit kan veroorzaakt zijn doordat het gistingsproces nog niet klaar is. Het kan ook betekenen dat de resterende suiker de oppervlaktespanning heeft doen toenemen en het aflezen beïnvloedt.

Vruchtensappen kunnen meerdere verschillende zuren bevatten, zoals wijnsteenzuur, appelzuur , citroenzuur en oxaalzuur en in verschillende verhoudingen, afhankelijk van het soort fruit. Het overheersende zuur in wijn is wijnsteenzuur, die een pH tussen 3 en 4 heeft . Vanwege het complexe mengsel van verschillende zuren en basen , eiwitten en zouten , kan het totale zuurgehalte niet worden afgeleid uit de pH-waarde alleen. In plaats daarvan wordt het bepaald door titratie tot de oplossing neutraal is en uitgedrukt als totale equivalente hoeveelheid wijnsteenzuur in g/l . De meest voorkomende hoeveelheid zuur is 4-8,5 g/l , maar kan oplopen tot 15 g/l . Het moet altijd worden bekeken in combinatie met de hoeveelheid resterende suiker ( zie ‘ bepalen van het suikergehalte “).
Wijnsteenzuur ( molecuulgewicht 150 g ) is een diprotisch zuur (dat twee waterstofatomen per molecuul bevat die in water uiteen vallen tot protonen ) die volledig geneutraliseerd kan worden met natriumhydroxide. Omdat 1 mol NaOH 0,5 mol wijnsteenzuur (75 g/l) neutraliseert, neutraliseert 1 mL 0,1 M NaOH dus 7,5 mg wijnsteenzuur.
HOOC-CH(OH)-CH(OH)-COOH + 2NaOH → Na+-OOC-CH(OH)-CH(OH)-COO– Na+ + 2H2O
Alle wijnen bevatten een bepaalde hoeveelheid zuur. De wijnmaker is geinteresseerd in de totale zuurgraad die voornamelijk bepaald wordt door wiijnsteenzuur. De totale zuurgraad wordt bepaald door titratie met verdund natriumhydroxide.
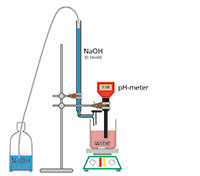
Voor elk monster (wijn of azijn):
Bijvoorbeeld: we gebruikten 14 mL 0,1 M NaOH om 10 mL oplossing te neutraliseren. De concentratie is daarom (14 x 7.5 mg/ml x 100) = 10,5 g/l zuur.
| Most | Wijn | |
|---|---|---|
| Begin pH | ||
| Begin volume NaOH (mL) | ||
| Eind volume NaOH (mL) | ||
| Gebruikte NaOH (mL) | ||
| Concentratie zuur (g/l) |
Draag een veiligheidsbril en handschoenen. Lees ook de algemene veiligheidsvoorschriften.

In de practica 1-3 heb je de drie belangrijkste factoren die de kwaliteit van het uiteindelijke produkt bepalen, geanalyseerd: zoetheid en het alcoholgehalte en de hoeveelheid zuur.
De auteur zou graag het wijnlaboratorium van Pfäffle GmbH in Heilbronn, Duitsland, willen bedanken voor de ondersteuning tijdens het ontwikkelen van de practica. Hij zou ook graag in het bijzonder Christine Dietrich en Karsten Wiese van de lerarenopleiding in Heilbronn willen bedanken voor hun samenwerking.
Schmitt A (1975) Aktuelle Weinanalytik, Ein Leitfaden für die Praxis. Germany: Heller Chemie. ISBN: 978-3-9800498-3-2
Het opzetten van je gisting (Word)
Het opzetten van je gisting (Pdf)
Download this article as a PDF