La science au secours des navires anciens Understand article
Traduction Dominique Cornuéjols. Le Mary Rose fait partie des vaisseaux célèbres qui, après avoir coulé, ont été relativement bien conservés au fond de l’eau grâce aux conditions anaérobies. Sortis de l’eau pour leur intérêt historique, ils risquent cependant de se dégrader.…
Le Mary Rose

Image reproduite avec
l’aimable autorisation de Mary
Rose Trust
Le Mary Rose, le navire amiral du roi Henry VIII, est le seul vaisseau de guerre du 16e siècle qui soit présenté au public. Construit à Portsmouth et lancé en 1511, il fit la gloire de la marine Tudor pendant 34 ans, jusqu’en 1545, date à laquelle il fut coulé lors d’une bataille navale contre les Français. Bien que la cause exacte du naufrage du Mary Rose ne soit pas clairement établie, une erreur humaine est l’hypothèse la plus probable. Au cours d’une mauvaise manoeuvre, le bateau s’est incliné fortement et l’eau a pu pénétrer par les ouvertures latérales prévues pour les canons, ce qui a définitivement scellé son sort, ainsi que celui de centaines d’hommes à bord. Il est ainsi resté au fond de la Manche pendant environ 400 ans, à une profondeur de 14 mètres, recouvert de glaise, jusqu’à ce que des archéologues le délivrent en 1982. Le bateau offre un aperçu unique sur la vie en mer au temps des Tudor, mais le fait d’être à l’air libre impose des soins de conservation particuliers.
Le danger des composés de soufre et de fer
Les composés soufrés qui se sont accumulés dans la structure en bois du bateau constituent la menace principale pour le Mary Rose aujourd’hui. Dans l’eau de mer, les bactéries qui se nourrissent à partir de matière organique (les hydrates de carbone, (CH2O)n), réduisent les ions sulfates, SO42-, en sulfure d’hydrogène H2S.
(CH2O)n + n/2SO42- → n/2H2S(aq) + nHCO3–
Le sulfure d’hydrogène dissous, H2S(aq), pénètre ensuite dans le bois, où il est transformé en composés soufrés réduits solides, tels que les thiols, R-SH (R représente une partie organique), dans la lignine du bois et en sulfures de fer (II) lorsque des ions de fer sont disponibles. Au cours des siècles, le soufre réduit s’est accumulé ; des analyses chimiques ont montré que le bois de la coque du Mary Rose contient aujourd’hui environ 1% de son poids (au total, 2 tonnes) de soufre S.
Une fois le bateau sorti de l’eau, les composés soufrés à l’intérieur du bois commencent à s’oxyder, formant de l’acide sulfurique H2SO4. Si rien n’est fait, l’acide pourrait lentement dégrader les fibres de la cellulose du bois et mettre en danger la stabilité de la coque.
En présence des ions de fer, la menace de l’acide devient particulièrement aiguë car les ions de fer servent de catalyseurs dans les processus d’oxydation et amplifient la production d’acide sulfurique. La structure en bois du Mary Rose, comme celle de beaucoup d’autres épaves, contient du fer provenant de la corrosion des rivets, clous et autres objets présents sur le bateau. Au fond de la mer, les ions de fer (II) dissous se sont combinés avec le sulfure d’hydrogène pour former des sulfures de fer, comme par exemple la pyrite, FeS2, qui est instable lorsque le bois humide est exposé à l’oxygène :
FeS2(s) + 7/2O2 + (n+1)H2O → FeSO4·n(H2O)(s) + H2SO4(aq)
Les sulfates de fer (II) hydratés comme la mélantérite, FeSO4·7(H2O)(s) et la rozénite, FeSO4·4(H2O)(s), sont trouvés couramment sous forme de précipités dans le bois archéologique chargé en soufre.
Les rayons X au secours
Les rayons X sont connus pour leur utilisation médicale en imagerie et radiothérapie, mais ils peuvent être aussi d’un grand secours au chevet des épaves de bateaux. Les rayons X ont la capacité d’analyser de façon non destructive les différents éléments présents dans un objet, ainsi que leur état chimique. Pour obtenir une telle information sur le soufre, la technique de choix est la spectroscopie d’absorption des rayons X. Des rayons X d’une certaine énergie sont envoyés sur l’échantillon à étudier, excitant les électrons des couches profondes des atomes de soufre qui sautent alors sur des couches plus extérieures ou sont éjectés sous forme de photoélectrons. Une technique, connue sous le nom de spectroscopie photoélectronique, consiste à mesurer l’énergie cinétique de ces photoélectrons. Une autre technique, la fluorescence X, analyse les rayons X émis par l’échantillon lorsque les atomes excités reviennent à leur état d’origine.
De cette façon, l’énergie de liaison de l’électron excité peut être mesurée, ce qui caractérise le type de composé soufré. Pour le Mary Rose, il était essentiel de trouver les quantités et les localisations des composés de soufre et de fer dans le bois. Des rayons X très intenses, connus sous le nom de lumière synchrotron (voir encadré), ont été nécessaires pour investiguer la composition chimique du Mary Rose au niveau microscopique, et en déduire la stratégie la plus adaptée pour le protéger d’une dégradation annoncée.
Améliorer la conservation

vaporisée avec une solution
de polyéthylène glycol depuis
10 ans pour remplacer l’eau
et empêcher l’apparition de
fissures pendant le séchage
des poutres.
Image reproduite avec
l’aimable autorisation de Mary
Rose Trust
Pour conserver le Mary Rose dans les meilleures conditions sur le long terme, il est indispensable de retirer du bois les sulfures de fer qui provoquent la formation d’acide. Au cours du traitement de vaporisation actuel, qui a commencé il y a 10 ans, l’acide est emporté dès qu’il se forme (voir photo). Pour pouvoir extraire plus rapidement les sulfures de fer, une technique innovante a été testée, l’oxydation douce par oxygène singulet 1O2, une forme d’oxygène énergétique, de courte durée de vie, produite par rayonnement ultraviolet en excitant un électron de valence de la molécule ordinaire O2. Pour augmenter le rythme des réactions, on pourrait élever légèrement la température de la solution vaporisée, mais la formation de bactéries légionelles peut présenter un danger pour la
Des investigations récentes, en particulier les analyses par microscopie à rayons X à l’ESRF (European Synchrotron Radiation Facility), ont permis de suggérer de nouvelles pistes de recherche. Une méthode testée récemment consiste à enlever le fer au moyen d’un chélate, connu sous le nom d’EDMA (ethylenediiminobis (2-hydroxy-4-methyl-phenyl) acide acétique). Ce composé a la capacité de former des liens très forts avec le fer (III) et ainsi de dissoudre les composés de fer. Même la rouille, FeOOH(s), forme des complexes solubles dans l’eau en solution alcaline avec EDMA et peut ainsi être évacuée en dehors du bois. En l’absence de fer, le soufre restant s’oxyde lentement et peut être contrôlé grâce à une atmosphère stable et des antioxydants.
Par-dessus tout, il est important d’évaluer l’efficacité du traitement, et l’analyse par les rayons X est un bon moyen de contrôler la procédure d’extraction du fer et l’enlèvement de composés soufrés spécifiques.
Les rayons X synchrotron
Dans un synchrotron, des électrons sont accélérés jusqu’à atteindre une énergie très élevée (six milliards d’électronvolts à l’ESRF – European Synchrotron Radiation Facility – en France). Ces électrons de très haute énergie sont ensuite injectés dans un anneau de stockage où ils circulent dans le vide à une vitesse proche de celle de la lumière. Les rayons X synchrotron, émis lorsque les électrons changent de direction dans des champs magnétiques élevés, sont dirigés vers les stations expérimentales qui entourent l’anneau de stockage.

Les rayons X produits par l’ESRF sont mille milliards de fois plus intenses que le faisceau produit par un générateur à rayons X à l’hôpital. Ainsi, ces faisceaux de lumière synchrotron très fins et très intenses peuvent être utilisés pour résoudre la structure de la matière avec une précision impossible à obtenir avec des rayons X standards. Les sources de lumière synchrotron peuvent être considérées comme des super-microscopes, et sont utilisées dans de nombreux domaines de recherche, dont les matériaux, l’archéologie, la biologie ou la physique.
Il y a environ 70 synchrotrons dans le monde. Des techniques variées, allant de la diffraction des rayons X à la diffusion aux petits angles, de la spectroscopie photoélectronique à l’absorption des rayons X sont mises à la disposition d’un nombre croissant de scientifiques. Ces techniques permettent l’étude de la matière à l’échelle microscopique, pour toutes sortes d’échantillons, cristallins, polymères, biologiques ou environnementaux, solides, liquides ou gazeux.
Les rayons X synchrotron sont utiles pour analyser les vaisseaux historiques naufragés, en déterminant les quantités, la localisation et l’état chimique des composés de soufre et de fer à l’échelle microscopique. Ainsi les chercheurs peuvent contrôler la détérioration du bois archéologique et améliorer les méthodes de conservation.
C’est pour cela que Magnus Sandström et son équipe de l’Université de Stockholm, en Suède, sont allés régulièrement depuis 2001 au Laboratoire de Rayonnement Synchrotron de Stanford en Californie (Etats-Unis). Ils se sont d’abord intéressés au Vasa, un bateau de guerre suédois du 17e siècle, dans lequel la formation d’acide sulfurique a été observée pour la première fois, puis ont étendu leur recherche à d’autres épaves historiques telles que le Mary Rose. L’année dernière, ils se sont réunis à l’ESRF pour réaliser des expériences complémentaires à celles menées à Stanford.
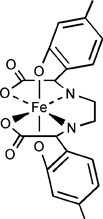
Comment extraire les composés de fer des épaves

noir du Vasa est plongé dans
une solution alcaline de
sodium-EDMA, les composés
de fer du bois se dissolvent
dans le complexe rouge sang
[FeIII-EDMA]-.
Image reproduite avec
l’aimable autorisation de Stefan
Evensen, Musée Vasa,
Stockholm, Suède
En travaillant sur le vaisseau de guerre suédois le Vasa, qui a sombré lors de sa première sortie en mer le 10 août 1628, les scientifiques ont eu l’idée de dissoudre les composés de fer présents dans le bois et de les retirer grâce à des complexes solubles dans l’eau. Le chélate appelé EDMA est en cours de tests. Le sel de sodium du complexe ferrique soluble, [Fe(III)-EDMA]-, est utilisé en grandes quantités en agriculture comme micronutriment en fer pour les plantes qui ne peuvent pas extraire le fer des sols alcalins, où le fer n’est pas soluble. Ces composés sont utilisés pour fertiliser les plantations d’orange en Espagne et pour faire pousser des citrons et des raisins en Italie et en France.
Questions de compréhension
Magnus Sandström
- Les poutres des coques du Vasa et du Mary Rose contiennent environ deux tonnes de soufre, sous forme de l’élément S. Si 1000 kg de soufre dans le bois étaient sous forme de pyrite, FeS2, combien d’acide sulfurique (H2SO4 (aq)) serait produit quand toute la pyrite serait complètement oxydée?
Deux réactions sont courantes, produisant: soit du sulfate de fer(II) hydraté:
FeS2(s) + 7/2O2 + (n+1)H2O → FeSO4·n(H2O)(s) + H2SO4(aq)
soit de la goethite, alpha-FeOOH (comme dans la rouille):
FeS2(s) + 15/4O2 + 5/2H2O → FeOOH(s) + 2H2SO4(aq)
- De l’hydrogénocarbonate de sodium (bicarbonate de sodium NaHCO3) a été ajouté à la solution que l’on vaporise sur le Mary Rose, afin que le pH reste autour de 7. De combien de bicarbonate de sodium aurait-on besoin pour neutraliser l’acide formé dans la question 1 (à partir de pyrite oxydée contenant 1000 kg de soufre)?
- La pyrite cristalline a un volume de 40 Å3 par unité de FeS2 mais elle prend beaucoup plus de volume lorsqu’elle est oxydée. Par exemple, le volume par unité de formule de la mélantérite (sulfate de fer II hydraté FeSO4·7(H2O)(s)) est 243,5 Å3 et de la rozénite (FeSO4·4(H2O)(s)) 162,7 Å3. La natrojarosite, NaFe3(SO4)2(OH)6, avec un volume de 266,0 Å3 par unité de formule, est aussi trouvée couramment dans le bois du Vasa.
Donnez une estimation de l’augmentation de volume lorsqu’un cristal de pyrite s’oxyde et que les sels suivants cristallisent : a) FeSO4·7(H2O)(s), b) FeSO4·4(H2O)(s) et c) NaFe3(SO4)2(OH)6. Quels effets auraient ces réactions si elles avaient lieu à l’intérieur de la structure du bois?
- Dans un livre de chimie, trouvez un diagramme schématique des niveaux d’énergie des orbitales moléculaires d’une molécule d’oxygène O2 dans son état fondamental. Expliquez comment un supplément d’énergie venant de la lumière peut produire l’oxygène 1O2, avec tous les électrons sous forme de paires.
Vous trouverez les réponses ici.
Resources
- Le Mary Rose peut être visité au Musée du Mary Rose à Portsmouth, au Royaume-Uni. Des informations concernant le navire, des documents pédagogiques et des détails sur les visites se trouvent sur le site web.
- Le Vasa est exposé dans le Musée Vasa à Stockholm, en Suède. Des détails sur l’histoire du Vasa, les recherches scientifiques en cours pour préserver le navire et comment visiter sont sur le site web.
- Le travail de recherche du Professeur Sandström et de son équipe pour préserver le Vasa et le Mary Rose est présenté sur son site.
- L’ESRF (European Synchrotron Radiation Facility) est un organisme international qui utilise, entretient, et développe la plus puissante source de lumière synchrotron en Europe, avec 18 pays participants. Plus de 5000 chercheurs viennent à l’ESRF chaque année pour utiliser la source de lumière et les instruments qui y sont liés.
Institutions
Review
Cet article devrait intéresser les professeurs de sciences mais aussi les professeurs d’histoire. Il devrait être utile aux professeurs qui souhaitent inclure dans leurs cours des exemples d’applications de la chimie et de la physique et qui veulent montrer à quoi peuvent servir ces sciences dans des situations inattendues. Il peut aussi servir de base pour les étudiants plus âgés qui auraient le désir d’approfondir les aspects scientifiques et historiques liés à ce sujet, grâce aux liens vers les sites internets cités.
J’ai moi-même apprécié cet article. Il m’a stimulé suffisamment pour que j’aie envie de suivre certaines des informations données.
Tim Harrison, Royaume-Uni





