Ένας ωκεανός στο σχολικό εργαστήριο: διοξείδιο του άνθρακα στη θάλασσα Teach article
Γνωρίζατε ότι το διοξείδιο του άνθρακα διαλύεται στο νερό και επηρεάζει τους ωκεανούς ; Ερευνήστε την επίδραση του διοξειδίου του άνθρακα στη χημεία των ωκεανών…
Η χημεία του διοξειδίου του άνθρακα στους ωκεανούς
Οι ωκεανοί διαδραματίζουν έναν σημαντικό ρόλο στην διαμόρφωση του κλίματος της Γης. Παρόλο που αποτελούν ένα πολυσύνθετο σύστημα, που συνδέουν μεταξύ τους όλα τα μέρη της υδρογείου, οι ωκεανοί υπακούουν σε απλούς κανόνες της φυσικής και της χημεία που μπορούν να αξιοποιηθούν για την ευαισθητοποίηση σχετικά με τη δυναμική των ωκεανών και τον αντίκτυπό τους στις ζωές μας.
Η αυξανόμενη συγκέντρωση του διοξειδίου του άνθρακα στην ατμόσφαιρα της Γης ως αποτέλεσμα των ανθρώπινων δραστηριοτήτων, για παράδειγμα η καύση ορυκτών καυσίμων (κύρια πηγή ανθρωπογενών εκπομπών διοξειδίου του άνθρακα), μεταβάλλει την ατμόσφαιρα και καθιστά τους ωκεανούς περισσότερο όξινους. Το ζήτημα της οξίνισης των ωκεανών συνδέεται φυσικά με ενότητες του αναλυτικού προγράμματος όπως τα οξέα και βάσεις, pH, ακόμα και με αντιδράσεις καταβύθισης.
Η βροχή είναι όξινη (pH περίπου 5.6) λόγω της διάλυσης του ατμοσφαιρικού διοξειδίου του άνθρακα και του σχηματισμού ανθρακικού οξέος :
Σε αντίθεση με τη βροχή, οι ωκεανοί είναι βασικοί (pH ελαφρώς πάνω από 8) καθώς περιέχουν ανθρακικά και όξινα ανθρακικά ιόντα. Οι ωκεανοί, επομένως, αποτελούν έναν σημαντικό αποθέτη του ανθρωπογενούς διοξειδίου του άνθρακα, το οποίο απομακρύνεται από την ατμόσφαιρα. Αυτό μπορεί να φαίνεται ως κάτι καλό, αλλά έχει ως αποτέλεσμα την μείωση του pH των ωκεανών και μεταβολές στη χημεία τους. Η οξίνιση των ωκεανών επηρεάζει τη διαθεσιμότητα των ανθρακικών ιόντων, σημαντικού συστατικού των οστράκων. Το διοξείδιο του άνθρακα διαλύεται στο νερό για να σχηματίσει ανθρακικό οξύ το οποίο αντιδρά με τα ανθρακικά ιόντα. Ως αποτέλεσμα, η ποσότητα των ανθρακικών ιόντων μειώνεται και των όξινων ανθρακικών ιόντων αυξάνεται :
1η Δραστηριότητα : Διοξείδιο του άνθρακα και pH του νερού – Μέρος Ι
Με το πείραμα αυτό θα δείξουμε πώς το διοξείδιο του άνθρακα αλλάζει το pH του νερού και γιατί η φυσική βροχή είναι όξινη. Οι αλλαγές του χρώματος του γενικού δείκτη καθιστά το πείραμα πιο ελκυστικό σε μικρότερους μαθητές.
Υλικά
- 2 Κωνικές φιάλες (100 cm3)
- Γλυκό νερό (40 cm3)
- Καλαμάκια
- Γενικός δείκτης ή δείκτη μπλε της βρωμοθυμόλης (5 με 7 σταγόνες)
Τα χρώματα των δεικτών φαίνονται στο σχήμα 1. Σε όλα τα σχήματα που ακολουθούν, έχει γίνει χρήση του δείκτη μπλε της βρωμοθυμόλης.

Gregor Trefalt/Wikimedia, CC BY-SA 4.0
Διαδικασία
- Οι μαθητές γεμίζουν τις φιάλες με 40 cm3 γλυκού νερού. Μπορεί να δοκιμάσετε τη δραστηριότητα με θαλασσινό νερό ή να ετοιμάσετε το δικό σας δείγμα διαλύοντας 3,5 g θαλασσινού αλατιού σε 100 cm3 νερού.
- Προσθέστε σταγόνες δείκτη pH σε κάθε μία από τις φιάλες και μετρήστε το pH.
- Στη μία φιάλη, φυσήξτε ελαφρά με ένα καλαμάκι αέρα στο νερό.
- Οι μαθητές παρατηρούν τις αλλαγές στο χρώμα (σχήμα 2) και καταγράφουν τις νέες τιμές pH.

Οι εικόνες είναι ευγενική προσφορά του Ole Ahlgren
2η Δραστηριότητα : Διοξείδιο του άνθρακα και pH του νερού – Μέρος ΙΙ
Το διοξείδιο του άνθρακα δεν διοχετεύεται στους ωκεανούς. Η επαφή ανάμεσα στους ωκεανούς και την ατμόσφαιρα είναι αρκετή ώστε το αέριο να διαλυθεί. Αυτό το πείραμα αποτελεί καλύτερη αναπαράσταση του τι συμβαίνει φυσικά στους ωκεανούς, με τα αποτελέσματα όμως να μην είναι αμέσως ορατά.
Υλικά
- Ποτήρι ζέσης των 250 cm3 με ελαστικό πώμα
- Κωνική φιάλη των 250 cm3
- 50 cm3 νερού βρύσης με 10 σταγόνες γενικού δείκτη ή μπλε της βρωμοθυμόλης
- 10 cm3 ξιδιού (οξικού οξέος)
- Μαγειρική σόδα (2 κουταλιές του γλυκού)
- Σπίρτα (προαιρετικά)
Διαδικασία
- Οι μαθητές προσθέτουν σιγά σιγά το ξίδι στη μαγειρική σόδα στην κωνική φιάλη (σχέδιο 3). Όταν σταματήσει ο αφρισμός, οι μαθητές ελέγχουν αν η φιάλη είναι γεμάτη διοξείδιο του άνθρακα τοποθετώντας στο εσωτερικό της ένα αναμμένο σπίρτο. Το σπίρτο θα σβήσει αμέσως λόγω της παρουσίας του CO2.
- Στη συνέχεια, οι μαθητές «αποχέουν» το αέριο σε ένα ποτήρι ζέσης, που περιέχει 50 cm3 νερού με δείκτη, και το κλείνουν με ένα ελαστικό πώμα.
- Το διοξείδιο του άνθρακα θα διαλυθεί σιγά σιγά στο νερό, διαδικασία που μπορεί να χρειαστεί έως και μία ημέρα για να παρατηρηθεί αλλαγή στο pH (σχέδιο 3).

Οι εικόνες είναι ευγενική προσφορά του Ole Ahlgren
3η Δραστηριότητα : Διοξείδιο του άνθρακα από την καύση ξύλου
Μία εναλλακτική της 2ης Δραστηριότητας περιλαμβάνει την καύση ενός κομματιού ξύλου, για παράδειγμα ενός σπίρτου, προκειμένου να παραχθεί διοξείδιο του άνθρακα πάνω από την επιφάνεια του νερού. Αυτό το σενάριο προσομοιάζει περισσότερο την καύση ορυκτών καυσίμων στην πραγματική ζωή και έχει παρόμοια αποτελέσματα.
Υλικά
- Κωνική φιάλη των 100 cm3 με ελαστικό πώμα
- 20 cm3 νερού βρύσης με περίπου 5 σταγόνες γενικού δείκτη
- Καλαμάκια
Διαδικασία
- Οι μαθητές μεταφέρουν στην κωνική φιάλη 20 cm3 νερού, στο οποίο έχουν προσθέσει σταγόνες του δείκτη και μετράνε το pH του.
- Οι μαθητές θα πρέπει να φορούν προστατευτικά γυαλιά. Ανάβουν ένα μικρό κομμάτι ξύλου και το εισάγουν ανεστραμμένο στην κωνική φιάλη (σχήμα 4) μέχρι η φλόγα να σβήσει λόγω της έλλειψης επαρκούς ποσότητας οξυγόνου που θα μπορούσε να διατηρήσει την καύση του ξύλου.
- Η φιάλη κλείνει με το πώμα και αναδεύεται για λίγα δευτερόλεπτα.
- Το χρώμα του δείκτη αλλάζει, και μετράται εκ νέου το pH του νερού (σχήμα 4).
- Κατά την ανάδευση της φιάλης, το CO2 απορροφάται ταχύτατα από το νερό. Σε κανονικές συνθήκες η διαδικασία πραγματοποιείται με αργό ρυθμό. Για να το επιβεβαιώσετε, επαναλάβατε τη διαδικασία, αυτή τη φορά χωρίς ανάδευση, και αφήστε τη φιάλη σε ηρεμία για αρκετές ώρες οπότε και θα παρατηρηθεί η αλλαγή του χρώματος εξαιτίας του απορροφημένου CO2.

Οι εικόνες είναι ευγενική προσφορά του Ole Ahlgren
Σημείωση για την ασφάλεια
Οι μαθητές θα πρέπει να φορούν προστατευτικά γυαλιά καθ’ όλη τη διάρκεια της δραστηριότητας.
4η Δραστηριότητα : Διοξείδιο του άνθρακα και ανθρακικά ιόντα
Αυτό το πείραμα θα δείξει ποσοτικά την ποσότητα ανθρακικών που είναι διαθέσιμα στο διάλυμα.
Το ανθρακικό ασβέστιο είναι αδιάλυτο στο νερό, σε αντίθεση προς το όξινο ανθρακικό ασβέστιο, που είναι πολύ ευδιάλυτο. Κατά την προσθήκη ιόντων ασβεστίου (με τη μορφή διαλύματος νιτρικού ασβεστίου) σε διάλυμα ανθρακικών ιόντων (με τη μορφή διαλύματος ανθρακικού νατρίου), θα παρατηρήσουμε το σχηματισμό λευκού ιζήματος ανθρακικού ασβεστίου, ενός από τα συστατικά των κοχυλιών. Με την μείωση του pH, θα παρατηρήσουμε πως η μεταβολή αυτή επηρεάζει τη διαθέσιμη ποσότητα των ανθρακικών στο διάλυμα μετρώντας την ποσότητα του ανθρακικού ασβεστίου που καταβυθίζεται.
Υλικά και αντιδραστήρια
- Na2CO3 (διάλυμα 0.05 mol/dm3 (0.52 g Na2CO3 σε 100 cm3 H2O)
- HNO3 (διάλυμα 1 mol/dm3)
- Ca(NO3)2 (διάλυμα 0.03 mol/dm3 (0.33 g Ca(NO3)2 σε 100 cm3 H2O))
- 3 δοκιμαστικοί σωλήνες
- pH-μετρο ή ταινίες μέτρησης pH
Διαδικασία
- Οι μαθητές προσθέτουν 5 cm3 διαλύματος Na2CO3 σε καθέναν από τους τρεις δοκιμαστικούς σωλήνες (Α, Β και C. Σχήμα 5).
- Προσθέτουν 10 σταγόνες ΗΝΟ3 στον δοκιμαστικό σωλήνα Α, 5 σταγόνες στον σωλήνα Β και καμία σταγόνα στον σωλήνα C (διάλυμα ελέγχου).
- Με το pH-μετρο ή ταινίες μέτρησης του pH μετράται το pH σε κάθε σωλήνα και στη συνέχει προστίθεται 1 cm3 διαλύματος Ca(NO3)2 (περίπου 25 σταγόνες) σε κάθε σωλήνα.
- Οι μαθητές παρατηρούν τα αποτελέσματα και καταλήγουν σε συμπεράσματα σχετικά με το ποιο διάλυμα περιέχει περισσότερα ανθρακικά ιόντα διαθέσιμα για το σχηματισμό ιζήματος.

Οι εικόνες είναι ευγενική προσφορά του Ole Ahlgren
Συζήτηση
Μπορεί κάποιος να εξηγήσει σε μικρότερους μαθητές τα αποτελέσματα απλούστερα λέγοντας ότι τα ανθρακικά ιόντα (CO32-), τα όξινα ανθρακικά ιόντα (HCO3–) και το ανθρακικό οξύ (H2CO3) διαλύθηκαν στο νερό. Το τελευταίο διασπάται σε νερό και διοξείδιο του άνθρακα. Η σχετική ποσότητα κάθε ουσίας εξαρτάται από το pH του διαλύματος. Στο διάλυμα με το χαμηλότερο pH, υπάρχουν λίγα ανθρακικά ιόντα και περισσότερο ανθρακικό οξύ, το οποίο διασπάται, και έτσι παρατηρούμε τον σχηματισμό διοξειδίου του άνθρακα. Σε μεγαλύτερους μαθητές τα αποτελέσματα μπορούν να ερμηνευθούν με τις ακόλουθες χημικές εξισώσεις, την έννοια της χημικής ισορροπίας και την αρχή Le Chatelier.
Μετά τη διάλυση CaCO3 στο νερό (διάλυμα με υψηλό pH) :
Μετά την προσθήκη ΗΝΟ3 :
Σε ένα πιο όξινο διάλυμα, η ισορροπία μετατοπίζεται προς τα δεξιά, και σύμφωνα με την αρχή Le Chatelier, λιγότερα είναι διαθέσιμα. Στον σωλήνα Α η ισορροπία μετατοπίζεται σχεδόν πλήρως προς τα δεξιά και έτσι παρατηρούμε τον σχηματισμό φυσαλίδων CO2.
Μετά την προσθήκη Ca(NO3)2 :
Το διάλυμα στο οποίο σχηματίζεται η μεγαλύτερη ποσότητα λευκού ιζήματος είναι αυτό με τη μεγαλύτερη ποσότητα διαθέσιμων ανθρακικών ιόντων. Σε αυτή την περίπτωση, πρόκειται για τον σωλήνα C, που περιέχει ανθρακικό νάτριο (pH = 11) και καθόλου νιτρικό οξύ (HNO3).
Οι επιπτώσεις στη ζωή στους ωκεανούς
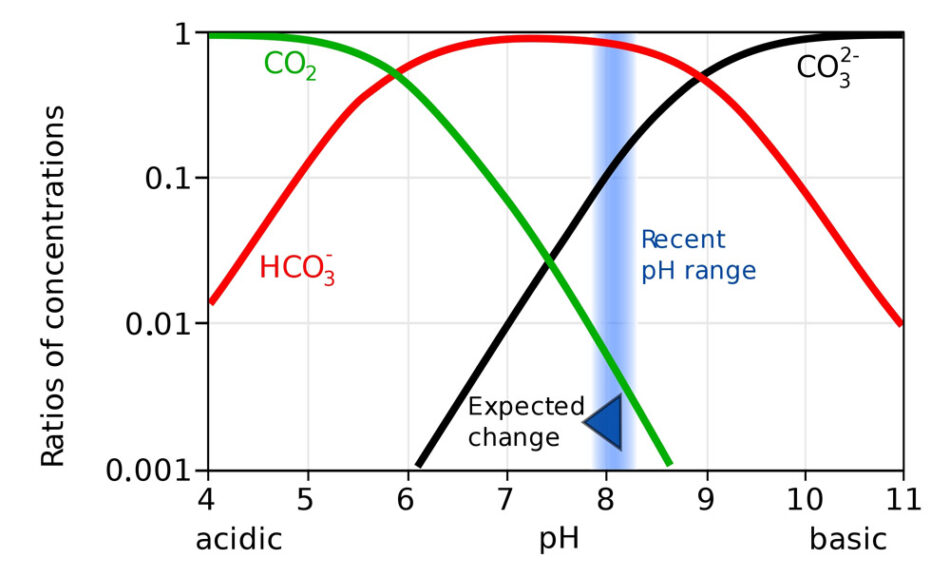
Η αύξηση της συγκέντρωσης του διοξειδίου του άνθρακα στην ατμόσφαιρα εξαιτίας των ανθρώπινων δραστηριοτήτων επηρεάζει τους ωκεανούς. Το 30 % περίπου αυτού του αερίου απορροφάται από τους ωκεανούς και ένα μέρος αυτού αντιδρά με το νερό και σχηματίζεται ανθρακικό οξύ. Αυτό το ασθενές οξύ ευθύνεται για την οξίνιση των ωκεανών. Ο όρος «οξίνιση των ωκεανών», παρ’ όλο που είναι σωστός, μπορεί να παραπλανήσει, δεδομένου ότι οι ωκεανοί είναι αλκαλικοί με το pH τους να κυμαίνεται στο 8,1 (σχήμα 6).[1]
Αν και οι ωκεανοί παραμένουν αλκαλικοί, μία μείωση του pH τους επηρεάζει τις βιοχημικές αντιδράσεις στους οργανισμούς και τον σχηματισμό ασβεστούχων θαλάσσιων οργανισμών.[2,3]
Γενικής χρήσης
Σύμφωνα με το σχήμα 6, καθώς το pH μειώνεται, μειώνεται και η ποσότητα των ανθρακικών ιόντων, που είναι διαθέσιμα. Τα ανθρακικά ιόντα μετατρέπονται σε όξινα ανθρακικά ιόντα και σε διοξείδιο του άνθρακα. Για αυτό τον λόγο στην 4η δραστηριότητα, στο pΗ 7, παρατηρείται ο σχηματισμός αερίου.
Ερωτήσεις προς τους μαθητές
- Γιατί στην 1η Δραστηριότητα το νερό αλλάζει χρώμα μόλις εμφυσούμε αέρα σε αυτό ;
- Πως το πείραμα στην 3η Δραστηριότητα αποτυπώνει μία από τις συνέπειες της καύσης των ορυκτών καυσίμων ;
- Εξηγήστε τη διαφορά μεταξύ των καταβυθίσεων στους τρεις δοκιμαστικούς σωλήνες της 4ης Δραστηριότητας στηριζόμενοι στα σχήματα 5 και 6.
- Μερικές φορές για να εξηγήσουμε τις επιπτώσεις της οξίνισης των ωκεανών βάζουμε κοχύλια σε ένα οξύ. Γιατί το πείραμα αυτό μπορεί να είναι παραπλανητικό ;
- Αν το pH των ωκεανών πέσει από το 8,1 σε 8,0, πόσο κατά προσέγγιση θα μειωθεί το ποσοστό των ανθρακικών ιόντων, σύμφωνα με το σχήμα 6 ;
References
[1] Άρθρο για την οξίνιση των ωκεανών από National Oceanic and Atmospheric Administration (NOAA): https://www.noaa.gov/education/resource-collections/ocean-coasts/ocean-acidification
[2] Μία έκθεση σχετικά με τις επιπτώσεις της οξίνισης των ωκεανών: https://worldoceanreview.com/en/wor-1/ocean-chemistry/acidification/
[3] Μία έκθεση για το πώς η κλιματική αλλαγή μεταβάλλει τη χημεία των ωκεανών: https://worldoceanreview.com/en/wor-1/ocean-chemistry/
Resources
- Δοκιμάστε περισσότερες δραστηριότητες σχετικές με τους ωκεανούς: Ribeiro C I, Ahlgren O (2021) An ocean in the school lab: rising sea levels. Science in School 53.
- Μάθετε περισσότερα για το πως η οξίνιση των ωκεανών επηρεάζει τη θαλάσσια ζωή: Korn A (2016) Opening seashells to reveal climate secrets. Science in School 35:12–14.
- Διαβάστε για τον ρόλο των ωκεανών μας στην κλιματική αλλαγή: Harrison T, Khan A, Shallcross D (2017) Climate change: why the oceans matter. Science in School 39: 12–15.
- Διερευνήστε άλλα πειράματα χημείας σχετικά με την κλιματική αλλαγή: Shallcross D, Harrison T (2008) Practical demonstrations to augment climate change lessons. Science in School 10:46–50.
- Διαβάστε για τον αντίκτυπο των ανθρώπινων δραστηριοτήτων στην κλιματική αλλαγή και τις συνέπειες τους στη Γη: Follows M (2019) Ten things that affect our climate. Science in School 47:19–25.
- Ανακαλύψτε πως οι συνέπειες της κλιματικής αλλαγής επηρεάζουν ήδη τις κοινότητες: Unwin H (2020) The social science of climate change. Science in School 49:18–22.
- Ανακαλύψτε πρακτικές δραστηριότητες στο Earth Learning Idea.
Review
Το διοξείδιο του άνθρακα και οι επιπτώσεις του σπάνια να μην πρωταγωνιστούν στις ειδήσεις. Σε αυτό τους το άρθρο, οι Ribeiro και Algren συγκεντρώνουν τρεις απλές δραστηριότητες για να υποστηρίξουν τη διδασκαλία της χημείας που σχετίζεται με την διάλυση του διοξειδίου του άνθρακα στους ωκεανούς του πλανήτη.
Μέσα από αυξανόμενη πολυπλοκότητα, οι συγγραφείς διερευνούν μία σειρά από σημαντικές ιδέες όπως : οι διαφορές στην οξύτητα ανάμεσα στο θαλασσινό και το πόσιμο νερό, η επίπτωση που έχει η διάλυση του διοξειδίου του άνθρακα στο pH και τελικά η μελέτη των ισορροπιών μεταξύ ανθρακικών και όξινων ανθρακικών ιόντων. Το τελικό πείραμα μπορεί να αποτελέσει το έναυσμα για συζητήσεις με πιο χαρισματικούς μαθητές σχετικά με την αρχή Le Chatelier. Τα πειράματα αυτά θα μπορούσαν να αποτελέσουν για τους δασκάλους ένα χρήσιμο συμπλήρωμα στην εξήγηση όλων εκείνων των θεωρητικών σημείων του αναλυτικού προγράμματος.
Δρ Chris Millington, Δάσκαλος Χημείας, Γυμνάσιο Oldham Hulme, Ηνωμένο Βασίλειο





