Jocul numerelor: extinderea tabelului periodic Understand article
Tradus de Mircea Băduţ. Până acum câteva secole, oamenii credeau că lumea este făcută numai din pământ, aer, apă şi foc. De atunci, cercetătorii au descoperit 118 elemente chimice şi acum se caută elementul 119.

Mikulak; sursa imaginii:
Wikimedia Commons
În epoca laboratoarelor spaţiale europene, cercetătorii se străduiesc să descopere noi elemente chimice. Dacă reuşesc, ei se vor înscrie în clubul oamenilor de ştiinţă care au rescris tabelul periodic.
Grecii antici s-au înşelat privind faptul că sunt doar patru elemente – pământ, aer, foc şi apă – dar au avut dreptate cu ceva: elementele sunt ingredientele a tot ceea ce ne înconjoară, legate între ele în compuşi şi amestecate împreună în diferite proporţii. În timp ce compuşii există într-o imensă varietate caleidoscopică, elementele sunt destul de simple, iar deocamdată există doar 118 elemente cunoscute ştiinţeiw1. Descoperirea unui element nou este o chestiune extraordinară.
Pentru imagine, multumim
Halfdan; sursa imaginii:
Wikimedia Commons
Atomii, cărămizile materiei, sunt compuşi cu toţii din aceleaşi componente simple: particule minuscule numite protoni şi neutroni, plus o serie de electroni şi mai mici orbitând în jurul lor. Numărul de protoni din atom – adică numărul său atomic – defineşte distinct elementul. Un atom de oxigen, de exemplu, are opt protoni, opt neutroni (de obicei) şi opt electroni, în timp ce elementele cele mai grele pot avea peste o sută din fiecare.
* * *
Chimistul rus Dmitri Mendeleev nu cunoştea acest lucru atunci când, în 1869, a aranjat elementele într-un tabel ordonându-le după masa lor atomică. El a observat rapid anumite modele evolutive aplicate repetitiv: în particular, coloanele grupau împreună elemente cu surprinzătoare proprietăţi similare. De exemplu, potasiul, rubidiul şi cesiul – trei metale ce reacţionează energic cu apa – sunt aşezate unul sub altul în tabel.
La început, tabelul lui Mendeleev avea o problemă: era plin de goluri. Între zinc şi arseniu, de exemplu, se părea că lipsesc două elemente. Dar savantul a prezis cu îndrăzneală că acele goluri vor fi umplute cu elemente noi, şi a folosit tabelul pentru a prognoza care vor fi proprietăţile acelor viitoare elemente. Şi a avut dreptate: lipsurile au fost umplute curând de galiu şi germaniu.

Mendeleev, publicat în 1869.
Faceți clic pe imagine pentru
a o mări.
Imagine din domeniul public;
sursa imaginii: Wikimedia
Commons
După câteva modificări şi rafinări, tabelul creat de Mendeleev a devenit ceea ce utilizăm astăzi: tabelul periodic al elementelor chimicew1, ceva atât de fundamental încât gândim neîncetat că el trebuia neapărat să fie inventat.
În deceniile următoare, chimiştii au concurat în a umple golurile rămase în tabel. Între timp ei au descoperit şi de ce tabelul periodic este atât de aplicabil: că rândurile şi coloanele reflectă modul în care electronii sunt aranjaţi pe orbite în elemente diferite, şi că electronii dictează multe dintre proprietăţile elementelor.
Ultimul gol din tabel a fost completat în 1945. Descoperise ştiinţa toate elementele? Paradoxal, răspunsul era şi da şi nu. Toate elementele care existau în mod natural pe Pământ erau cunoscute. Dar – şi acesta este un ‘dar’ mare – nu se putea nega că s-ar putea crea artificial noi elemente, etichetabile la capătul tabelului periodic, dincolo de elementul cu numărul 92, uraniul.

Imagine din domeniul public;
sursa imaginii: Wikimedia
Commons
Astfel, prin dezvoltarea cercetărilor atomice din ani 1940, odată cu completarea ultimelor goluri din tabel, o pleiadă de noi elemente create în laboratoare s-au alăturăt capătului de tabel periodic, aducându-ne astăzi la 118 elemente cunoscute. Nimeni nu ştie câte elemente ar mai putea fi descoperite.
Ceea ce, totuşi, se cunoaşte, este că sintetizarea de noi elemente va fi tot mai dificilă. Astăzi ai nevoie de cele mai avansate laboratoare din lume dacă vrei să ai şanse: soluţiile facile au fost toate găsite.
* * *
Cunoscut prin numele scrântitor-de-limbă, ununennium, elementul prezis, pe care o echipă internaţională încearcă astăzi să-l descopere, este probabil cel mai dificil.

119, savanţii intenţionează
să bombardeze atomii de
berkeliu cu un fascicul de
atomi de titaniu.
Imagine obţinută prin
amabilitatea stock photos
for free.com
Echipa, coordonată de Centrul GSI Helmholtz pentru Cercetarea Ionilor Grei (GSI Helmholtzzentrum für Schwerionenforschung), din Germania, şi implicând aproape 20 de centre de cercetare din întreaga lume, intenţionează să creeze elementul 119. Metoda lor sună amăgitor de simplu: un fascicul de atomi de titaniu (număr atomic 22) este trimis să ciocnească nişte atomi de berkeliu (97). Se unesce cei doi şi – evrika! – se obţine elementul 119.
Desigur, nu este uşor.
Mai întâi pentru că berkeliul, înalt radioactiv, nu există în natură: trebuie mai întâi creat într-un reactor nuclear. În plus, este de o dificultate grotească să striveşti împreună elementele.
a o mări.
Pentru imagine, multumim
shape; sursa imaginii:
Wikimedia Commons
„Crearea fasciculului intens de titaniu este extrem de dificilă. Pentru aceasta am folosit proceduri pe care dorim să le păstrăm confidenţiale,” explică profesorul Jon Petter Omtvedt, unul din membrii echipei. „Vom bombarda platoul cu o rază de un trilion [5 x 1012] de atomi de titaniu pe secundă. […] Probabilitatea de ciocnire directă [între atomi] este extrem de redusă. Când se întâmplă totuşi ca atomii să se ciocnească, de obicei ei sunt sfărâmaţi sau parţial distruşi prin coliziune. Totuşi, la câteva săptămâni sau luni, obţinem prin coliziune un atom complet.”

Profesorul Christoph
Düllmann şi Dr Alexander
Yakushev, membri ai echipei,
în faţa instalaţiei
experimentale. Cu ajutorul
unei particule acceleratoare,
ionii de titaniu sunt
acceleraţi până aproape de
viteza luminii, apoi ei trec
printr-un tub de argint
până la ţinta confecţionată
din atomi de berkeliu (în
caseta cu benzi galbene din
centru). Folosind trei magneţi
(casetele roşii din dreapta),
ionii de ununennium rezultaţi
sunt separaţi de alte
particule, după care sunt
conduşi în detector, unde va
fi înregistrată
descompunerea lor.
Pentru imagine, multumim G
Otto / GSI
Este ca şi când ai câştiga premiul cel mare la loterie cumpărând suficient de multe bilete ca să îţi garanteze câştigul. Este lent şi ineficient, dar este un joc de numere, şi până la urmă vei reuşi.
Însă mai este o problemă. Toate elementele grele sunt radioactive şi instabile: în timp atomii lor se divid în atomi mai uşori, emiţând radiaţie. Iar cele mai grele element descoperite se vădesc incredibil de instabile. Ununoctium (elementul 118) se descompune la câteva milisecunde după creare, iar ununennium probabil va trăi şi mai puţin.
Nu, nu sunt periculoşi – cantităţile de radiaţii sunt aşa de mici încât doza nu-i dăunătoare. Dar elementul pe care tocmai l-ai creat este dificil de studiat: nu-l poţi picura într-o eprubetă şi nici nu-l poţi încălzi într-un arzător Bunsen, deoarece vei obţiune doar câte un atom odată şi doar pentru o fracţiune de secundă.
Soluţia echipei este să creeze ununennium cu ajutorul unei particule-accelerator, apoi să îl trimită într-un detector şi să urmărească semnele martor ale dezintegrării nuceului de ununennium – radiaţia şi atomii în care se divide – mai degrabă decât să urmărească însuşi noul element.
Este o soluţie inteligentă, dar ea lasă nesatisfăcută una dintre ambiţiile echipei: cercetătorii ar dori să poată studia modul în care atomii acestor elemente exotice reacţiunează între ei. Dar probabil că asta nu va fi posibil, cel puţin nu utilizând vreo tehnologie pe care ne-o putem imagina astăzi.
Dar, dacă aveţi sarcina de a crea noi elemente chimice, înfruntând deci improbabilitatea câştigului de loterie, atunci cuvântul ‘imposibil’ ar putea suna ca o provocare…
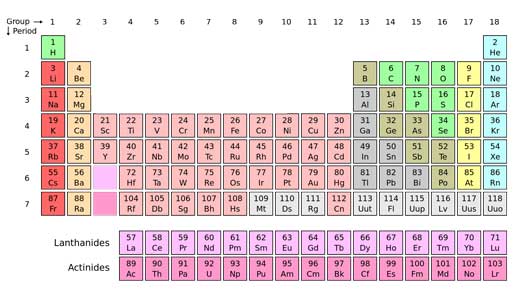
Pentru imagine, multumim NikNaks; sursa imaginii: Wikimedia Commons
Mulțumiri
Editorii revistei Science in School doresc să mulţumească profesorului Christoph Düllmann de la Centrul GSI Helmholtz pentru Cercetarea Ionilor Grei (GSI Helmholtz Centre for Heavy Ion Research) pentru ajutorul dat în realizarea acestui articol.
Web References
- w1 – International Union of Pure and Applied Chemistry (IUPAC – Uniunea Internaţională de Chimie Pură şi Aplicată) este organismul oficial care decide dacă un element nou a fost întradevăr descoperit. Tabelul periodic al IUPAC include toate elementele de la 1 la 112, precum şi elementele 114 şi 116. Elementele 113, 115, 117 şi 118 nu sunt oficial recunoscute de IUPAC, deşi în literatura ştiinţifică au fost făcute revendicări privind descoperirea lor.
Resources
- Două comunicate de presă de la Universitatea din Oslo, Norvegia, furnizează mai multe informaţii despre descoperirea elementului ununennium:
- Universitatea din Nottingham, Marea Britanie, a creat un web-site cu imagini video referitoare la fiecare dintre elementele tabelului periodic. Pentru o recenzie asupra web-site-ului vedeţi:
-
Walsh M (2012) Review of the Periodic Table of Videos website. Science in School 24.
-
- Web-site-ul Societăţii Regale de Chimie a Marii Britanie (Royal Society of Chemistry) oferă o versiune interactivă a tabelului periodic, cu toate cele 118 elemente cunoscute.
Review
După un scurt sumar asupra creării şi dezvoltării tabelului periodic al elementelor chimice, articolul ne introduce în cercetările actuale pentru descoperirea de noi elemente. El poate fi util în lecţiile de chimie şi fizică, şi în mod special la studierea chimiei nucleare, a fizicii atomului şi la istoria ştiinţei. Articolul poate fi folosit şi pentru a discuta metodele ştiinţifice, viteza progresului ştiinţific, dificultăţile întâmpinate de cercetători, şi utilitatea cercetării fundamentale.
Istoria ştiinţei este un subiect rar dezbătut în şcoală/liceu, şi poate fi foate util pentru a face ştiinţa mai plăcută, în special pentru elevii interesaţi mai mult de latura umanistă. Acest articol se poate folosi şi pentru a demonstra legăturile dintre ştiinţe şi umanitate/cultură.
Chestionar cu potenţial de aplicare:
- Câte elemente considerau grecii antici că există?
- Ce este numărul atomic?
- Câte elemente cuprinde astăzi tabelul periodic?
- Descrieţi metoda folosită de echipa de cercetători pentru a descoperii noi elemente. Care sunt problemele şi dificultăţile acestei metode?
Mireia Güell Serra, Spania





