Aprender bioquímica com bananas Teach article
Estas experiências simples e rápidas com um fruto muito apreciado ilustram alguns processos bioquímicos.
A banana é um dos frutos mais populares do mundo – o consumo anual ultrapassa 100 mil milhões. Além de um alimento muito apreciado por milhões de pessoas, é uma importante fonte de rendimento e de emprego, especialmente na América Latina.
As bananas pertencem ao género Musa, que inclui cerca de 70 espécies. No entanto, hoje em dia quase todas as bananas doces são de uma única variedade, Cavendish. São cultivadas por reprodução assexuada para serem geneticamente idênticas. Mas a perda de biodiversidade torna-as particularmente vulneráveis a ataques de parasitas, e há actualmente uma infecção por um fungo, Fusariumw1, que está muito disseminada e tem causado grandes perdas.
As bananas são um modelo útil para nos ajudar a compreender certos processos bioquímicos. Nestas actividades com bananas ilustram-se alguns aspectos da bioquímica: metabolismo do açúcar, armazenamento do amido, produção de melanina e principais componentes do aroma. As actividades são adequadas a estudantes do ensino básico e secundário de vários níveis diferentes.

Hanna_photo/Shutterstock.com
Actividade 1: Medição do conteúdo de açúcar com um refractómetro
Começa-se por apresentar aos alunos seis bananas de maturação diferente (bananas 1 a 6, tabela 1, numeradas por ordem crescente de grau de maturação). Qual será a banana mais doce? A maioria dos alunos vota na banana preta; terão acertado? De seguida faz-se um teste cego de degustação; as papilas gustativas acertaram? Para saber, os alunos medem o teor de açúcar nas bananas, por refractometria. A actividade dura cerca de 20 minutos.
Material
- Bananas com 6 graus de maturação (três bananas para cada um, 18 bananas no total)
- Refractómetro
- Garfo
- Tigela ou prato
- Pano macio humedecido
Procedimento
- Descasque a banana menos madura (banana 1 na tabela 1) e corte um pedaço com cerca de 3 cm de comprimento.
- Com um garfo, esmague a amostra até obter uma polpa semifluida.
- Aplique um pouco de polpa sobre o prisma do refractómetro. Feche de modo que a polpa se espalhe por toda a superfície do prisma sem criar bolhas de ar ou pontos secos.
- Oriente o refractómetro na direcção de uma fonte de luz natural e olhe pela ocular. Verá um campo circular com a graduação em grau Brix, ou seja, o número de gramas de sacarose por 100 gramas de amostra (1 g de sacarose/100 g de amostra = 1ºBrix). Pode ter de focar a ocular para ver a escala mais nitidamente.
- Registe numa tabela o teor de açúcar em ºBrix.
- Limpe cuidadosamente o refractómetro (a tampa e o prisma) com o pano húmido.
- Repita os passos 1 a 6 para as outras duas bananas com o mesmo grau de maturação. Calcule o valor médio da concentração de açúcar e registe-o na tabela (veja a tabela 1 e a figura 1).
- Repita os passos 1 a 8 com as bananas restantes. Fica assim com 18 valores individuais e 6 valores médios.
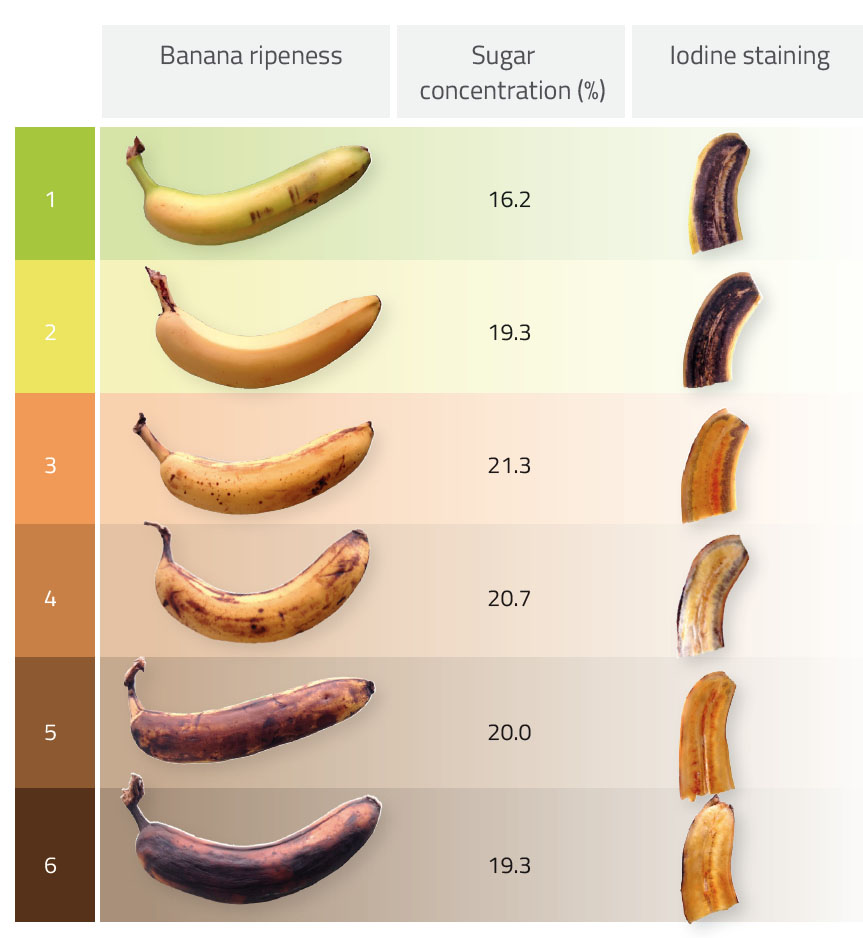
Jill Skarvan
Banana ripeness: Grau de maturação, Sugar concentration (%): Concentração de açúcar (%), Iodine staining: Coloração com iodo

Jill Skarvan
Sugar content (% Brix): Concentração de açúcar (ºBrix), Degree of ripeness: Grau de maturação
Actividade 2: Análise de amido com iodo
Testa-se a presença de amido em diferentes bananas, com solução de Lugol, e verifica-se que a quantidade de amido diminui durante o amadurecimento. Esta actividade demora cerca de dez minutos.
Material
- Bananas com 6 graus de maturação (três bananas para cada um, 18 bananas no total)
- Solução de Lugol (KI3): 2% iodeto de potássio (KI), 1% iodo (I2), em água
- Faca de cozinha
- Pincel
Procedimento
- Corte as bananas ao meio longitudinalmente.
- Com um pincel, cubra a superfície das bananas com solução de Lugol.
- Após um minuto compare os resultados e registe-os. (veja a tabela 1).
Discussão
No processo de amadurecimento, enzimas denominadas amilases catalisam a degradação do amido, um polissacarídeo, em açúcares simples; primeiro forma-se maltose, um dissacarídeo, e depois glucose, um monossacarídeo. A tabela 1 mostra que a banana com maior teor de açúcar (na forma de monossacarídeos e dissacarídeos) é a banana 3. Com mais tempo de maturação o teor de açúcar começa a diminuir porque a maior parte do amido foi convertida em açúcares simples e a banana continua a usar glucose para a respiração celular.
Este fenómeno pode ser demonstrado pela reacção com a solução de Lugol: as bananas mais verdes têm um teor de amido superior ao das bananas maduras, evidenciado por uma coloração mais escura. Com o amadurecimento, o teor de amido diminui, e por conseguinte a coloração devida à reacção de amido com iodo também diminui.
No ensaio de degustação cego, os alunos podem não identificar correctamente a banana mais rica em açúcar. Outros factores, como, por exemplo, a maciez da banana e o seu teor de água, podem influenciar o sabor. Além disso, como a saliva também contém amilase, os alimentos ricos em amido e pobres em açúcar começam a ter um sabor adocicado após a mastigação, pois a amilase decompõe parte do amido em açúcar.
Exemplos de questões para discutir com os alunos:
- Qual é a banana mais doce?
- Porque é que o teor de açúcar aumenta no início do processo de amadurecimento, mas diminui na fase final?
- Como varia o conteúdo de amido durante o amadurecimento?
- As bananas mais verdes são mais ricas ou menos ricas em amido do que as mais maduras? A que se deve a diferença?
- A doçura só depende do teor de açúcar ou há outros factores em causa?
Actividade 3: Localização dos organelos de armazenamento de amido
Nesta actividade, os alunos preparam amostras de polpa de bananas com diferentes graus de maturação para observação ao microscópio, identificam os organelos celulares de armazenamento de amido (amiloplastos) e verificam que eles desaparecem com o amadurecimento. A experiência demora cerca de 15 minutos.
Material

polpa de banana para
observação ao microscópio
Samuel Ginsburg
- Polpa de bananas da actividade 1 (por ex. bananas 1 e 6, tabela 1)
- Solução de Lugol
- Microscópio
- Lâminas
- Lamelas
Procedimento
- Coloque uma pequena porção de polpa de banana na lâmina para microscópio e adicione uma gota de solução de Lugol (figura 2).
- Coloque a lamela cuidadosamente. Localize os organelos que armazenam amido, com ampliação 100x e 400x.
- Repita os passos 1 a 3 com a outra amostra de polpa de banana.
Discussão
Os amiloplastos são responsáveis pela síntese e armazenamento dos grãos de amido, por polimerização de glucose. Nas bananas verdes, amido e amiloplastos adquirem cor violeta intensa quando se adiciona solução de Lugol (figura 3). Nas bananas mais maduras a quantidade de amido é reduzida e já não há amiloplastos (figura 4).
Exemplos de questões para discutir com os alunos:
- Qual é a função do iodo nesta experiência?
- Como se chama o organelo que armazena amido em plantas?
- Que diferenças observou entre estes organelos das duas amostras e porquê?

Samuel Ginsburg

Samuel Ginsburg
Actividade 4: Escurecimento de bananas

água muito quente a casca de
banana fica escura devido à
produção de melanina.
Sacha Glardon
Nesta actividade, de cerca de 5 minutos, os alunos verificam que a casca de bananas mergulhadas em água quente escurece rapidamente, devido à produção de melanina.
Material
- Banana amarela (por ex., banana 2 da tabela 1)
- Copo de 1 L com água acabada de ferver
Procedimento
- Mergulhe metade da banana na água quente.
- Após cerca de 1 minuto a metade submersa fica escura (figura 5).
Discussão
Quando se mergulha uma banana em água quente, as suas células são danificadas pelo calor e produz-se melanina, um pigmento que escurece a casca. A melanina forma-se por oxidação do aminoácido tirosina, que é catalisada por uma enzima chamada tirosinase. Quando as células de banana são danificadas, há libertação de tirosinase. A produção de melanina não afecta o processo de amadurecimento, mas as bananas maduras são em geral mais escuras porque, sendo mais velhas, sofreram mais danos celulares. Em plantas e animais, a melanina protege as células externas dos danos causados pelos raios ultravioleta e “neutraliza” radicais livres devido às suas propriedades antioxidantes.
Discuta as questões seguintes com os seus alunos:
- Porque é que a banana fica escura?
- Qual é o composto que confere essa cor?
- A introdução da banana em água a ferver acelera o amadurecimento?
- Qual é a diferença entre uma banana que foi introduzida em água quente e uma banana que ficou escura naturalmente?
Actividade 5: Produção de aroma de banana artificial
Esta actividade, de síntese de aromas artificiais, é adequada a estudantes do ensino secundário. Partindo de 2-metil-1-butanol sintetiza-se acetato de isoamilo (acetato de isopentilo, acetato de 3-metilbutilo), que tem aroma de banana e pêra. E a partir de 1-pentanol sintetiza-se acetato de amilo (acetato de pentilo), com aroma de banana e maçã. A actividade demora cerca de 15 minutos. Pode dividir-se a turma em dois grupos: um grupo sintetiza acetato de isoamilo, o outro sintetiza acetato de amilo, e depois comparam os aromas.
Material
- Ácido acético (CH3COOH)
- 2-metil-1-butanol (C5H12O, CH3 CH2 CH CH3CH2OH)
- 1-pentanol (C5H12O, CH3 CH2 CH2 CH2 CH2OH)
- Ácido sulfúrico (H2SO4)
- Reguladores de ebulição
- Bico de Bunsen
- Tubo de ensaio
- Copo de 500 mL
Nota de segurança
Esta experiência envolve o uso de ácido sulfúrico e aquecimento. Deve por isso ser realizada no nicho, com óculos de segurança e luvas. Os alunos devem seguir as regras de segurança para as aulas laboratoriais de química. Como em qualquer experiência de química, não devem provar os compostos. Ver também as normas de segurança.
Procedimento
- Pipete 2 mL de ácido acético para um tubo de ensaio.
- Adicione 2 mL de 2-metil-1-butanol ou de 1-pentanol.
- Agite um pouco para homogeneizar e adicione uma gota de ácido sulfúrico.
- Adicione 1 ou 2 reguladores de ebulição e aqueça a mistura no bico de Bunsen durante cerca de dois minutos, sem deixar ferver. Aponte a abertura do tubo de ensaio para onde não haja ninguém.
- Transfira o conteúdo do tubo de ensaio para um copo de 500 mL e sinta o aroma.
Discussão
O aroma artificial de banana tem como principal componente acetato de isoamilo, e em geral também contém acetato de amilo. Mas sabemos que os fabricantes de aromas mantêm quase sempre as suas receitas exactas em segredo. O acetato de isoamilo e o acetato de amilo são ésteres produzidos por condensação de ácido acético com 2-metil-1-butanol e 1-pentanol, respectivamente. Estas reacções de esterificação são catalisadas por ácido sulfúrico (figura 6). Tal como acontece com todos os frutos, o aroma natural da banana é uma mistura de muitos componentes w2, por isso é difícil obter aromas artificiais que igualem o aroma natural.
Discuta as questões seguintes com os seus alunos:
- A que cheiram os produtos das reacções?
- Qual é o principal componente do aroma da banana?
- Qual é a diferença entre aromas naturais e artificiais e porque têm cheiros diferentes?

Sacha Glardon
Acetic acid: Ácido acético, 2-methyl-1-butanol: 2-metil-1-butanol, Isoamyl acetate: Acetato de isoamilo, 1-pentanol: 1-pentanol, Amyl acetate: Acetato de amilo
Outras actividades: descobrir mais sobre bananas
Há muitas outras experiências que pode fazer para aprender mais sobre a biologia e a química das bananas, ou para actividades interdisciplinares. Por exemplo:
- IsolarADN de banana. Todos os organismos vivos contêm ADN.
- Demonstrar a respiração celular colocando uma banana num recipiente hermeticamente fechado e mostrando que as concentrações de CO2 e O2 variam com o tempo.
- Medir o nível de açúcar no sangue de 15 em 15 min após comer uma banana (se for permitido fazer análise de sangue), para saber mais sobre o metabolismo do amido e o seu efeito sobre os níveis de açúcar no sangue e o armazenamento de glicogénio no fígado.
- Aprender um pouco sobre a importância da biodiversidade nos surtos de doenças.
- Explorar os aspectos históricos, económicos e éticos do comércio de bananas.
Web References
- w1 – Uma doença devastadora que afecta actualmente as bananas é causada pelo fungo Fusarium. Para saber mais, consulte o website of the United Nations’ Food and Agriculture Organization.
- w2 – James Kennedy, professor de química na Austrália, criou um gráfico divertido que mostra a lista de ingredientes das bananas: ‘all natural banana’.
Resources
- Visite o Banana Link website para saber mais sobre a produção e comércio de bananas.
- Veja este vídeo da National Geographic sobre a história das bananas.
Institutions
Science on StageReview
Este artigo descreve experiências simples com bananas para ilustrar alguns processos metabólicos básicos. Por exemplo, o processo de amadurecimento (e as consequentes mudanças de cor e de doçura) é usado para ilustrar a conversão do amido em maltose e glucose. Os alunos devem saber a diferença entre açúcares simples e complexos. Para tirar o máximo partido destas actividades o professor pode usar as perguntas sugeridas.
Monica Menesini, professora de ciências do ensino secundário (aposentada), Itália





