De que são feitas as estrelas? Teach article
Traduzido por Pedro Augusto. Descubra como sabemos de que é feito o Sol (e as estrelas).
Ao contrário de componentes do Sistema Solar como planetas e satélites, as estrelas estão fora do alcance de naves espaciais ou, no caso do Sol, quentes demais para uma aproximação. Sendo assim, como conseguimos compreendê-las se não conseguimos usar sondas, rovers ou astronautas para as estudar? A resposta está no uso da sua luz. Sabemos que a cor de uma estrela nos dá a sua temperatura (Ribeiro, 2015), mas como sabemos a composição das estrelas? Mais uma vez a luz estelar ou, mais especificamente, o espetro estelar é a resposta.
No festival Science on Stage que teve lugar em Londres em junho de 2015, surgiu entre nós uma conversa sobre a combinação de experiências hands-on com o ensino a propósito da composição química de uma estrela. Assim nasceu a ideia para esta atividade. Esta está desenhada para permitir que alunos de 15-18 anos explorem diferentes espetros de luz e compreendam como estes podem ser utilizados para identificar componentes químicos em lâmpadas e, mais importante, na nossa estrela mais próxima, o Sol.
Espetro da luz
Na sua famosa experiência de 1666, Isaac Newton utilizou um prisma para demonstrar que a luz poderia ser separada em cores componentes e que essas cores poderiam ser recombinadas para gerar luz branca. Newton demonstrou que as cores não tiveram origem no cristal usado, como antes se pensava, mas que, em vez disso, eram componentes (ou comprimentos de onda) da luz solar. Introduziu a palavra “espetro” para descrever o arco-íris de cores e a sua descoberta lançou a ciência da espetroscopia.

Para Newton o espetro solar parecia contínuo, sem falhas entre as cores. Mas em 1814 Joseph von Fraunhofer descobriu que quando a luz era dispersa o suficiente através de uma fenda estreita, o espetro continha um certo número de riscas escuras, agora conhecidas por riscas de Fraunhofer (figura 1). Cerca de 45 anos mais tarde estas riscas provaram ser essenciais na determinação da composição do Sol, graças ao trabalho de Gustav Kirchhoff e Robert Bunsen.
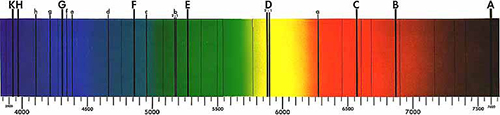
Imagem do domínio público. Fonte: Wikimedia Commons
Em 1860, Kirchhoff e Bunsen estudaram um diferente tipo de espetro. Em vez de observarem riscas escuras contra um fundo branco, estudaram riscas brilhantes contra um fundo escuro, emitidas quando aqueciam elementos na chama de gás de Bunsen. Um desses espetros era o do sódio (figura 2), que pode ser obtido na queima de sal de mesa (NaCl) ou acendendo uma lâmpada de sódio de baixa pressão, como aquelas utilizadas nas luzes da rua.
Bunsen e Kirchhoff concluiram que os elementos químicos poderiam ser identificados usando estas riscas de emissão e, tendo isso em conta, descobriram dois novos elementos nos dois anos seguintes: o césio e o rubídio.
Kirchhoff continuou o seu trabalho e apercebeu-se que as riscas de emissão coincidiam com várias riscas de Fraunhofer. Por exemplo, a risca amarela brilhante do espetro do sódio estava na mesma posição da risca escura na região amarela do espetro solar, designada como ‘D’ por Fraunhofer.

Imagem do domínio público. Fonte: Wikimedia Commons
Estas experiências iniciais revelaram três tipos principais de espetro: contínuo, de absorção e de emissão. O primeiro mostra todos os comprimentos de onda, o segundo contém apenas alguns dos comprimentos de onda da luz e o terceiro mostra falhas, ou riscas escuras, contra um fundo brilhante. Estes espetros formam-se de acordo com as três leis da espetroscopia de Kirchhoff:
- Um espetro continuo é emitido por um sólido, líquido ou gás incandescente sob alta pressão.
- Um espetro de absorção forma-se quando um espetro contínuo passa através de um gás frio de baixa densidade.
- Um espetro de emissão é criado por um gás quente a baixa pressão.
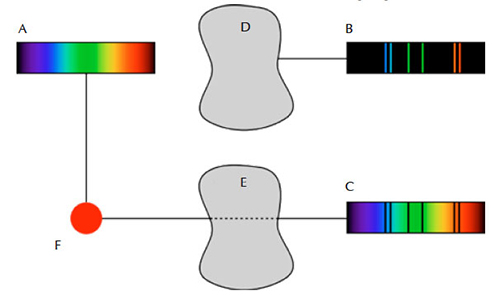
Imagem do domínio público. Fonte: Wikimedia Commons
Kirchhoff descobriu, não só, que um dado elemento químico era responsável pelas riscas espetrais na mesma posição quer em espetros de emissão quer de absorção, mas também descobriu que o Sol contém sódio. Assim, para sabermos a composição do Sol ou de qualquer outra estrela apenas precisamos de comparar o espetro de elementos conhecidos com o espetro da estrela.
Registando espetros de diferentes fontes de luz
Materiais
- Várias fontes de luz (tais como lâmpadas incandescentes, fluorescentes, de rua e luzes de néon).
- Espetrómetros – construídos utilizando uma caixa de cereaisw1 (ver a caixa de atividades na sala de aula) ou comprando e montando um kit de mini-espetrómetro extensível (disponível onlinew2).
- Espetros de emissão de diferentes elementos – imagens adequadas podem ser encontradas em livros ou descarregadas da Internetw3.
Construindo um espetrómetro
Materiais
- Caixa de cereais
- Papel grosso
- CD
- Tesoura
- Fita adesiva escura
Procedimento
- Num dos lados estreitos da caixa fazer um corte de forma a formar uma fenda horizontal. Para que a linha fique direita, pode ser utilizada fita adesiva para prender dois pequenos pedaços de papel grosso muito próximos, deixando uma pequena fenda entre eles. O espaço ideal é de 0.2mm.
- Cortar o CD a meio utilizando a tesoura. No lado oposto à fenda, cortar outra linha horizontal. Prolongar esta linha para além dos cantos da caixa em cada um dos lados de forma a que o CD encaixe na fenda fazendo um ângulo de 60º com o fundo da caixa.
- Cortar um buraco no topo da caixa, através do qual o CD pode ser visto.
- Excluir qualquer entrada indesejada de luz na caixa cobrindo as extremidades do CD com a fita escura.
Para mais informações sobre como construir este espetrómetro, clicar aqui.
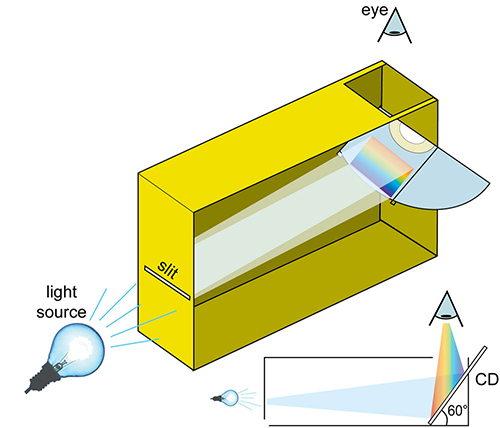
A imagem é cortesia de Mark Tiele Westra
Uma opção alternativa é utilizar o mini-espetrómetro extensível, disponível para compra onlinew2. Permite aos alunos fotografar o espetro observado utilizando um smartphone.
Nota de segurança
Não olhar diretamente para o Sol, mesmo com um espetrómetro. Em vez disso, apontar o espetrómetro para o céu para observar o espetro da luz do Sol difusa.
Procedimento
Comparando espetros
Pedir aos alunos para observarem a luz das várias fontes luminosas através de um espetrómetro. Isto vai mostrar-lhes que nem todas as fontes de luz são iguais, uma vez que o seu espetro não é igual.
Questões:
- Que tipo de espetro é emitido por cada fonte de luz?
- Que nos diz isso sobre o tipo de fonte de luz?
- Que tipo de fonte de luz é mais utilizado e porquê?
Explicação:
Os alunos vão observar um espetro diferente dependendo da fonte de luz:
- Uma lâmpada incandescente emite um espetro contínuo com todas as cores do visível presentes.
- Uma lâmpada de descarga de gás tipicamente contém hélio (He), néon (Ne), árgon (Ar), kripton (Kr) e xénon (Xe) (figura 3). Cada gás emite o seu próprio espetro de emissão.
- As luzes da rua usualmente contêm sódio e por isso emitem o espetro de emissão deste elemento.
- O espetro emitido por uma lâmpada LED depende do material semicondutor deste. Um LED azul cria um espetro contínuo com uma zona azul mais brilhante no espetro.
- O Sol emite um espetro contínuo. Um espetrómetro mais sofisticado mostra as riscas de absorção escuras causadas pelos elementos através dos quais a luz passa na atmosfera solar.
Espetros diferentes indicam que estas fontes de luz são diferentes, bem como o mecanismo por trás da sua formação, exceto para o Sol e para a lâmpada incandescente. A luz mais frequentemente utilizada é a incandescente por ter um espetro contínuo semelhante ao do Sol.
Analisando espetros de emissão
Utilizando diferentes lâmpadas de descarga de gás, pedir aos alunos para que identifiquem os elementos presentes ao compararem o espetro de cada lâmpada com imagens imprimidas dos espetros de emissão de diferentes elementos. Esta é a base da espetroscopia como um método de análise química.
Nota de segurança
As lâmpadas de descarga de gás precisam de altas voltagens pelo que devem ser manuseadas pelo professor.

A imagem é cortesia de Heinrich Pniok; fonte: Wikimedia Commons
Questões:

mini-espetrómetro
extensível para onter o
espetro de emissão do hélio.
A imagem é cortesia de Ole
Ahlgren
- Têm todas as riscas espetrais a mesma intensidade?
- Qual é a relação entre as riscas espetrais e a cor de uma lâmpada?
- Como podem os espetros ser utilizados para identificar diferentes elementos químicos?
Explicação:
Alguns comprimentos de onda são mais intensos do que outros, o que resulta em algumas riscas de emissão serem mais brilhantes do que outras. Isto vê-se pela cor da lâmpada. Por exemplo, a luz da lâmpada de sódio é amarelada por emitir principalmente luz amarela, apesar de também emitir luz vermelha e verde. Uma vez que cada elemento tem o seu comprimento de onda específico, podem-se utilizar espetros para identificar quais os elementos químicos presentes.
Atividade de extensão
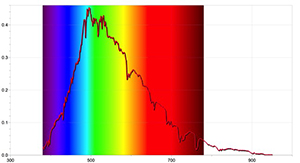
Para se obterem resultados mais detalhados, outras atividades podem ser feitas com um espetrómetro capaz de detetar as riscas de absorção do Sol e utilizando software de data–logger apropriado. As Figuras 4 e 5 foram obtidas utilizando o espetrómetro Red Tide da Ocean Optics e o programa LoggerPro.
Os espetros obtidos são diferentes dos recolhidos com um espetro simples pois contêm mais informação, incluindo o comprimento de onda de cada risca espetral e a sua intensidade relativa. O espetro solar pode também mostrar que a presença de um espetro de absorção não quer dizer que alguns comprimentos de onda da luz faltem totalmente; apenas que são menos intensos do que outros comprimentos de onda.
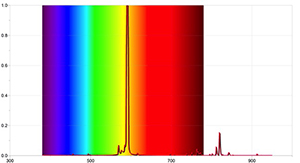
A imagem é cortesia de Ole Ahlgren
A imagem é cortesia de Ole Ahlgren

mercúrio com o espetrómetro
Red Tide da Ocean Optics e
com o programa Logger Pro.
A imagem é cortesia de Ole
Ahlgren
Materiais
Procedimento
Os alunos podem registar o espetro do Sol utilizando um espetrómetro mais sofisticado. O programa de data-logger dará o comprimento de onda de cada risca de absorção escolhida pelos alunos. Estas devem ser as mais proeminentes. De forma a determinar os elementos presentes, há duas hipóteses:
- Os alunos comparam cada comprimento de onda com os que constam numa tabela, como a que está disponível na página do Columbus Optical SETI Observatoryw6.
- Os alunos registam o espetro de emissão de vários elementos e depois comparam os comprimentos de onda das riscas com os das do Sol. O número de elementos que pode ser utilizado está limitado aos presentes em lâmpadas de descarga de gás. É possível queimar metais e obter o espetro de emissão, mas existirão riscas de outros elementos. Por exemplo, as riscas mais proeminentes ilustradas na figura 6 quando se queima magnésio são devidas à presença de azoto.

A imagem é cortesia de Ole Ahlgren
Tirando espetros de diferentes fontes de luz e elementos químicos e comparando-os com o espetro do Sol, os alunos aprendem como podemos determinar a composição do Sol e de outras estrelas.
References
- Ribeiro C (2015) Starlight inside a light bulb. Science in School 31: 37–42.
Web References
- w1 – Para instruções de como construir um espetrómetro utilizando uma caixa de cereais, ver:
- Westra M (2007) Uma nova visão da luz: construa o seu próprio espectrómetro. Science in School 4.
- w2 – É possível encomendar online um kit mini-espetrómetro extensível da Public Laboratory store.
- w3 – O espetro de emissão de vários elementos pode ser descarregado do Open Discovery Space.
- w4 – Exemplos de espetrómetros adequados para utilizar na extensão desta atividade podem ser encontrados aqui.
- w5 – O LoggerPro é um software premiado para recolha e processamento de dados para Windows e Mac.
- w6 – Riscas de Fraunhofer e os seus comprimentos de onda podem ser vistos no site do Columbus Optical SETI Observatory.
Resources
- Para um panorama das utilizações práticas da luz, ver:
- Douglas P, Garley M (2010) Chemistry and light. Science in School 14: 63-68.
- Science on Stage é uma rede europeia para professores de ciência, tecnologia, engenharia e matemática (STEM), inicialmente lançada em 1999 pelo EIROforum, o publicador do Science in School. O Science on Stage junta professores de toda a Europa para troca de ideias e melhores práticas de ensino com colegas entusiastas de 25 países.
Institutions
Science on StageReview
Neste artigo os autores descrevem sumariamente como se descobriram os espetros e como diferentes tipos destes podem ser utilizados para identificar de que são feitas as estrelas.
Eles também mostram como podem ser construídos e utilizados para medições espetrais, espetrómetros “faça você mesmo”. Esta atividade de ensino pode fornecer resultados fascinantes utilizando esses espetrómetros.
Questões de compreensão sobre o tópico podem ser as seguintes:
- Como descobriu Newton o espetro da luz?
- Que cores estão incluídas no espetro da luz?
- Em que cores começa e acaba o espetro visível?
- Descreve as descobertas de Bunsen e Kirchhoff.
Gerd Vogt, Escola Secundária para o Ambiente e a Economia (HLUW), Yspertal, Austria





