Wykrywanie cukrów: codzienny problem w obliczu cukrzycy Teach article
Tłumaczenie: Katarzyna Mleczko-Sanecka. Fred Engelbrecht i Thomas Wendt z Laboratorium Szkoleniowego ExploHeidelberg opisują doświadczenia związane z detekcją cukrów, ukazując tym samym problemy, którym chorzy na cukrzycę muszą stawiać czoła każdego dnia.
Cukrzyca, współczesna choroba cywilizacyjna
Glukoza, będąca cukrem prostym, stanowi najważniejsze źródło energii dla wszystkich organizmów eukariotycznych i wykorzystywana jest przez komórki zarówno w oddychaniu tlenowym jak i beztlenowym. Jest ona również prekursorem w procesie syntezy białek, a także w metabolizmie tłuszczów. Glukoza jest zatem jedną z kluczowych molekuł w wielu szlakach metabolicznych i w związku z tym jej stężenie we krwi musi być ściśle regulowane na drodze hormonalnej przez insulinę i glukagon.
Cukrzyca (łac. diabetes mellitus) to schorzenie charakteryzujące się zaburzeniem metabolizmu glukozy, objawiające się wysokim poziomem cukru we krwi (hyperglikemią). Przyczyną choroby jest brak lub niedobór insuliny bądź oporność komórek na jej działanie. W przypadku insulinooporności również wydzielanie hormonu jest przeważnie zaburzone, co nie pozwala przezwyciężyć niewrażliwości tkanek.
Wyróżniamy dwie główne formy cukrzycy: typu pierwszego i typu drugiego. Chociaż schorzenia te mają różne przyczyny, w obu przypadkach u osób chorych komórki beta trzustki nie produkują wystarczających ilości insuliny, aby zapobiec hyperglikemii.
Cukrzyca typu pierwszego stanowi około 10% wszystkich przypadków cukrzycy w Europie i charakteryzuje się utratą komórek beta trzustki, zwykle na drodze reakcji autoimmunologicznej. Z racji tego, że choroba ta rozwija się już u osób w młodym wieku, często nazywana jest cukrzycą młodzieńczą. Jest to również najcięższa postać choroby, ponieważ niedostępna jest skuteczna metoda jej leczenia. Schorzenie to wymusza na pacjentach odpowiednie dostosowanie stylu życia, poprzez poprawę diety, regularne wykonywanie ćwiczeń fizycznych oraz ciągłą kontrolę poziomu cukru. Ponadto, chorzy muszą otrzymywać podskórne zastrzyki lub przyjmować insulinę do krwiobiegu za pomocą specjalnej pompy, aby zapobiec śpiączce, a nawet śmierci.
Cukrzyca typu drugiego spowodowana jest opornością lub zmniejszoną wrażliwością tkanek na działanie insuliny, czemu zwykle towarzyszy niedostateczne wydzielanie hormonu. W większości przypadków obniżona odpowiedź tkanek na insulinę związana jest z zaburzoną aktywnością receptorów insulinowych na komórkach docelowych. W konsekwencji, aby utrzymać prawidłowe stężenie cukru we krwi, zapotrzebowanie na insulinę w całym organizmie jest nadmiernie podwyższone. Choroba rozwija się, gdy komórki beta trzustki nie są w stanie sprostać wymaganiom ze strony tkanek. Cukrzyca typu drugiego, zwana również cukrzycą dorosłych, przeważnie pojawia się u osób w wieku powyżej 30 lat. Bardzo często powiązana jest z otyłością i małą ilością ruchu. W związku z tym zdrowszy tryb życia może przyczynić się do poprawy stanu zdrowia pacjentów, a nawet do ich całkowitego wyleczenia. Aby dowiedzieć się więcej o cukrzycy, można sięgnąć po artykuł zamieszczony w pierwszym numerze Science in School, Dugi (2006) K. “Cukrzyca”.
Ludzie dotknięci każdym z typów cukrzycy muszą nauczyć się, jak na co dzień żyć z jej objawami, takimi jak częste oddawanie moczu, zwiększone pragnienie i, co za tym idzie, przyjmowanie płynów. Ponieważ stosunkowo duża liczba dzieci cierpi na cukrzycę, tak ważne jest, aby w szkołach już we wczesnym wieku uczniowie mogli uzyskać wiadomości na temat tego schorzenia. Osoby dotknięte cukrzycą muszą dowiedzieć się jak zminimalizować objawy choroby albo nawet zapobiec jej rozwojowi poprzez odpowiednią dietę i większą ilość ruchu. Zdrowe dzieci powinny natomiast zrozumieć sytuację i potrzeby kolegów cierpiących na cukrzycę.
W tym artykule opisujemy serię doświadczeń umożliwiających uczniom wykrywanie węglowodanów. Pierwsza część doświadczeń pozwoli stwierdzić, czy dany roztwór zawiera skrobię, białka czy cukry prostsze jak glukozę, laktozę czy sacharozę. Gdy już roztwory z cukrami zostaną zidentyfikowane, dalsze doświadczenia, wykorzystujące reakcję enzymatyczną, pomogą rozróżnić, w których próbkach obecna jest laktoza, a w których glukoza. Na tej samej zasadzie jak przedstawione poniżej doświadczenia działają testy medyczne, oznaczające poziom glukozy we krwi, stosowane w diagnostyce cukrzycy. Te same reakcje wykorzystuje się również do pomiaru zawartości glukozy i laktozy w produktach spożywczych, jak soki owocowe, mleko czy nabiał. Opisane doświadczenia pozwolą zatem uczniom zrozumieć w jaki sposób monitoruje się poziom cukrów u osób dotkniętych cukrzycą.
Doświadczenie 1: Wykrywanie cukrów, skrobi i białek
Uczniowie otrzymują pięć próbek, podpisanych od A do E, które zawierają skrobię, białko (bydlęcą albuminę), cukier prosty glukozę i dwucukry: laktozę lub sacharozę. Wszystkie roztwory należy przygotować w stężeniach 0,1% w wodzie. Dodatkowo można również wykorzystać próbki bezbarwnych napojów energetyzujących zawierających glukozę (np. Powerade®-Lemon). Używając opisanych niżej odczynników uczniowie powinni być w stanie określić, w których próbkach obecne są cukry, skrobia czy białka.
Dla klasy liczącej 30 uczniów, pracujących w parach, potrzebne będą następujące roztwory:
- Świeżo przygotowany odczynnik Fehlinga, otrzymany poprzez zmieszanie równych objętości jasno niebieskiego roztworu Fehlinga I (7 g CuSO4·5H2O rozpuszczone w 100 ml wody destylowanej) i bezbarwnego roztworu Fehlinga II (35 g C4H4KNaO6·4H2O i 10 g NaOH rozpuszczone w 100 ml wody destylowanej).
- Płyn Lugola, przygotowany poprzez rozpuszczenie 1 g jodyny i 2 g jodku potasu w 50 ml wody destylowanej.
- Barwnik Coomassie Brilliant Blue do testu Bradford, który dostępny jest komercyjnie, na przykład z firmy Bioradw1.
a) Wykrywanie cukrów redukujących (reakcja Fehlinga)
- Przenieś pipetą 1 ml każdej z próbek od A do E do probówek i grzej w temperaturze 60°C w łaźni wodnej przez 2 min.
- Dodaj 16 μl ciemno-niebieskiego odczynnika Fehlinga do każdej z probówek i inkubuj w 60°C przez kolejne 10 min, do momentu zaobserwowania barwnej reakcji i wytrącania osadu.
Roztwory zawierające cukry redukujące jak fruktoza, glukoza czy laktoza powinny dać barwę czerwoną, z wytrącaniem czerwonego osadu (rozpuszczalne jony miedzi (II) są redukowane do nierozpuszczalnych tlenków miedzi (I)). W roztworach sacharozy czy skrobi nie powinna następować zmiana koloru, a próbki zawierające białko powinny przybrać barwę jasnofioletową.
b) Detekcja skrobi za pomocą płynu Lugola
- Przenieś pipetą 500 μl każdej z próbek od A do Z do oddzielnych probówek.
- Dodaj 50 μl płynu Lugola do każdej z probówek i obserwuj barwną reakcję.
Płyn Lugola jest wskaźnikiem obecności skrobi. W wyniku oddziaływanie ze zwiniętą strukturą wielocukru barwnik ten daje ciemnoniebieską barwę. Nie wchodzi on natomiast w reakcję z cukrami prostymi, jak glukoza czy z dwucukrami (jak laktoza lub sacharoza).
c) Detekcja białek
Test na obecność białek oparty jest na metodzie Bradford, wykorzystującej zmianę koloru barwnika Coomassie Brilliant w wyniku wiązanie do łańcucha białkowego.
- Przenieś pipetą 20 μl każdej z próbek od A do E do pięciu oddzielnych probówek, a następnie dodaj 800 μl wody destylowanej oraz 200 μl barwnika Coomassie Brilliant Blue (odczynnik Bradford).
- Wymieszaj zawartość probówek, a następnie odczekaj około 5 min i obserwuj zmianę barwy testowanych próbek.
W obecności białek roztwór przybiera barwę niebieską (intensywność koloru może być zmierzona za pomocą spektrofotometru przy długości fali 595 nm). W przypadku próbek zawierających cukry lub skrobię nie powinniśmy zaobserwować żadnej zmiany koloru.
Uwaga
Test na obecność białek z firmy Biorad zawiera metanol i kwas fosforowy, więc powinien być używany z zachowaniem środków ostrożności.

Dzięki uprzejmośc Thomasa Wendt
| Fehling’s reaction | Lugol’s reaction | Protein assay | Compound | |
|---|---|---|---|---|
| Roztwór A | Czerwony osad | Barwa brązowa | Barwa brązowa | Cukier redukujący |
| Roztwór B | Niebieski roztwór | Barwa ciemnoniebieska | Barwa brązowa | Skrobia |
| Roztwór C | Czerwony osad | Barwa brązowa | Barwa brązowa | Cukier redukujący |
| Roztwór D | Fioletowy roztwó | Barwa brązowa |
Brown |
Białko |
| Roztwór E | Niebieski roztwór | Barwa brązowa |
Brown |
Sacharoza |
Wyniki i ich interpretacja
Roztwór B daje pozytywny wynik w reakcji z płynem Lugola, co wskazuje na obecność skrobi. Roztwór D reaguje barwnie z odczynnikiem Bradford, a więc jest to roztwór białka. W obecności odczynnika Fehlinga w roztworach A i C obserwujemy wytrącanie czerwonego osadu, co pozwala stwierdzić obecność cukrów redukujących, glukozy lub laktozy (choć na tym etapie nie potrafimy rozróżnić tych roztworów). W ostatnim roztworze E nie następuje żadna reakcja, a więc wnioskujemy, że zawiera on sacharozę.
Doświadczenie 2: Enzymatyczna identyfikacja cukrów
W drugim doświadczeniu ponownie zbadamy roztwory A i C, aby określić, który z nich zawiera glukozę, a który laktozę. Do tego celu użyjemy komercyjnie dostępnego testu EnzyPlus EZS 962+ lactose/D-glucose, który może być zakupiony od firmy BioControlw2. Procedura naszego doświadczenia będzie bardzo podobna do tej, która wykorzystywana jest rutynowo do pomiaru poziomu glukozy we krwi u pacjentów chorych na cukrzycę. Standardowy protokół, według którego stosuje się test EnzyPlus został przez nas tak zmodyfikowany i przeskalowany, aby możliwe było wykonanie większej ilości doświadczeń. Jeden test EnzyPlus powinien więc wystarczyć dla około 20 par uczniów.
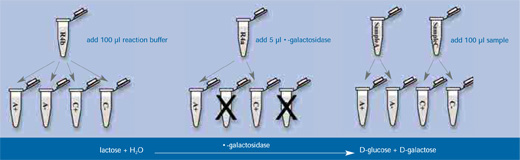
Zasada działania testu jest następująca (patrz rysunek poniżej):
- Dwucukier laktoza jest hydrolizowana przez enzym β –galaktozydazę do D-galaktozy i D-glukozy (Etap 1 poniżej).
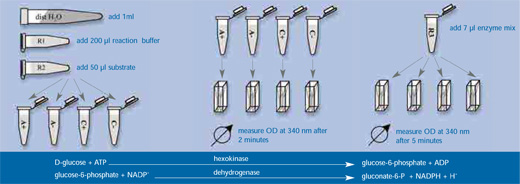
- W obecności ATP D-glukoza jest specyficznie fosforylowana przez enzym heksokinazę do glukozo-6-fosforanu, z równoczesnym wytworzeniem adenozyno-5-difosforanu (Etap 2).
- Glukozo-6-fosforan jest następnie utleniany przez dehydrogenazę glukozo-6-fosforanu do glukonylo-6-fosforanu.
- W tej reakcji NADP+ redukowany jest do NADPH. Ilość NADPH powstającego na tym etapie jest stechiometrycznie proporcjonalna do ilości laktozy na początku ciągu reakcji enzymatycznych i może być mierzona fotometrycznie poprzez wzrost absorbancji przy długości fali 340 nm.
Dzięki uprzejmości Thomasa Wendt
Dzięki uprzejmości Thomasa Wendt
Jak przeprowadzić reakcję:
- Przygotuj cztery probówki 1.5 ml i podpisz je kolejno: A+, A-, C+ oraz C-.
Do każdej z probówek dodaj 100 µl odczynnika R4b (jest to bufor fosforowy o pH 6.6), a następnie po 5 µl roztworu β-galaktozydazy R4a, ale tylko do probówek A+ i C+ (a nie do A- czy C-). - Przenieś pipetą 100 µl próbki A do probówek podpisanych A+ i A- oraz 100 µl próbki C do probówek C+ i C-.
Uwaga: Od tego momentu już wszystkie 4 probówki będą traktowane identycznie.
- Wstaw probówki do łaźni wodnej o temperaturze 37°C na 30 min, aby mogła nastąpić hydroliza laktozy.
- Po ukończonej inkubacji, dodaj do każdej probówki 1 ml wody destylowanej, a następnie 200 µl buforu reakcyjnego R1 oraz 50 µl odczynnika R2 (zawierających odpowiednio ATP i NADP) i mocno wymieszaj.
- Przenieś 1 ml z każdej mieszaniny reakcyjnej do oddzielnych kuwet fotometrycznych i po 2 minutach zmierz absorbancję przy długości fali 340 nm.
- Do każdej kuwety dodaj następnie 7 µl odczynnika R3 zawierającego enzymy heksokinazę i dehydrogenazę glukozo-6-fosforanu, inkubuj 5 min, a nastepnie zmierz ponownie absorbancję przy tej samej długości fali.
| Pierwszy pomiar (OD340) | Drugi pomiar (OD340) | Wynik | |
|---|---|---|---|
| Próbka A+ | 0.09 | 2.43 | Glukoza |
| Próbka- | 0.09 | 2.37 | Glukoza |
| Próbka C+ | 0.10 | 1.43 | Lactose |
| Próbka C- | 0.09 | 0.10 | Laktoza |
Wyniki i ich interpretacja
Przy pierwszym pomiarze absorbancji wszystkie próbki powinny dać niski odczyt, wskazując na brak obecności NADPH. Drugi pomiar (po dodaniu enzymów), powinien pomóc rozróżnić roztwory A i C. Ponieważ roztwór A daje pozytywny wynik niezależnie od obecności β-galaktozydazy, możemy wyciągnąć wniosek, że zawiera on glukozę. W przypadku próbki C obserwujemy natomiast, że wzrost absrobancji nastąpił jedynie po dodaniu β-galaktozydazy, co wskazuje na obecność laktozy.
Podczas opisanych ćwiczeń praktycznych uczestnicy mają okazję zdobyć wiadomości na temat cukrzycy, a także dowiedzieć się, jakim problemom chorzy na cukrzycę muszą stawiać czoła. Pacjenci dotknięci tym schorzeniem monitorują swój poziom glukozy we krwi używając testów paskowych, działających na tej samej zasadzie jak reakcje przedstawione w Doświadczeniu 2. Przeprowadzanie opisanych eksperymentów może pomóc uświadamiać uczniom, na czym polega cukrzyca, jak można ją zwalczać i zapobiegać jej poprzez poprawę stylu życia.
Doświadczenia przedstawione w tym artykule mogą być bezpiecznie przeprowadzone w szkolnych laboratoriach, jako że używane w nich odczynniki nie są zaliczane do niebezpiecznych (zgodnie z europejskimi przepisami o materiałach niebezpiecznych). Stężenia azydku sodu w odczynnikach są również niższe niż te uznawane za toksyczne.
ExploHeidelberg
The ExploHeidelbergw3 to nieoficjalne i interaktywne centrum edukacji naukowej. W jego skład wchodzą trzy różne części: interaktywna wystawa, laboratorium multimedialne oraz program zajęć praktycznych, czyli tak zwane laboratorium szkoleniowe.
Na wystawie interaktywnej odwiedzający mają okazję zaobserwować i doświadczyć różnych zjawisk optycznych, akustycznych i mechanicznych. Koncepcja oraz projekt wystawy powstał w ścisłej współpracy z Uniwersytetem Pedagogicznym w Heidelberguw4. Nauczyciele stażyści jak również pracownicy zakładu fizyki pełnią rolę przewodników, a ponadto projektują i opracowują eksponaty, przygotowują warsztaty, organizują szkolenia dla nauczycieli a także projekty badawcze.
Całodzienne zajęcia praktyczne w ramach laboratorium szkoleniowego oferują nauczycielom szkół ponadpodstawowych możliwość przeprowadzenia doświadczeń biotechnologicznych niemożliwych do wykonania w salach klasowych
Laboratorium multimedialne składające się z 12 komputerowych stanowisk pracy, posiadające instalacje umożliwiające publikowanie w internecie a także sprzęt do wideo-obrazowania dopełnia centrum edukacyjne ExploHeidelberg.
Wystawa interaktywna oraz laboratorium multimedialne otwarte są codziennie dla szerokiej publiki i mają na celu zainteresowanie zwiedzających naukami przyrodniczymi. Laboratorium szkoleniowe umożliwia natomiast uczniom i studentom, jak również nauczycielom i stażystom udział w specjalnych kursach, związanych z programami nauczania, dającymi wgląd w nowoczesne techniki biotechnologiczne. Uczestnicy mogą wybrać zajęcia jednodniowe, podczas których poznają podstawowe metody pracy z DNA czy białkami lub specjalistyczne tygodniowe kursy, które pozwolą im zetknąć się z bardziej zaawansowanymi technikami, zwykle ujętymi nauczaniem dopiero na poziomie uniwersyteckim.
References
- Dugi K (2006) Cukrzyca (diabetes mellitus). Science in School 1. www.scienceinschool.org/2006/issue1/diabetes/polish
Web References
- w1 – Biorad: www.bio-rad.com
- w2 – BioControl: www.rapidmethods.com
- w3 – ExploHeidelberg: www.explo-heidelberg.de
- w4 – Uniwersytet Edukacji Heidelberg: www.ph-heidelberg.de
Review
W tym artykule Fred Engelbrecht i Thomas Wendt odnoszą się do ważnego problemu cukrzycy oraz proponują dwa doświadczenia pozwalające zidentyfikować podstawowe składniki pożywienia, a także ukazujące podstawy naukowe glukozowych testów paskowych rutynowo używanych przez osoby cierpiące na cukrzycę.
Styl artykułu, przejrzysty i poprawny, jest łatwiejszy w pierwszej części, dotyczącej cukrzycy; część doświadczalna stanowi już pewne wyzwanie i daje nauczycielom możliwość wyboru odpowiednich sekcji, w zależności od poziomu nauczania w klasach.
Artykuł ten może być przydatny w programach nauczania biologii i chemii, przedstawiając interdyscyplinarne podejście do problemu cukrzycy i łącząc tym samym zagadnienia z dziedziny biochemii, biologii i edukacji zdrowotnej. Ukazując szeroko pojęta naturę choroby, autorzy podnoszą świadomość społeczną i podkreślają jak ważna jest akceptacja i całkowite włączanie osób cierpiących na cukrzycę do życia społecznego.
Artykuł może być również wykorzystany, aby poszerzyć wiadomości na temat węglowodanów i białek, przybliżyć zagadnienia z zakresu metabolizmu (biochemia), układu trawiennego (biologia), pożywienia i zdrowia (edukacja zdrowotna), jak również technik laboratoryjnych (chemia).
Pierwsza część może być wykorzystana, aby sprawdzić stopień przyswojenia wiadomości na temat cukrzycy, a druga stopień zrozumienia zagadnień doświadczalnych. Przykładowe pytania mogą brzmieć następująco:
Która spośród niżej wymienionych cech nie jest charakterystyczna dla cukrzycy?
a) Wysoki poziom glukozy we krwi
b) Niedostateczna produkcja insuliny lub oporność tkanek na jej działanie
c) Niski poziom glukozy we krwi
d) Częste oddawanie moczu oraz zwiększone pragnienie.
Dane przedstawione w Tabeli 2 oznaczają, że:
a) Glukoza wymaga obecności β-galaktozydazy, aby nastąpiła produkcja NADPH
b) Laktoza wymaga obecności β-galaktozydazy, aby nastąpiła produkcja NADPH
c) Laktoza nie wymaga obecności β-galaktozydazy, aby nastąpiła produkcja NADPH
d) Glukoza wymaga glukozo-6-fosforanu, aby nastąpiła produkcja NADP+.
Giulia Realdon, Włochy





