Verso una chimica più verde Understand article
Tradotto da Giovanna Dalvit. La chimica non è sempre completamente ecologica; la chimica verde sta cercando di cambiare questo fatto.
La chimica ha una reputazione ambivalente. Noi tutti beneficiamo dei beni di consumo e dei farmaci che l’industria chimica produce, ma c’è anche un lato negativo – come l’enorme richiesta di energia delle industrie e la produzione di solventi, reagenti e prodotti di scarto tossici. Da più di 20 anni, i chimici stanno provando a ripulire la chimica grazie al settore emergente della chimica verde.
Conosciuta anche come chimica sostenibile o chimica ecocompatibile, la chimica verde è un concetto che sta lentamente venendo introdotto a livello scolastico. Due dei suoi primi paladini, Paul Anastas e John Warner, definiscono la chimica verde come ‘l’ideazione di prodotti e processi chimici che riducano o eliminino l’uso e la creazione di sostanze pericolose’.
originali nella sintesi
dell’ibuprofene sono stati ora
rimpiazzati da una sintesi più
efficiente a tre passaggi.
Immagine per gentile
concessione di Nicola Graf
L’eliminazione, o la riduzione, di rifiuti chimici; la diminuzione della richiesta totale di energia per i processi; e l’incremento della consapevolezza sulla sicurezza sono nell’interesse dell’umanità e dell’ambiente. Anche l’industria è interessata: un rapporto del 2011 ha suggerito che la chimica verde potrebbe far risparmiare all’industria 65,5 miliardi di dollari USA entro il 2020.
Le idee principali alla base della chimica verde possono essere riassunte brevemente in pochi semplici punti, che potrebbero costituire interessanti argomenti da discutere genericamente a lezione o dare adito a considerazioni più profonde sui processi chimici tradizionalmente insegnati nelle scuole. Qui affronteremo il discorso dalla prospettiva della chimica del clima. Un elenco completo dei 12 principi della chimica verde può essere trovato onlinew1, ma noi ci limiteremo a quegli aspetti maggiormente applicabili a livello scolastico: l’economia atomica, la provenienza dei reagenti, l’uso di sostanze ecocompatibili e il risparmio energetico.
Ridurre lo scarto
Uno dei temi della chimica verde è quanta parte dei reagenti e dei solventi vada a formare il prodotto desiderato e quanta invece finisca in scarti o sotto-prodotti. Ridurre lo scarto riduce i problemi ambientali ad esso associati. L’idea di ‘economia atomica’ e i semplici esercizi che gli studenti possono eseguire (vedi riquadro) rafforzeranno queste idee. Si dovrebbe considerare anche la provenienza delle sostanze di partenza. Dove possibile, i reagenti dovrebbero essere rinnovabili, o ottenuti da fonti prontamente e facilmente accessibili.
I farmaci, in particolare, sono spesso prodotti mediante reazioni di sintesi a più stadi, invece che in reazioni semplici in provetta dove il reagente A reagisce col reagente B per creare il farmaco. Nelle sintesi multi-fasiche, il prodotto ottenuto in un passaggio è usato nel successivo, ma la resa di ogni fase è molto minore del 100%, di conseguenza lungo la strada si perdono materiali, solventi ed energia.
Le vie sintetiche con pochi passaggi più produttivi, sempre considerando gli altri principi ‘verdi’, producono meno scarto. Per esempio, l’antidolorifico ibuprofene era originariamente prodotto partendo dall’isobutilbenzene in una sintesi a 6 passaggi, ma una nuova via più efficiente ne impiega solamente tre (figura 1).
Ridurre la tossicità
La chimica verde cerca anche di usare unicamente sostanze non dannose per l’ambiente. In uno dei peggiori disastri industriali a livello mondiale, il gas metilisocianato (CH3NCO) usato nella produzione di pesticidi, fuoriuscì dall’impianto della Union Carbide India Limited, a Bhopal, in India, nel 1984, a cui furono esposte migliaia di persone. L’immediato bilancio riportava diverse migliaia di morti, e quasi mezzo milione di persone lese, con disabilità temporanee o permanenti.
Oltre a scegliere reagenti meno tossici, i chimici verdi cercano anche di passare a solventi inorganici come l’acqua e l’anidride carbonica in fase supercritica. I solventi idrocarburici precedentemente utilizzati sono tossici ed emettono vapori che formano gas serra, mentre i solventi alogenati sono spesso cancerogeni, oltre ad essere anch’essi gas serra e fonti di radicali liberi – che distruggono l’ozono.
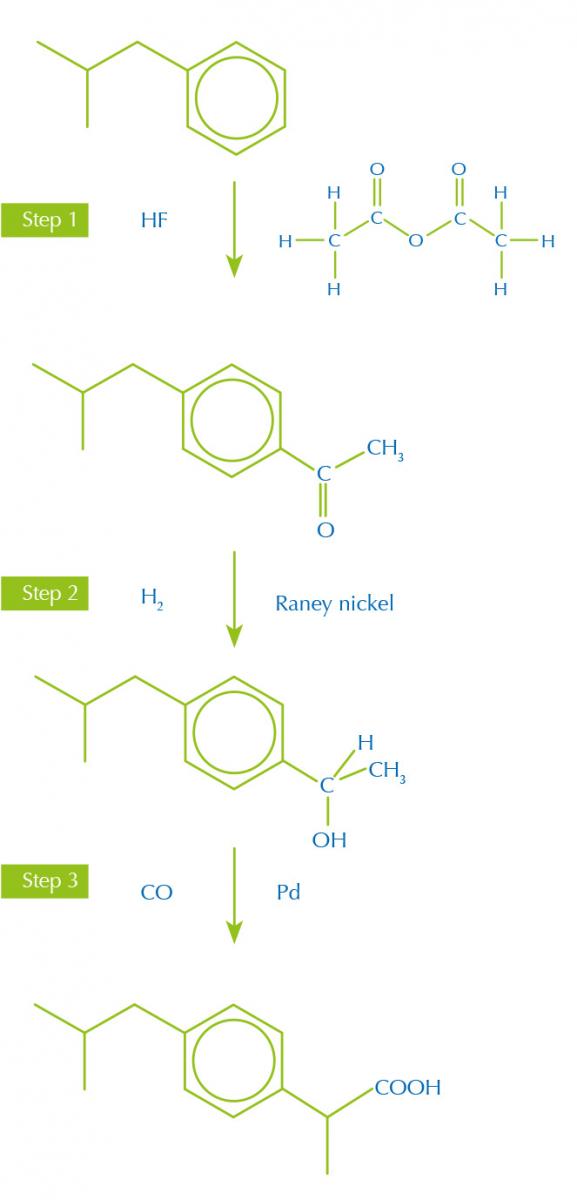
dell’ibuprofene
Immagine per gentile
concessione di Nicola Graf
Ridurre le emissioni
L’industria chimica necessita di un’enorme quantità di elettricità; ridurre questa richiesta è importante sia economicamente che dal punto di vista ambientale. I ricercatori usano l’energia per riscaldare e aumentare la pressione nelle reazioni, oltre che per trasportare materiali. Gli scienziati stanno cercando percorsi di reazione alternativi, che funzionino a temperature e pressioni inferiori, riducendo la quantità di anidride carbonica prodotto nella combustione dei combustibili fossili.
Trovare catalizzatori più efficienti per le reazioni esistenti contribuirà a ridurre lo spreco di energia e di reagenti. Idealmente, i catalizzatori dovrebbero essere costituiti da metalli prontamente disponibili come il ferro, invece che da metalli rari come il platino, che sono scarsi e che richiedono per il loro ottenimento una considerevole quantità di energia. Alcuni catalizzatori vengono anche ‘avvelenati’ durante la reazione, il che significa che i composti chimici si legano al sito attivo del catalizzatore e formano prodotti sulla sua superficie che potrebbero essere tossici e difficilmente gestibili in sicurezza.
Applicare la chimica verde ai biocarburanti
Quando c’è bisogno di energia, i biocombustibili sono sostituti desiderabili dei carburanti fossili. L’etanolo è un biocombustibile molto noto, prodotto da molti processi fermentativi. Può essere prodotto da materia vegetale, incluse alcune erbe e gli scarti del mais. I veicoli adattati possono usare etanolo al 100% (E100) o miscugli etanolo-benzina, noti come miscele di bioetanolo (in inglese gasohol: gasoline + alcohol), che spaziano da E5 a E25. Tuttavia l’etanolo non è un combustibile particolarmente buono, perché:
- non evapora con la stessa facilità della benzina;
- ha solo circa il 70% della densità energetica della benzina;
- ha la tendenza ad attirare l’acqua;
- è acido alle temperature interne al motore e può causare corrosione;
- richiede motori adattati per funzionare con una maggiore proporzione di questo combustibile.
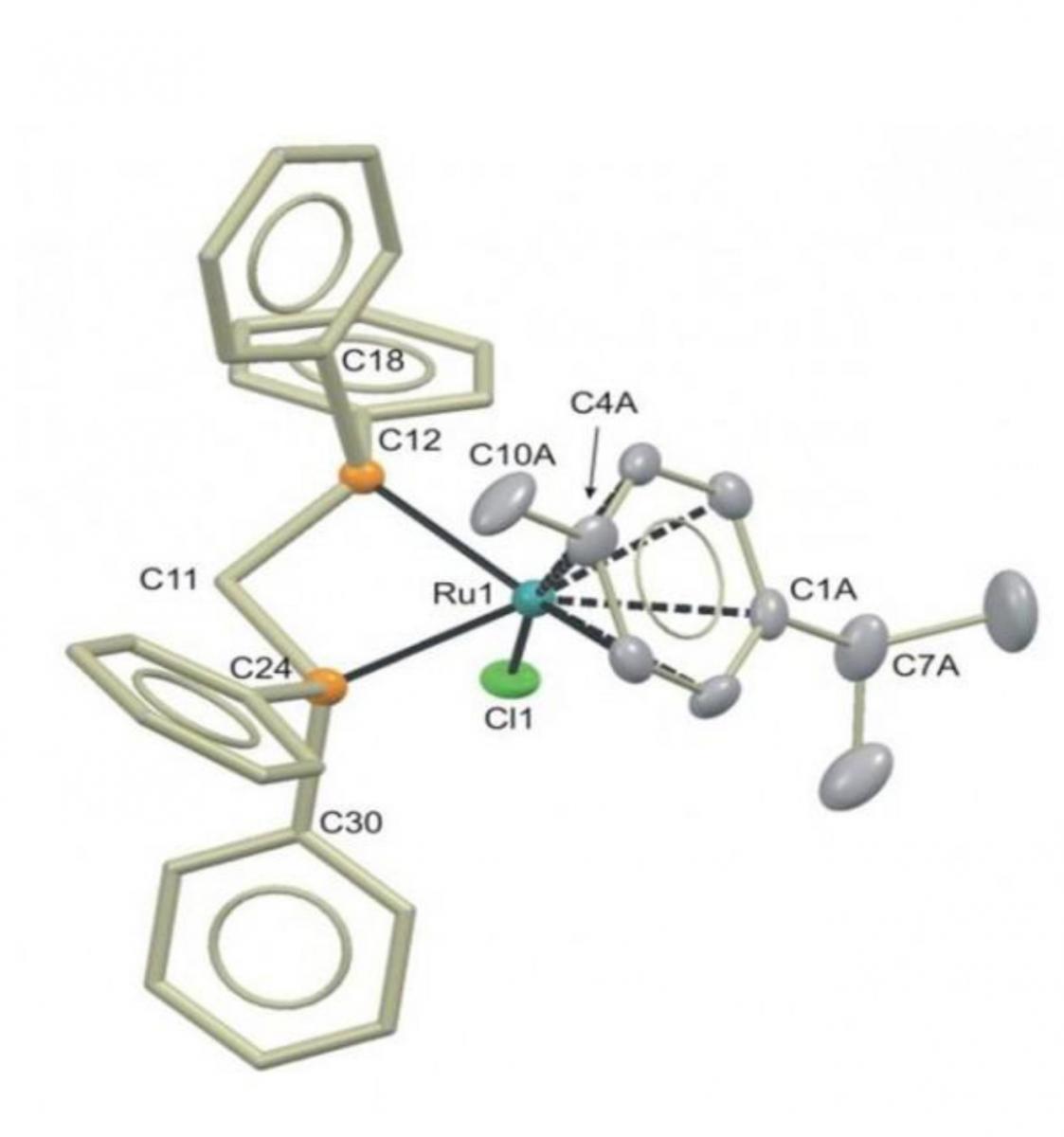
come catalizzatore per
produrre il butanolo
dall’etanolo
Immagine per gentile
concessione di Duncan
Wass/Università di Bristol
Il butan-1-olo , o 1-butanolo, (che ha una densità di energia di 29,2 MJ/l) sarebbe un carburante molto migliore dell’etanolo (19,6 MJ/l). Il butan-1-olo può essere prodotto da biomasse (biobutanolo) e da combustibili fossili (butanolo derivato dal petrolio). Però questi processi o necessitano di grandi quantità di energia o si affidano a catalizzatori biologici (enzimi) con bassa resa. La separazione del butanolo da un miscuglio di prodotti è a sua volta energeticamente costosa.
La produzione di butanolo dalla condensazione di due molecole di etanolo è stata a lungo un obiettivo dell’industria chimica:
CH3CH2OH + HOCH2CH3 → CH3CH2CH2CH2OH + H2O
Nel 2013, però, una sensazionale scoperta ha permesso di produrre butanolo da etanolo con rese maggiori del 95% usando un catalizzatore al rutenio. La sfida ora è di adattare il processo all’uso industriale.
Le problematiche ambientali non se ne andranno, quindi la chimica verde diventerà ancora più importante. Sarà necessario insegnare ai giovani ad applicare i principi della chimica verde in tutte le scienze chimiche e nell’ingegneria.
Economia atomica
Tradizionalmente, i chimici calcolano l’efficienza di una reazione considerando la resa percentuale.
Resa percentuale = (moli di prodotto ottenute / moli di prodotto attese) x 100
Barry Trost della Standford University, negli Stati Uniti, ha introdotto il concetto dell’economia atomica come modo alternativo di definire l’efficienza di una reazione. L’economia atomica mette in rapporto la massa del prodotto desiderato con la massa totale del materiale di partenza. Quindi, il calcolo evidenzia le risorse sprecate: se solo una piccola parte del materiale di partenza si trova nel prodotto, deve essere finito tra gli scarti.
Economia atomica percentuale = (massa del prodotto desiderato / massa totale di tutti i reagenti) x 100
È facile dimostrare coi calcoli che un chimico che usi l’economia atomica preferirà utilizzare materiali di partenza semplici per costruire il prodotto, piuttosto che rompere grosse molecole, producendo di conseguenza molti prodotti di scarto.
Consideriamo le reazioni in cui il prodotto voluto è l’ossido di magnesio:
2Mg + O2 → 2MgO
2 x 24 = 48 g 32 g 2 x 40 = 80 g
Economia atomica = (80 / (48 + 32)) x 100 = 100%
MgCO3 → MgO + CO2
84 g 40 g 44 g
Economia atomica = (40 / 84) x 100 = 48%
Gli studenti migliori potrebbero voler verificare come i cambiamenti nella produzione dell’ibuprofene migliorino l’efficienza atomicaw2.
References
- Anastas PT, Warner C (1998) Green Chemistry Theory and Practice. New York, NY, USA: Oxford University Press. ISBN: 0198502346
- Trost BM (1991) The atom economy – a search for synthetic efficiency, Science 254: 1471–1477
Web References
- w1 – Il libro 12 principles of green chemistry può essere trovato sul sito della American Chemistry Society.
- Il sito della ACS offre anche una serie di risorse didattiche sulla chimica verde, inclusi libri, risorse online e protocolli sperimentali per tutte le età (dalla scuola secondaria alla laurea triennale).
- w2 – Sul sito Learn Chemistry della Royal Society of Chemistry c’è una lezione sulla sintesi dell’ibuprofene, che considera anche la struttura e i legami molecolari del farmaco.
Resources
- Per le attività pratiche associate al cambiamento climatico, consultare:
- Shallcross D, Harrison T (2008) Practical demonstrations to augment climate change lessons. Science in School 10: 46–50.
- Shallcross D, Harrison T, Henshaw S, Sellou L (2009) Fuelling interest: climate change experiments. Science in School 11: 38–43.
- Shallcross D, Harrison T, Henshaw S, Sellou L (2009) Looking to the heavens: climate change experiments. Science in School 12: 34–39.
Review
Come puntualizzato dall’autore, la chimica è circondata da un’aura negativa tra gli studenti e il pubblico in genere, ma la chimica che sta dietro agli oggetti e ai materiali è indispensabile per la nostra vita. Questa è la ragione per cui consiglio questo articolo prima di iniziare un corso di chimica nella scuola secondaria.
Le idee dietro alla chimica verde sono chiaramente espresse in uno stile semplice con esempi presi dalla vita di tutti i giorni, dalla sintesi di farmaci ai biocarburanti. Varrebbe la pena, ovviamente, di approfondire l’argomento ulteriormente e, se possibile, di farne esperienza diretta tramite attività pratiche.
Entrambi questi obiettivi sono raggiungibili grazie ai riferimenti citati (sito di ACS e pagine educative della Royal Society of Chemistry).
Inoltre, la storia degli incidenti chimici, come il disastro di Bhopal, può fornire agli insegnanti gli elementi per discutere di sicurezza chimica, sostenibilità ambientale e del ruolo della chimica verde.
Gulia Realdon, Italia





