Waterstof: de groene energiedrager van de toekomst? Understand article
Vertaald door Piet Das. Waterstof kan de brandstof van de toekomst zijn, maar hoe kunnen we het duurzaam produceren ? Karin Willquist legt het uit.

iStockphoto
Waterstof wordt ook wel ‘de energiedrager van de toekomst’ genoemd – omdat het kan worden geoxideerd in een brandstofcel om elektriciteit op te wekken, om bijvoorbeeld auto’s aan te drijven zonder dat er kooldioxide (CO2) vrijkomt. Het kan worden geproduceerd in afgelegen gebieden zonder een elektriciteitsinfrastructuur. In tegenstelling tot de beschikbare bronnen als aardgas en benzine , moet waterstof worden geproduceerd , waardoor het een energiedrager is en geen brandstof.
Een energiesysteem waarin waterstof wordt gebruikt om energie te leveren – een waterstofeconomie – werd voorgesteld door John Bockris in 1970; in 1977 werd een internationale waterstof overeenkomst opgezet om dat te verwezenlijkenw1.
Waterstof wordt tegenwoordig meer gebruikt als een chemische reagens dan als energiedrager, maar het heeft zonder twijfel de potentie om onze vervoers- en energiesystemen volledig te veranderen. Het realiseren van die potentie is echter niet eenvoudig. De brandstoffen die momenteel gebruikt worden zijn vloeistoffen, vaste stoffen of gassen met een hoge energie per volume ( energiedichtheid) . Waterstof daarentegen heeft een lage energiedichtheid: bij een gegeven druk geeft het verbranden van een liter waterstof maar een derde van de energie die het verbranden van een liter methaan geeft. Hierdoor ontstaan problemen bij de opslag, distributie en gebruik, die worden aangepakt door wetenschappers (Schlapbach & Züttel, 2001)w2. Een fundamenteel probleem is echter om waterstof op duurzame wijze te produceren . Hier zal ik mij in dit artikel op focussen.
Manieren om waterstof te maken

die op waterstof
brandstofcellen rijden
Figuur met dank aan Felix O;
beeldbron: Flickr
Waterstof is een veel voorkomend element op aarde. Het is meestal gekoppeld aan koolstof in koolhydraten (in planten) of aan zuurstof in water (H2O). Waterstofgas (H2), daarentegen komt alleen in kleine hoeveelheden op aarde voor. Een van de uitdagingen voor een duurzame productie van waterstof is het vrijmaken van H2 uit de verbindingen met koolstof en zuurstof.
Op dit moment wordt H2 voornamelijk geproduceerd uit fossiele brandstoffen (bijv. aardgas) met behulp van stoom: het verwarmen van brandstoffen bij hoge temperaturen met waterw2:
CH4 + H2O → CO + 3H2 (1)
CO + H2O → CO2 + H2 (2)
Deze methode is echter afhankelijk van fossiele brandstoffen en door de CO2 – uitstoot geeft het dezelfde emissieproblemen als het verbranden van fossiele brandstoffen. Omzetting met behulp van stoom is alleen duurzaam als hernieuwbare koolwaterstoffen zoals biogas worden gebruikt, omdat de vrijkomende CO2 al eerder opgenomen werd bij het ontstaan van koolwaterstoffen in planten.
H2 kan ook worden geproduceerd door elektrolysew2, waarbij elektriciteit wordt gebruikt om H2O in H2 en zuurstof te splitsen:
2H2O → 2H2 + O2 (3)

telefoonoplader van
Powertrekk . Voeg wat water
toe en na een paar minuten
heb je een batterij voor je
mobiele telefoon
Figuur met dank aan David
Berkowitz; beeldbron: Flickr
Deze methode kan duurzaam zijn als de elektriciteit van hernieuwbare bronnen komt, zoals wind, water of zonne-energie. H2 kan op deze manier worden gebruikt om energie op te slaan op winderige dagen als de windmolens meer elektriciteit produceren dan kan worden geconsumeerd.
Interessant is dat het splitsen van H2O van nature voorkomt in de oceanen , omdat microscopische algen en cyanobacteriën zonne-energie gebruiken om water te splitsen in een proces genaamd biofotolyse (Reactievergelijking 3). De snelheid van de H2 productie is echter uiterst traag.
Men heeft zich ingespannen om de productie te verhogen onder gecontroleerde omstandigheden met behulp van gemodificeerde micro-organismen, maar de processen zijn nog steeds te traag en te duur om een realistische bron van H2 op korte termijn te zijn (Hallenbeck & Ghosh, 2009).
Tot slot kan biowaterstof met behulp van bacteriën worden geproduceerd uit gewassen en van industriëel bos-en landbouwafval. Net als wij oxideren deze bacteriën plantaardig materiaal als bron van energie, maar anders dan wij leven ze in anaërobe omstandigheden ( tekort aan zuurstof). Bij aërobe verbanding gebruiken we bijvoorbeeld O2 om suikers te oxideren.
C6H12O6 + 6O2 → 6CO2 + 6 H2O (4)
In tegenstelling hiermee: Om het substraat zoveel mogelijk te oxideren en daarmee energiewinst te optimaliseren, reduceren deze anaerobe bacteriën protonen die tijdens de oxidatie van het substraat ontstaan tot H2 ( Reactievergelijking 6, hieronder).
“Hot bugs”

bacterie onder de electronen
microscope
Figuur met dank aan Harald
Kirsebom
Tijdens mijn promotie heb ik onderzoek gedaan naar het waterstof-producerende vermogen van een van deze bacteriën, Caldicellulosiruptor saccharolyticus (figuur 1) die leeft in hete bronnen : anaërobe omstandigheden bij 70° C en kleine hoeveelheden beschikbare koolhydraten . Deze bacterie is met name van belang omdat het twee keer zo efficiënt is als de meeste bacteriën gebruikt voor de productie van H2.
In tegenstelling tot mensen krijgt C. saccharolyticus energie uit een breed spectrum van plantaardige bouwstenen : niet alleen glucose, maar ook bijvoorbeeld xylose (Willquist et al., 2010).
Hierdoor kan de bacterie H2 produceren uit afvalstoffen zoals die bij de aardappel-, suiker- en wortelverwerking ontstaan en tevens uit industrieel afval van de pulp en papierproductie of uit landbouwafval zoals stro.
Dit is een veelbelovend begin maar zelfs C. saccharolyticus haalt slechts 33% van de potentiële H2 die zou kunnen worden vrijgemaakt uit het substraat. Vergelijking 5 toont de mogelijke totale oxidatie van glucose waarbij 12 H2 per molecuul glucose vrijkomt. Vergelijking 6 toont fermentatie in het donker door C. saccharolyticus die slechts 4 H2 (33 % ) per molecuul glucose geeft. De rest van de energie komt vrij als acetaat ( CH3COOH ).
Totale omzetting van glucose tot H2: C6H12O6 + 6H2O → 12H2 + 6CO2 (5)
Fermentatie in het donker: C6H12O6 + 2H2O → 4H2 + 2CO2 + 2CH3COOH (6)
Om de rest van de H2 vrij te maken uit het acetaat is energie van buitenaf nodig . Ook kan methaan (CH4) – waaruit met behulp van stoom H2 kan ontstaan (vergelijkingen 1 en 2) – uit acetaat worden gehaald. Gelukkig zijn er drie veelbelovende manieren om dit te doen (figuur 2).
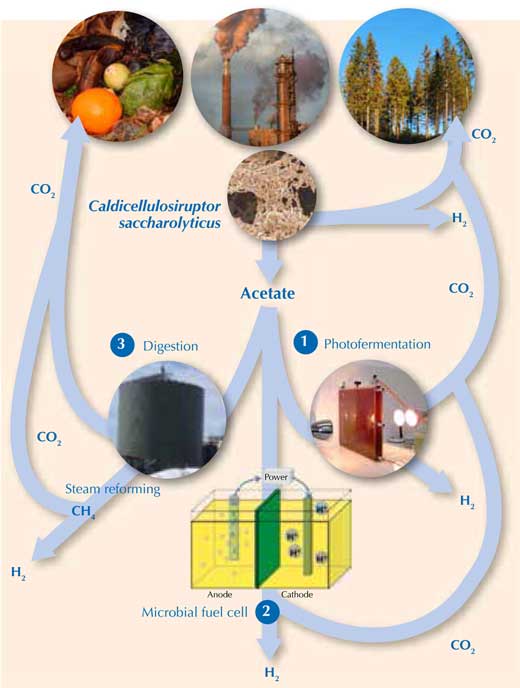
Foto met dank aan Holger / pixelio.de (afval ), Michael Caven ( papierfabriek ), Keith Bryant (bomen), Marcel Verhaart (C. saccharolyticus ), Jakub Gebicki ( fotobioreactor ), Gokce Avcioglu, METU Biowaterstof Research Lab, Turkije ( anaërobe verteringsreactor) en Karin Willquist (microbiële brandstofcel)
- Met zonlicht acetaat omzetten in H2 met behulp van fotofermentatieve bacteriën ( reactievergelijking 7)w3. Net zoals de productie van H2 door algen is dit proces echter op dit moment te traag en te duur om commercieel levensvatbaar te zijn op de korte termijn (Hallenbeck & Ghosh, 2009).
2CH3COOH + 4H2O → 8H2 + 4CO2 (7)
- Elektriciteit gebruiken om de reactie van acetaat tot H2 in een microbiële brandstofcel met een mengsel van bacteriesoorten te versnellen (Vergelijking 7)w4. Dit is een elegant concept maar de toepassing ervan wordt momenteel beperkt door een lage productie (Hallenbeck & Gush, 2009). (Om te leren hoe je je eigen microbiële brandstofcel op te bouwen, zie Madden, 2010.)
- Methaan genereren met behulp van methaanproducenten (Archaea) die acetaat verteren (reactievergelijking 8). De combinatie van fermentatie in het donker ( reactievergelijking 6) en methaanproductie staat bekend als het “hythane” = waterstofmethaan proces en daarmee kan ongeveer 90% van het oorspronkelijke substraat omgezet worden in H2 en methaan.
CH3COOH → CH4 + CO2 (8)
De methaan kan met behulp van stoom worden omgezet in H2.

aangedreven dooreen
waterstofbrandstofcel
Figuur met dank aan
Bull-Doser; beeldbron:
Wikimedia Commons
Om het waterstofmethaanproces in het juiste perspectief te plaatsen: als vier mensen in een huis 10 kg aardappelproducten eten in één maand kan hun afval 0,5% van hun maandelijkse huishoudelijke energiebehoefte (3500 kWh) leveren, op voorwaarde dat de H2 die wordt geproduceerd direct wordt gebruikt (om energieverlies te voorkomen) en dat het huis is uitgerust met een krachtwarmte-brandstofcelw5. Meer waterstof kan uiteraard worden opgewekt uit ander afval – 0,5% is alleen van de aardappelen.
Dit is een ruwe schatting van het potentieel van de waterstofmethaanproces, op basis van a) 30% energieverlies in de productie van H2 en CH4 (waterstof en methaan) en b) 30% in vervolgens met stoom omzetten van CH4 in H2. De stoom-omzetting stap (b) wordt gebruikt bij de productie van waterstof uit aardgas en is een goed uitontwikkelde commerciële techniek. De productie van waterstofmethaan (a) is echter nog niet zo erg efficiënt, hoewel nog steeds onderzoek wordt gedaan om de efficiëntie van 70% (zoals in het voorbeeld) te verbeteren, en om op deze manier de productie van biowaterstof te laten concurreren met de stoom-omzetting van fossiele brandstoffen in waterstof .
Hoewel er recent enige vooruitgangw6 is geboekt (zie kader), is het te vroeg om een betrouwbare schatting van de tijd te geven voor het tijdstip waarop de duurzame productie van H2 een belangrijke rol zal kunnen spelen in het leveren van onze energie. Zoals de dichter Mark Strand echter ooit zei: ” De toekomst begint altijd nu.”
Onderzoek naar de waterstofopslag en -productie

Waterstof veilig en efficiënt opslaan is een van de belangrijkste technologische uitdagingen voor het aanvaarden van waterstof als energiedrager. Het Institut Laue – Langevin (ILL)w7 his een sterke partij geworden bij grensverleggend onderzoek naar de waterstof-economie, daarbij gebruik makend van neutronendiffractie om hydrogenering en dehydrogeneringsreacties in potentiële materialen voor waterstofopslag te bestuderen. Bezoek de IBL websitew7 voor meer informatie.
De krachtige X-stralen van de Europese Synchrotron Radiation Facility (ESRF)w8 hebben onlangs onderzoek gedaan naar de complexe mechanismen waarbij waterstof wordt geproduceerd door enzymen genaamd hydrogenasen. De meeste van deze enzymen werken onder anaerobe omstandigheden en worden in feite geremd door de aanwezigheid van zuurstof. Hydrogenasen die actief blijven onder aërobe omstandigheden , zijn daarom van groot belang voor technologieën zoals enzymatische brandstofcellen en de met behulp van licht opgewekte productie van waterstof . Een Duits team van wetenschappers heeft onlangs de kristallijne structuur van een van deze enzymen (Fritsch et al., 2011) ontraadseld- Misschien een stap op weg naar een waterstofeconomie ?
Zowel ILL als ESRF zijn leden van het EIROforumw9, de uitgever van Science in School.
References
- Fritsch J et al. (2011) The crystal structure of an oxygen-tolerant hydrogenase uncovers a novel iron-sulphur centre. Nature 479: 249–252. doi: 10.1038/nature10505
-
Download hier het artikel gratis, of abonneer u vandaag op Nature: www.nature.com/subscribe
-
- Hallenbeck P, Ghosh D (2009) Advances in fermentative biohydrogen production: the way forward? Trends in Biotechnology 27: 287–297. doi: 10.1016/j.tibtech.2009.02.004
- Madden D (2010) The microbial fuel cell: electricity from yeast. Science in School 14: 32-35. www.scienceinschool.org/2010/issue14/fuelcell
- Rifkin J (2002) The Hydrogen Economy: the Creation of the Worldwide Energy Web and the Redistribution of Power on Earth. New York, NY, USA: JP Tarker. ISBN: 1585421936
- Schlapbach L, Züttel A (2001) Hydrogen-storage materials for mobile applications. Nature 414(6861): 353–358. doi: 10.1038/35104634
-
Download hier het artikel gratis, of abonneer u vandaag op Nature: www.nature.com/subscribe
-
- Willquist K, Zeidan A, van Niel E (2010) Physiological characteristics of the extreme thermophile Caldicellulosiruptor saccharolyticus: an efficient hydrogen cell factory Microbial Cell Factories 9: 89. doi: 10.1186/1475-2859-9-89
- Microbial Cell Factories is een vrij in te zien tijdschrift , dus het artikel is gratis beschikbaar.
Web References
- w1 – Voor meer informatie over de waterstof- implementeringsovereenkomst van de International Energy Agency, zie: http://ieahia.org
- w2 – Om meer over de kansen voor waterstof aan de weet te komen, lees dan Joseph Romm ‘s analyse van de Ecologen Voor Kernenergie website (www.ecolo.org; onder “ documenten”) of via de directe link: http://tinyurl.com/77dhx8x
-
Zie ook de door vakgenoten getoetste analyse van Joan Ogden: Hydrogen as an Energy Carrier: Outlook for 2010, 2030 and 2050 (Waterstof als energiedrager : Vooruitblik voor 2010 , 2030 en 205)0 op de website van de Universiteit van Californië : http://escholarship.org/uc/item/9563t9tc
-
- w3 – Voor een video over hoe waterstof wordt vrijgemaakt uit aardappelbiomassa met behulp van zonlicht , zie: www.biohydrogen.nl/hyvolution
- w4 – Om meer kennis op te doen over microbiële brandstofcellen, zie: www.microbialfuelcell.org
- w5 – Als je meer over krachtwarmte brandstofcellen wil weten, zie: www.fchea.org/index.php?id=57
- w6 – Als je nog iets wilt lezen over de recente vorderingen op een biowaterstoftankstation in Taiwan , zie de Focus Taiwan website (http://focustaiwan.tw) of gebruik de directe link : http://tinyurl.com/7jao2tp
- w7 – IBL is een vooraanstaand internationaal onderzoekscentrum voor neutronenwetenschap en technologie , gevestigd in Grenoble , Frankrijk. Voor meer informatie, zie: www.ill.eu
-
Voor meer informatie over IBL ’s onderzoek over de waterstofeconomie, zie de IBL- website of gebruik de directe URL: http://tinyurl.com/illhydrogen
-
- w8 – Gelegen op dezelfde campus als IBL in Grenoble , Frankrijk, exploiteert ESRF de krachtigste synchrotron stralingsbron in Europa. Voor meer informatie , zie: www.esrf.eu
-
Voor meer informatie over het onderzoek van ESRF naar de opslag van waterstof , zie de ESRF website of gebruik de directe URL: http://tinyurl.com/87bnj4c
-
- w9 – Om meer aan de weet te komen over EIROforum, zie: www.eiroforum.org
Review
Na de publicatie van het boek van Jeremy Rifkin ’s over de waterstof-economie (2002), komt dit onderwerp vaak aan bod in de media als een reële mogelijkheid voor de nabije toekomst . Een ander veel beschreven onderwerp over waterstof is zijn vermeende rol als schone energiebron . In dit artikel biedt Karen Willquist een grondig overzicht van problemen die betrekking hebben op de productie van waterstof en van het lopende onderzoek – met inbegrip van haar eigen werk – en naar duurzame manieren om dit doel te bereiken..
Gezien de heldere aanpak van de auteur, is het artikel met name geschikt voor docenten in de natuurwetenschappen en scholieren uit de bovenbouw van het middelbare onderwijs (leeftijd 14-19) die hun kennis van dit complexe onderwerp willen verdiepen. Bovendien zullen zowel docenten als studenten profiteren van de vele bronnen .
Het artikel is belangrijk voor lessen over biochemie ( ademhaling , fermentatie en fotosynthese ) , natuurkunde ( brandstofcellen , thermodynamica : energie en efficiëntie) , milieukunde (energiebronnen , fossiele brandstoffen en hernieuwbare energiebronnen) , biologie (algen , bacteriën , cyanobacteriën en archaea) en organische chemie ( koolwaterstoffen en stoomomzetting ). Het kan waardevolle achtergrondinformatie leveren voordat een bezoek gebracht wordt aan een elektriciteitscentrale of een onderzoekslaboratorium die werkt aan brandstofcellen of waterstof-productie, -gebruik of -opslag.
Het artikel kan worden gebruikt om een discussie te beginnen over het verschil tussen energiebronnen en energiedragers; de problemen van waterstof -gebruik en -opslag en mogelijke scenario’s voor de overgang van onze koolwaterstof- economie naar een waterstofeconomie.
Geschikte begripsvragen zijn:
- Welke van de volgende onderwerpen zijn van toepassing op ademhaling, fermentatie in het donker, of beide ?
- De aanwezigheid van glucose
- De aanwezigheid van zuurstof
- De afwezigheid van zuurstof
- Welke van de hieronder genoemde onderwerpen is geen process waarbij acetaat in waterstof wordt omgezet?
- Fermentatie in het donker
- Het gebruik van elektriciteit in een microbiële brandstofcel
- Het waterstofmethaan proces
Giulia Realdon, Italië





