Aggregatietoestanden & faseovergangen Teach article
Ontdek de faseovergangen tussen de verschillende aggregatietoestanden met een reeks uitdagende hands-on experimenten.

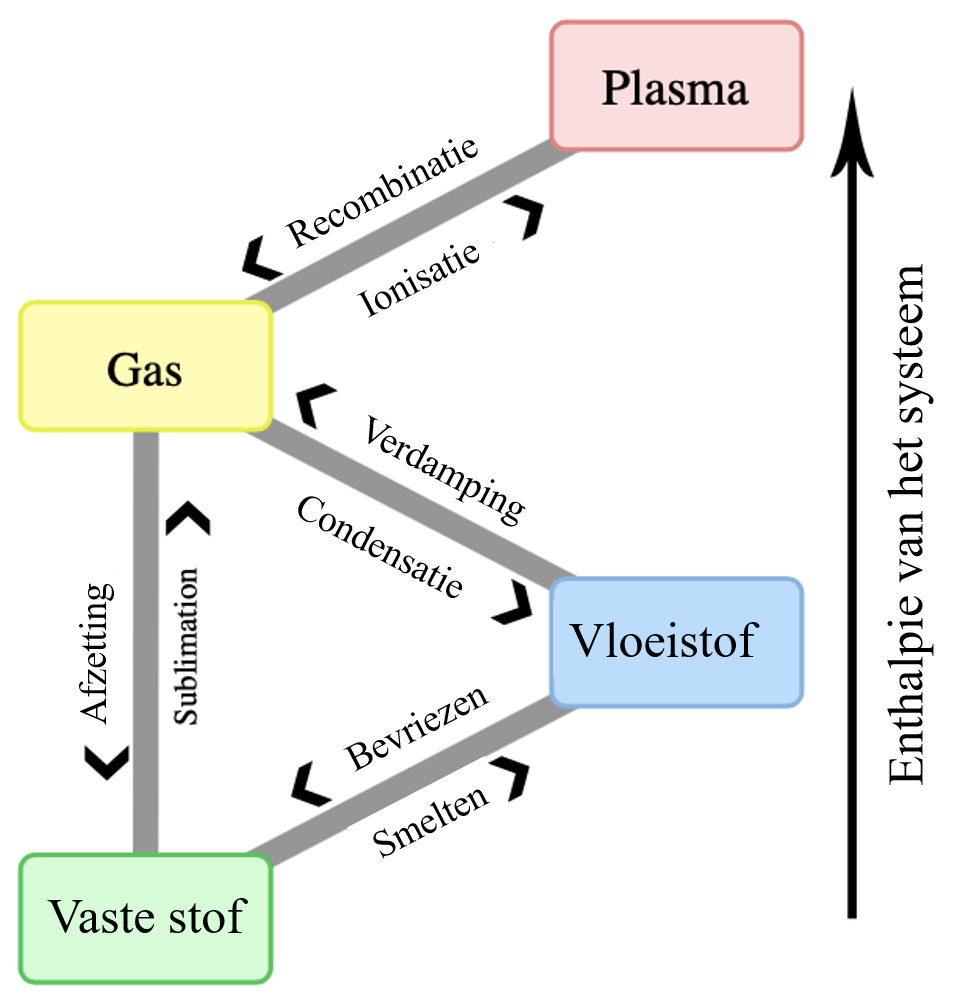
Materie komt in verschillende toestanden voor: vast, vloeibaar, gasvormig en plasma. Wanneer externe condities (zoals temperatuur of druk) veranderen, kan de aggregatietoestand eveneens veranderen. Bijvoorbeeld begint een vloeistof zoals water gas te worden wanneer het opgewarmd wordt tot zijn kookpunt of begint het te bevriezen wanneer het afgekoeld wordt tot zijn vriespunt. Een aggregatietoestand met zeer hoge energie is plasma. Hier zijn sommige van de buitenste elektronen niet langer gebonden aan atomen of moleculen. Daarom is plasma een gas van vrije elektronen en ionen.
In de natuur gebeuren vaak faseovergangen maar ze worden ook gebruikt in veel technologieën. In het bijzonder steunen verschillende deeltjesdetectors op faseovergangen. Bovendien kan hoge energie fysicaonderzoek een zelfs nog meer energetische aggregatietoestand maken, het zogenaamde quark-gluon plasma.
Daarom verstrekt hoge energie fysica een vruchtbare en opwindende context om de aggregatietoestanden en faseovergangen te bespreken met je leerlingen. Daarenboven zijn er verschillende leuke experimenten die leerlingen toelaten de verschijnselen zelfstandig te bestuderen. Hieronder stellen we enkele van onze favoriete experimenten voor en leggen we uit hoe deze te verbinden met de CERN fysica en technologieën. Wanneer deze experimenten gebruikt worden met leerlingen, moet je hen eerst laten voorspellen waar het experiment toe leidt, eer het experiment uit te voeren en het resultaat te bekijken.
Verdamping – van vloeistof naar gas
Wanneer je water verwarmt tot zijn kookpunt, beginnen er zich bellen van waterdamp te vormen als het water verandert van vloeistof in gasvormige toestand. Hierop lijkend beginnen bellen zich te vormen, wanneer een fles met spuitwater geopend wordt. Hier zal het afnemen van druk veroorzaakt door het openen van de dop het verdampingsproces doen beginnen.
Een interessant effect kan gezien worden aan oppervlakken waarin zich kleine verontreinigingen bevinden, bijvoorbeeld cellulosedraden binnen een glas. Deze verontreinigingen zorgen voor de startpunten voor het vormen van bellen, de zogenoemde condensatiekernen. Wanneer spuitwater in een glas geschonken wordt, worden kleine hoeveelheden gas opgesloten binnenin of rond kleine stofdeeltjes zoals cellulosedraden.
Een zeer vergelijkbaar principe vormt de basis van de techniek van het bellenvat voor het detecteren van deeltjes. Bellenvaten worden gevuld met super verhitte vloeistof die op het punt staat te veranderen in gas. Daarom zal iedere kleine verstoring of verontreiniging het proces van het vormen van bellen binnenin het bellenvat doen beginnen. Inderdaad, als er ioniserende deeltjes door die super verhitte vloeistof vliegen, zullen ze de moleculen op hun weg ioniseren. Deze ionen zullen dan optreden als condensatiekernen en er zullen bellen errond gevormd worden. Op die manier kan de baan van een ioniserend deeltje dat een spoor van ionen achterlaat zichtbaar gemaakt worden door het nemen van foto’s op het juiste ogenblik. (Vind hier meer over bellenvaten).
Tegenwoordig worden bellenvaten niet langer gebruikt voor onderzoek in CERN. Evenwel hebben ze onlangs een nieuwe rol gekregen in het donkere materie onderzoek, bijvoorbeeld in het PICO project in Canada.
Hands-on experimenteren met verdamping: dansende krenten in spuitwater

Een van onze favoriete experimenten is het ‘dansende krenten experiment’ dat de leerlingen toelaat de rol van de condensatiekernen te bestuderen in spuitwater.
Materiaal
- Een glas
- Spuitwater (of gelijk welk andere bruisende en transparente drank)
- Enkele krenten
Procedure
- Vul een glas met een bruisende vloeistof.
- Voeg enkele krenten toe.
- Bekijk de krenten, in het bijzonder hun beweging.
Veranderingen
- Je kan ook andere soorten van mogelijke ‘dansers’ bestuderen of andere soorten van bruisende vloeistoffen, bijvoorbeeld verschillende soorten nootjes, bevroren blauwe bessen, linzen, granen etc. Tracht de beste combinatie te vinden.
- Voeg krenten onmiddellijk aan de fles spuitwater toe en vergelijk hun beweging met en zonder dop.
Uitleg
De krenten zullen weldra beginnen op en neer te bewegen in het bruisend water. Wat gebeurt er? Het oppervlak van de krenten is niet zo glad als dat van het oppervlak van het glas. Het oppervlak van de krenten bevat veel draadjes die dienstdoen als condensatiekernen. Daarom zullen kleine bellen van koolstofdioxide gevormd worden aan het oppervlak van de krenten. Als er genoeg gasbellen vastgehecht zijn aan het oppervlak van een krent, zal deze beginnen op te stijgen naar het oppervlak (drijven, wet van Archimedes). Eens dat de krenten de bovenkant bereiken knallen ze uiteen omdat ze in contact komen met de lucht. Zonder hun luchtbellen gaan de krenten weer zinken.
Smelten – van vast naar vloeistof
Wanneer de energie van een stof toeneemt, bijv. bij het toevoeren van warmte of bij het uitoefenen van druk zal een vaste stof eventueel een vloeistof worden.
Bijvoorbeeld zullen ijsblokjes of een waskaars smelten bij het toevoeren van warmte, waarbij de druk gelijk blijft. Vaste stoffen zoals ijs of was verschillen echter wat betreft hun smeltpunten. Terwijl ijs smelt bij een temperatuur van ongeveer 0°C, smelt was bij ongeveer 40°C. Wanneer een stof zijn smeltpunt bereikt, neemt de temperatuur van de stof niet verder toe zelfs als er een constante warmte wordt toegevoerd, zo lang dat er nog enige vaste stof overblijft om te smelten. De toegevoerde warmte voor het smelten van de vaste stof wordt ook aangeduid als de latente warmte. Alleen als al de vaste stof veranderd is in vloeibare toestand begint de temperatuur terug te stijgen.
Hands-on experimenteren met smelten: koelbad
Tussen al de experimenten waarmee leerlingen het smeltproces kunnen bestuderen, is het maken van een koelbad het meest “cool”. Alle grapjes terzijde gelaten, het is echt koel! Bovendien, koeling is essentieel voor de werking van de LHC. Bezoek de cryogenische webpagina van CERN voor meer informatie.
De minimum temperatuur van een gewoon ijs-water mengsel is het smeltpunt van ijs 0°C. Je zou zulk een mengsel als een koelbad, bijv. voor het koelen van een fles frisdrank kunnen gebruiken. Evenwel is er een truk om je koelbad nog kouder te maken, bijv. om je frisdrank nog beter af te koelen. Het smeltpunt van een stof zoals ijs kan verlaagd worden door zout toe te voegen zoals natriumchloride. Daarom krijgen we uiteindelijk een ijs-water mengsel met een lagere temperatuur dan een ijs-water mengsel.
Materiaal

- Water, koud
- Zout
- Geplet ijs (alternatief: ijsblokjes, plastic zak en hamer), de verhouding zout: ijs moet 1 : 3 zijn
- Thermometer(alternatief: multimeter met een temperatuursensor, tot -20°C)
- Bekerglas, 600 ml
- Bekerglas, 400 ml
- Lepel
Opmerking over veiligheid
- Gebruik glas bestand tegen koude.
- Hou jongere leerlingen in het oog als ze werken met koelbaden.
Procedure
- Plaats de glasbeker van 400 ml in de glasbeker van 600 ml om een isolerend vat te maken.
- Voeg geplet ijs toe aan de binnenste glasbeker.
- Voeg genoeg koud water toe om het ijs te bedekken.
- Meet de temperatuur van het water-ijs mengsel (dat zou ongeveer 0°C moeten zijn).
- Voeg zout toe (vergeet niet dat de verhouding zout : ijs 1 : 3 moet zijn).
- Roer in het mengsel tot het ijs smelt.
- Meet de temperatuur van het water-ijs-zout mengsel (dit kan gaan tot -20°C).
Hands-on experimenteren met smelten: drijven van ijs
Een ander echt “cool”experiment is te bestuderen hoe smeltende ijsbergen invloed hebben op het peil van de zee of hoe smeltende ijsblokjes invloed hebben op het peil van je zoet zomerdrankje.
Omdat zoutwater (of suikerwater) een grotere massadichtheid heeft dan water, is de drijfkracht uitgeoefend op ijs groter. Dus zinken ijsblokjes niet zoveel in zoutwater (of suikerwater) als dat ze zouden doen in water. Daarom zal het peil van zoutwater (of suikerwater) stijgen, wanneer de ijsblokjes smelten, terwijl voor water het gelijk blijft. Dit effect treedt op als de ijsblokjes in je zoet zomerdrankje smelten. Ongelukkig , het versterkt ook de negatieve effecten van de klimaatsverandering: ijsbergen zijn grote brokken ijs die afbreken van gletsers (bijv. in Groenland). Ze bestaan uit water, niet uit zoutwater. Dus zal het peil van de zee niet alleen toenemen omdat er ijsbergen op zee gaan drijven maar ook wanneer ze smelten.
Materiaal

- Water, koud
- Zout (o6 suiker)
- 6 ijsblokjes
- 2 Bekerglazen, 50ml
- Lepel
Procedure
- Vul de 2 bekerglazen halfvol met water.
- Voeg 3-4 theelepels zout (of suiker) toe aan een beker en roer.
- Plaats 3 ijsblokjes in elk bekerglas.
- Voeg water toe aan het zoutwater (of suikerwater) tot het vloeistofpeil gelijk is in beide bekerglazen en roer.
- Markeer het vloeistofpeil op beide bekerglazen.
- Wacht tot de ijsblokjes gesmolten zijn.
Bijkomende Informatie
Je kan ook zien dat de ijsblokjes trager smelten in zoutwater (of suikerwater) dan in water. Dit is een ander gevolg van de hogere massadichtheid van zoutwater (of suikerwater) in vergelijking met water.
Wist je dat CERN betrokken is bij de Duurzame Ontwikkelings Doelstellingen? Vind meer over hoe CERN bijdraagt aan een betere planeet op de kennis overdracht website van CERN.
Condensatie – van gas naar vloeistof
De nevelkamer was een van de eerste deeltjesdetectors. Hier is het meest belangrijke aspect een supergekoelde superverzadigde alcoholdamp, dat in essentie een zeer koud en zeer nat gas is, dat echt een vloeistof wil worden. Inderdaad kan iedere verstoring van deze damp het condensatieproces opstarten. Wanneer de ioniserende deeltjes met hoge energie door deze damplaag vliegen, laten ze een spoor van ionen achter zich. Deze ionen triggeren dan het condensatieprocess door op te treden als condensationkernen. Daardoor verandert het spoor van ionen in een spoor van kleine druppels die kunnen bekeken worden met je ogen of door een camera onder de juiste belichting. Dit relatief eenvoudig principe liet deeltjesfysici reeds 100 jaar geleden toe om de banen van deeltjes op te nemen.
Vandaag onderzoekt het CLOUD experiment van CERN de vorming van wolken om meer te weten te komen over de klimaatsverandering. Interesse? Bekijk een les op TED door Kirby, Richer & Comes (2016): Bewolkte verandering van klimaat: Hoe wolken invloed hebben op de temperatuur van de aarde.
Hands-on experimenteren met condensatie: een wolk in een fles
Er zijn verschillende experimenten waarbij leerlingen condensatie kunnen bestuderen. De wolk in het fles experiment toont op een aangrijpende manier aan, hoe het vlug dalen van de druk de faseverandering van het condenseren kan triggeren. Er zijn verschillende videos en instructies online over hoe een wolk in een fles te maken. Afhankelijk van de inspanning en de uitrusting zal het effect zo indrukwekkend zijn als bij een demonstratie of zo gemakkelijk te doen op een veilige manier als bij een hands-on experiment. Daarom belichten we onze favoriete twee methodes hieronder. Als je beschikt over droog ijs,Thus, we highlight our favourite two methods below. If you have access to dry ice, you can also let your students kan je je leerlingen hun eigen nevelkamer laten bouwen met droog ijs en isopropanol alcohol.

1. Opvallende demonstratie
Materiaal
- 30 ml ontsmettingsmiddel (ongeveer 70% alcohol, of zuiverder alcohol)
- Een bus stofreiniger
- Een transparente PET fles van 1 l
- Water en bloem
Opmerking over veiligheid
- Draag veiligheidsbril om je ogen te beschermen tegen spatten en onvoorziene uitzettingen van je PET fles.
- Draag ook handschoenen om je huid te beschermen tegen alcohol, in het bijzonder als je zeer zuivere alcohol gebruikt.
Procedure
- Maak een klein gat in de dop van de fles om de bus stofreiniger erin te kunnen drukken.
- Gebruik een mengsel van meel en water om de opening af te sluiten (alternatieven: herbruikbare plakgum, boetseerklei, lijm …).
- Voeg 30 ml ontsmettingsmiddel (of relatief zuivere alcohol) in de PET fles toe en keer de fles om zodat je zeker bent dat de binnenkant bedekt is met alcohol.
- Plaats de dop er voorzichtig op, alle verbindingen moeten luchtdicht zijn.
- Pomp ongeveer 20 keer stofreiniger in de afgesloten fles.
- Open voorzichtig de dop (opgelet voor de druk die zich kan opbouwen!).
- Nu zou je een zeer dichte wolk moeten zien bestaande uit druppels alcohol in je fles.
Veranderingen
- Je kan ook een bal- of fietspomp gebruiken om de druk binnenin de fles te vergroten – evenwel kan het dat je enige bijkomende condensatiekernen moet toevoegen in dit geval.
- Bijkomende condensatiekernen: open de dop, knijp zachtjes op de fles en blaas een lucifer uit recht tegenover de dop, los de druk op de fles om enige rookdeeltjes op te zuigen (de rook zal zorgen voor bijkomende condensatiekernen).
- Het werkt ook met water in plaats van met alcohol maar het is niet zo overtuigend.
2. Gemakkelijk hands-on experiment
Materiaal
- 10 ml ontsmetter (ongeveer 70% alcohol of zuiverder alcohol)
- Een transparante PET fles van 0,5 l
- Een lucifer
Opmerking over veiligheid
- Draag een veiligheidsbril om je ogen te beschermen tegen alcoholspatten.
- Draag veiligheidshandschoenen om je huid te beschermen tegen alcohol, in het bijzonder als je zeer zuivere alcohol gebruikt.
- Je moet de leerlingen de nodige begeleiding geven gedurende deze activiteit.
- Als de leerlingen jong zijn zullen slechts de labohulp en de leraars lucifers gebruiken om er zeker van te zijn dat er geen leerling per ongeluk de alcohol binnen de fles in brand steekt.
Procedure
- Voeg de ontsmetter (of zuivere alcohol) in de PET fles.
- Sluit de fles met de dop.
- Draai de fles om er zeker van te zijn dat het binnenste oppervlak bedekt is met alcohol.
- Open nu de dop, knijp zachtjes op de fles en blaas een lucifer uit recht tegenover de dop.
- Los de druk op de fles om enige rookdeeltjes op te zuigen (de rook zal zorgen voor bijkomende condensatiekernen).
- Sluit de dop!
- Knijp de fles zoveel als je kan en los plots de druk van je handen.
- Nu zou je een wolk moeten zien ontstaan binnen de fles.
Bedankingen
Dit artikel is oorspronkelijk gepubliceerd als een onderwijsmodule van CERN.
Resources
- Bekijk een video van het krenten experiment op Twitter of Facebook.
- Je kan de video van het krenten experiment inladen van CERN CDS Videos.
- Aggregatietoestanden en superkoelen: een overzicht.
- Meer experimenten over faseovergangen en aggregatietoestanden.





